Производные (s)-энантиомера 2-бром-5-(2-хлор-4- трифторметилфенокси)бензоата, обладающие гербицидной активностьюПатент на изобретение №: 2049772 Автор: Йожеф Бакош[HU], Балинт Хейл[HU], Имре Тот[HU], Бела Едеш[HU], Иштван Гебхардт[HU], Ференц Бихари[HU], Анна Дурко[HU], Дьюла Ейферт[HU], Йене Кирай[HU], Ева Конок[HU], Ласло Лукач[HU], Агнеш Месарощ[HU], Бела Радвани[HU], Лайош Шароши[HU] Патентообладатель: Будапешти Ведьимювек (HU) Дата публикации: 10 Декабря, 1995 Адрес для переписки: подача заявки15.11.1991 публикация патента10.12.1995 Изображения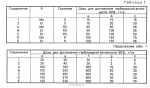  Использование: в качестве вещества, обладающего гербицидной активностью. Сущность изобретения: продукт ф-лы: 2-Cl-4CF3-C6H3-O-4-Br-3-(COOCH(CH3)COOR)C6H3 где R-метил или этил в виде (S)-изомера. Реагент 1: алкил(S)-лактат. Реагент 2: 2-бром-5-(2-хлор-4-трифторметилфенокси)бензоилхлорид. 3 табл. , ОПИСАНИЕ ИЗОБРЕТЕНИЯ К ПАТЕНТУИзобретение относится к гербицидноактивным (S)-1"-метоксикарбонилэтил 2-бром-5-(2-хлор-4-трифторметилфенокси) бензоату и (S)-1"-этоксикарбонилэтил 2-бром-5-(2-хлор-4-трифторметилфенокси) бензоату. В патенте ФРГ (DE-PS) N 3029728 описаны замещенные дифенилэфирные производные общей формулы I F3C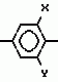 O O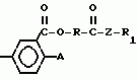 где А представляет собой галоген или цианогруппу; Х представляет собой водород или галоген; Y представляет собой водород или галоген; Z представляет собой кислород или серу; R представляет собой С1-С3 алкиленовую группу, в определенных случаях замещенную С1-С4 алкильной группой, и R1 представляет собой С1-С10 алкильную группу. В патенте ФРГ (DE-PS) N 3029728 описано одно индивидуальное, а именно (RS)-1"-этоксикарбонилэтил 2-бром-5-(2-хлор-4-трифторметилфенокси)бензоат, а также его гербицидные свойства. Указано, что это соединение эффективно даже при дозе, в 2 раза меньшей (140 г/га) по сравнению с известным втор-бутил 5-(2-хлор-4-трифторметилфенокси)-2-нитробензоатом. Однако не приводится никакого описания (инструкций) порогового значения селективности в отношении культурных растений. В указанной выше ссылке не приводится описание способа получения, физических, химических, а также гербицидных свойств обоих соединений по настоящему изобретению, таким образом, эти соединения не были получены и поэтому являются новыми. Общеизвестно, что постоянно существует необходимость на разработку новых соединений, способных подавлять развитие нежелательной растительности. Целью исследований является в большинстве случаев получение соединений с селективной способностью подавлять развитие сорняков на посевах наиболее распространенных культур, таких как пшеница, маис, рис, соевые бобы или хлопок, а именно неконтролируемый рост сорняков сопровождается значительными потерями урожая, в результате чего доход производителя (фермера) снижается и затраты покупателя становятся выше. В процессе исследований в области защиты растений было обнаружено, что соединения по изобретению (соединение 1 и 2) обладают значительно более высокой гербицидной активностью, чем (R)-антиподы (D и Е) или (RS)-1"-метоксикарбонилэтил 2-бром-5-(2-хлор-4-трифторметилфенокси) бензоат (соединение А) или (RS)-1"-этоксикарбонилэтил 2-бром-5-(2-хлор-4-трифторметилфенокси)-бензоат (соединение В), описанные в патенте ФРГ 3029728, или (RS)-1"-этоксикарбонилэтил-5-(2-хлор-4-трифтор- метилфенокси)-2-нитробензоат (соединение С), заявленное в опубликованной заявке на Европейский патент N 002052 AL. Однако пороговые величины селективности соединений по изобретению (соединения 1 и 2) равны аналогичным характеристикам соединений А, В или С. Гербицидная активность соединений 1 и 2 выше 90% выраженная в г/га, в 3-17 раз выше гербицидной активности рацематов А, В и С и в 4-22 раза выше гербицидной активности R-антиподов Д и Е, соответственно (табл. 1), факт, совершенно неожиданный для специалистов в этой области. Далее из равенства пороговых значений селективности (см. табл. 2) заключили, что соединения А, В, С, Д и Е являются фитотоксичными, а именно, они опасны для культурных растений в дозе, убивающей сорняки (50,500 г/га), поскольку эта доза существенно выше порогового значения селективности (30-200 г/га) культурных растений. В противоположность соединениям А, В, С, Д и Е оба соединения по изобретению могут быть использованы для уничтожения сорняков на посевах культурных растений, поскольку порог их селективности (50-180 г/га) во много раз превышает дозу (10-40 г/га), требуемую для достижения гербицидной эффективности выше 90% Зная гербицидную активность и порог селективности соединений 1 и 2 по изобретению, особенно по сравнению с соединениями А, В, С, Д и Е, можно отметить, что необыкновенная гербицидная активность и порог селективности соединений 1 и 2 по изобретению, и кроме того, прекрасная приспособленность этих соединений к использованию в результате сочетания обеих указанных характеристик, что является полной неожиданностью для специалистов, не отмечались у соединений аналогичного строения. Оба соединения по изобретению можно получить известными способами, а именно путем а) реакции (S) энантиомера или рацемата эфира молочной кислоты общей формулы III HO- где А представляет собой галоген или цианогруппу; Х представляет собой водород или галоген; Y представляет собой водород или галоген; Z представляет собой кислород или серу; R представляет собой С1-С3 алкиленовую группу, в определенных случаях замещенную С1-С4 алкильной группой, и R1 представляет собой С1-С10 алкильную группу. В патенте ФРГ (DE-PS) N 3029728 описано одно индивидуальное, а именно (RS)-1"-этоксикарбонилэтил 2-бром-5-(2-хлор-4-трифторметилфенокси)бензоат, а также его гербицидные свойства. Указано, что это соединение эффективно даже при дозе, в 2 раза меньшей (140 г/га) по сравнению с известным втор-бутил 5-(2-хлор-4-трифторметилфенокси)-2-нитробензоатом. Однако не приводится никакого описания (инструкций) порогового значения селективности в отношении культурных растений. В указанной выше ссылке не приводится описание способа получения, физических, химических, а также гербицидных свойств обоих соединений по настоящему изобретению, таким образом, эти соединения не были получены и поэтому являются новыми. Общеизвестно, что постоянно существует необходимость на разработку новых соединений, способных подавлять развитие нежелательной растительности. Целью исследований является в большинстве случаев получение соединений с селективной способностью подавлять развитие сорняков на посевах наиболее распространенных культур, таких как пшеница, маис, рис, соевые бобы или хлопок, а именно неконтролируемый рост сорняков сопровождается значительными потерями урожая, в результате чего доход производителя (фермера) снижается и затраты покупателя становятся выше. В процессе исследований в области защиты растений было обнаружено, что соединения по изобретению (соединение 1 и 2) обладают значительно более высокой гербицидной активностью, чем (R)-антиподы (D и Е) или (RS)-1"-метоксикарбонилэтил 2-бром-5-(2-хлор-4-трифторметилфенокси) бензоат (соединение А) или (RS)-1"-этоксикарбонилэтил 2-бром-5-(2-хлор-4-трифторметилфенокси)-бензоат (соединение В), описанные в патенте ФРГ 3029728, или (RS)-1"-этоксикарбонилэтил-5-(2-хлор-4-трифтор- метилфенокси)-2-нитробензоат (соединение С), заявленное в опубликованной заявке на Европейский патент N 002052 AL. Однако пороговые величины селективности соединений по изобретению (соединения 1 и 2) равны аналогичным характеристикам соединений А, В или С. Гербицидная активность соединений 1 и 2 выше 90% выраженная в г/га, в 3-17 раз выше гербицидной активности рацематов А, В и С и в 4-22 раза выше гербицидной активности R-антиподов Д и Е, соответственно (табл. 1), факт, совершенно неожиданный для специалистов в этой области. Далее из равенства пороговых значений селективности (см. табл. 2) заключили, что соединения А, В, С, Д и Е являются фитотоксичными, а именно, они опасны для культурных растений в дозе, убивающей сорняки (50,500 г/га), поскольку эта доза существенно выше порогового значения селективности (30-200 г/га) культурных растений. В противоположность соединениям А, В, С, Д и Е оба соединения по изобретению могут быть использованы для уничтожения сорняков на посевах культурных растений, поскольку порог их селективности (50-180 г/га) во много раз превышает дозу (10-40 г/га), требуемую для достижения гербицидной эффективности выше 90% Зная гербицидную активность и порог селективности соединений 1 и 2 по изобретению, особенно по сравнению с соединениями А, В, С, Д и Е, можно отметить, что необыкновенная гербицидная активность и порог селективности соединений 1 и 2 по изобретению, и кроме того, прекрасная приспособленность этих соединений к использованию в результате сочетания обеих указанных характеристик, что является полной неожиданностью для специалистов, не отмечались у соединений аналогичного строения. Оба соединения по изобретению можно получить известными способами, а именно путем а) реакции (S) энантиомера или рацемата эфира молочной кислоты общей формулы III HO-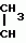 - -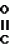 -O-R где R представляет собой метил или этилгруппу, с по меньшей мере стехиометрическим количеством 2-бром-5-(2-хлор-4-трифторметилфенокси)бензоилгалоида, предпочтительно хлорида, желательно в присутствии связывающего кислоту агента; или в) реакции (S) энантиомера или рацемата алкил 2-галоидпропионата общей формулы IV Hal- -O-R где R представляет собой метил или этилгруппу, с по меньшей мере стехиометрическим количеством 2-бром-5-(2-хлор-4-трифторметилфенокси)бензоилгалоида, предпочтительно хлорида, желательно в присутствии связывающего кислоту агента; или в) реакции (S) энантиомера или рацемата алкил 2-галоидпропионата общей формулы IV Hal-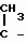 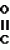 -O-R где R представляет собой метил или этилгруппу и Наl представляет собой хлор или бром, с 2-бром-5-(2-хлор-4-трифторметилфенокси)-бензойной кислотой, предпочтительно в присутствии аза-соединия, например 1,5-диазабицикло (5,4,0)-ундец-5-ена (ДБУ) и повторного растворения полученного продукта в том случае, когда один из реагентов представляет собой рацемическое соединение. При осуществлении описанных реакций можно использовать любой инертный растворитель. Подходящими растворителями являются, например, пентан, гексан, гептан, циклогексан, петролейный эфир, бензин, лигроин, бензол, толуол, ксилол, дихлорметан, дихлорэтан, хлороформ, четыреххлористый углерод, хлорбензол, о-дихлорбензол, диэтиловый эфир, дибутиловый эфир, этиленгликоль диметиловый эфир, тетрагидрофуран, диоксан, ацетон, метилэтилкетон, метилизопропилкетон, метилизобутилкетон, метилацетат, этилацетат, ацетонитрил, пропионитрил, диметилформамид (ДМФ), N-метилпирролидон, диметилсульфоксид (ДМСО), тетраметилансульфон, гексаметилфосфорной кислоты триамид. Гидроокиси, бикарбонаты, карбонаты и алкоголяты щелочных металлов, а также алифатические, ароматические или гетероциклические амины являются полезными связывающими кислоту агентами. В соответствии с предпочтительным вариантом воплощения изобретения примерно эквимолярные количества исходных материалов вводят во взаимодействие при температуре от -20о до температуры кипения реакционной смеси. Предпочтительно раствор 2-бром-5-(2-хлор-4-трифторметилфенокси)бензойной кислоты или 2-бром-5-(2-хлор-4-трифторметилфенокси)бензоила хлорида по частям добавляют между -20 и 35оС и после такого добавления реакционную смесь перемешивают при температуре дефлегмации до необходимого превращения. После охлаждения раствор промывают разведенной кислотой, затем разбавленным основанием и водой и, таким образом, разделяют фазы. Целевой продукт можно получить любым известным способом, например, путем выпаривания. Изобретение также относится и гербицидной композиции, включающей (S)-1"-метоксикарбонилэтил 2-бром-5-(2-хлор-4-трифтор-метилфенокси)бензоат или (S)-1"-этоксикарбонилэтил 2-бром-5-(2-хлор-4-трифторметилфенокси)бензоат в качестве активного ингредиента в количестве 0,01-95 мас. вместе с одним или более твердым и/или жидким носителем (лями), предпочтительно зерна природных или синтетических материалов; и/или с инертным (и) растворителем (лями), предпочтительно ксилол и/или циклогексанон; и при необходимости с поверхностно активным веществом, предпочтительно анионным и/или неионным эмульгирующим или диспергирующим агентом. Изобретение ниже проиллюстрировано неограничивающими примерами. В данным 1Н ЯМР и 13С ЯМР, приведенных в примерах, использован метод идентификации, показанный на общей формуле V F3C -O-R где R представляет собой метил или этилгруппу и Наl представляет собой хлор или бром, с 2-бром-5-(2-хлор-4-трифторметилфенокси)-бензойной кислотой, предпочтительно в присутствии аза-соединия, например 1,5-диазабицикло (5,4,0)-ундец-5-ена (ДБУ) и повторного растворения полученного продукта в том случае, когда один из реагентов представляет собой рацемическое соединение. При осуществлении описанных реакций можно использовать любой инертный растворитель. Подходящими растворителями являются, например, пентан, гексан, гептан, циклогексан, петролейный эфир, бензин, лигроин, бензол, толуол, ксилол, дихлорметан, дихлорэтан, хлороформ, четыреххлористый углерод, хлорбензол, о-дихлорбензол, диэтиловый эфир, дибутиловый эфир, этиленгликоль диметиловый эфир, тетрагидрофуран, диоксан, ацетон, метилэтилкетон, метилизопропилкетон, метилизобутилкетон, метилацетат, этилацетат, ацетонитрил, пропионитрил, диметилформамид (ДМФ), N-метилпирролидон, диметилсульфоксид (ДМСО), тетраметилансульфон, гексаметилфосфорной кислоты триамид. Гидроокиси, бикарбонаты, карбонаты и алкоголяты щелочных металлов, а также алифатические, ароматические или гетероциклические амины являются полезными связывающими кислоту агентами. В соответствии с предпочтительным вариантом воплощения изобретения примерно эквимолярные количества исходных материалов вводят во взаимодействие при температуре от -20о до температуры кипения реакционной смеси. Предпочтительно раствор 2-бром-5-(2-хлор-4-трифторметилфенокси)бензойной кислоты или 2-бром-5-(2-хлор-4-трифторметилфенокси)бензоила хлорида по частям добавляют между -20 и 35оС и после такого добавления реакционную смесь перемешивают при температуре дефлегмации до необходимого превращения. После охлаждения раствор промывают разведенной кислотой, затем разбавленным основанием и водой и, таким образом, разделяют фазы. Целевой продукт можно получить любым известным способом, например, путем выпаривания. Изобретение также относится и гербицидной композиции, включающей (S)-1"-метоксикарбонилэтил 2-бром-5-(2-хлор-4-трифтор-метилфенокси)бензоат или (S)-1"-этоксикарбонилэтил 2-бром-5-(2-хлор-4-трифторметилфенокси)бензоат в качестве активного ингредиента в количестве 0,01-95 мас. вместе с одним или более твердым и/или жидким носителем (лями), предпочтительно зерна природных или синтетических материалов; и/или с инертным (и) растворителем (лями), предпочтительно ксилол и/или циклогексанон; и при необходимости с поверхностно активным веществом, предпочтительно анионным и/или неионным эмульгирующим или диспергирующим агентом. Изобретение ниже проиллюстрировано неограничивающими примерами. В данным 1Н ЯМР и 13С ЯМР, приведенных в примерах, использован метод идентификации, показанный на общей формуле V F3C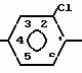 O O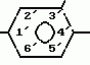 Br П р и м е р 1. Получение (S)-1"-метоксикарбонилэтила 2-бром-5-(2-хлор-4-трифторметилфенокси)бензоата (соединение 1) 100 мл бензола, 28,6 г (0,2747 моль) метил (S)-лактата / / Br П р и м е р 1. Получение (S)-1"-метоксикарбонилэтила 2-бром-5-(2-хлор-4-трифторметилфенокси)бензоата (соединение 1) 100 мл бензола, 28,6 г (0,2747 моль) метил (S)-лактата / / /D20=-8,97о (ядро)/ и 22,3 мл (0,2747 моль) безводного пиридина смешали в трехгорлой колбе, оборудованной мешалкой, капельной воронкой и обратным холодильником. Смесь охладили до 10оС и раствор, содержащий 113,7 г (0,2747 моль) 2-бром-5-(2-хлор-4-трифторметилфенокси)бензоилхлорида в 100 мл бензола по каплям добавили при энергичном перемешивании при такой скорости, что температура реакционной смеси оставалась между 10 и 20оС при внешнем охлаждении. После этой процедуры суспензию перемешивали при 20-30оС еще 10 ч и затем ее влили в 300 мл 3% -ного раствора соляной кислоты. После разделения органическую фазу последовательно промыли 200 мл 3%-ного раствора бикарбоната натрия, насыщенного хлористым натрием, и затем 200 мл насыщенного водного раствора хлористого натрия. После обезвоживания бензольного раствора надо безводным сульфатом магния растворитель выпарили при атмосферном давлении, а затем с помощью водоструйного насоса. Указанное в названии соединение получили в виде светло-желтого маслянистого продукта с выходом 110,2 г (92,7%). Мол. м. 481,4. Цвет и форма: светло-желтое масло. nD20 +9,21о(с 7,385 бензол). nD20 1,5424. Данные масс-спектрографии показывают, что указанное в названии соединение имеет изотропическое отношение характеристики соединений, содержащих один атом хлора и один атом брома. m/t(r,i)=482(280)= F3C(Cl)C6H3OC6H3(Br)COOCH(CH3)COOCH3 480(210)=F3C(Cl)C6H3OC6H3(Br)COOCH(CH3)COOCH3 381(230) F3C(Cl)C6H3OC6H3(Br)CO 379(1000) F3C(Cl)C6H3OC6H3(Br)CO 377(710) F3C(Cl)C6H3OC6H3(Br)CO 1H ЯМР (СDCl3): /D20=-8,97о (ядро)/ и 22,3 мл (0,2747 моль) безводного пиридина смешали в трехгорлой колбе, оборудованной мешалкой, капельной воронкой и обратным холодильником. Смесь охладили до 10оС и раствор, содержащий 113,7 г (0,2747 моль) 2-бром-5-(2-хлор-4-трифторметилфенокси)бензоилхлорида в 100 мл бензола по каплям добавили при энергичном перемешивании при такой скорости, что температура реакционной смеси оставалась между 10 и 20оС при внешнем охлаждении. После этой процедуры суспензию перемешивали при 20-30оС еще 10 ч и затем ее влили в 300 мл 3% -ного раствора соляной кислоты. После разделения органическую фазу последовательно промыли 200 мл 3%-ного раствора бикарбоната натрия, насыщенного хлористым натрием, и затем 200 мл насыщенного водного раствора хлористого натрия. После обезвоживания бензольного раствора надо безводным сульфатом магния растворитель выпарили при атмосферном давлении, а затем с помощью водоструйного насоса. Указанное в названии соединение получили в виде светло-желтого маслянистого продукта с выходом 110,2 г (92,7%). Мол. м. 481,4. Цвет и форма: светло-желтое масло. nD20 +9,21о(с 7,385 бензол). nD20 1,5424. Данные масс-спектрографии показывают, что указанное в названии соединение имеет изотропическое отношение характеристики соединений, содержащих один атом хлора и один атом брома. m/t(r,i)=482(280)= F3C(Cl)C6H3OC6H3(Br)COOCH(CH3)COOCH3 480(210)=F3C(Cl)C6H3OC6H3(Br)COOCH(CH3)COOCH3 381(230) F3C(Cl)C6H3OC6H3(Br)CO 379(1000) F3C(Cl)C6H3OC6H3(Br)CO 377(710) F3C(Cl)C6H3OC6H3(Br)CO 1H ЯМР (СDCl3):  1,52 (д, 3H) 3,65 (c, 3H) 5,22 (к, 1H), 6,77-7,63 млн.д. (комплекс м. 6H). 13С ЯМР (СDCl3): 155,0 (c, C-1) 126-2 (c, C-2) 128,4 (k, 3J (FCCC) 3,6 Гц, С-3), 125,6 (к, 3J (FCCC) 3,6 Гц), 120,1 (с, С-6), 155,0 (с, С-1") 122,1 (с, С-2"), 136,1 (с, С-3") 116,6 (с, С-4"), 133,1 (с, С-5"), 123,1 (с, С-6"), 170,7 (с, СООСН3), 164,4 (с, СООСН3), 52,4 (с, ОСН3), 16,9 (с, СН3), 70,0 млн. д. (с, СН). П р и м е р 2. Получение (S)-1"-этоксикарбонилэтила 2-бром-5-(2-хлор-4-трифтор-метилфенокси)бензоата (соединение 2). 100 мл бензола, 10,1 мл (0,1252 моль) безводного пиридина и 14,3 мл (0,1252 моль) этила (S)-лактата // 1,52 (д, 3H) 3,65 (c, 3H) 5,22 (к, 1H), 6,77-7,63 млн.д. (комплекс м. 6H). 13С ЯМР (СDCl3): 155,0 (c, C-1) 126-2 (c, C-2) 128,4 (k, 3J (FCCC) 3,6 Гц, С-3), 125,6 (к, 3J (FCCC) 3,6 Гц), 120,1 (с, С-6), 155,0 (с, С-1") 122,1 (с, С-2"), 136,1 (с, С-3") 116,6 (с, С-4"), 133,1 (с, С-5"), 123,1 (с, С-6"), 170,7 (с, СООСН3), 164,4 (с, СООСН3), 52,4 (с, ОСН3), 16,9 (с, СН3), 70,0 млн. д. (с, СН). П р и м е р 2. Получение (S)-1"-этоксикарбонилэтила 2-бром-5-(2-хлор-4-трифтор-метилфенокси)бензоата (соединение 2). 100 мл бензола, 10,1 мл (0,1252 моль) безводного пиридина и 14,3 мл (0,1252 моль) этила (S)-лактата //  /D20 -12о (ядро)/ поместили в трехгорлую колбу, снабженную мешалкой, капельной воронкой и обратным холодильником. После охлаждения гомогенного раствора до 10оС к нему по каплям добавили раствор 51,8 г (0,1252 моль) 2-бром-5-(2-хлор-4-трифторметилфенокси) бензоил хлорида в 100 мл бензола, одновременно перемешивая смесь и обеспечивая внешнее охлаждение для поддержания температуры реакционной среды и дефлегмировали при этой же температуре в течение 6 ч при перемешивании. После охлаждения в реакционную смесь добавили 200 мл 3%-ного раствора соляной кислоты. После кратковременного перемешивания органическую фазу отделили и последовательно промыли 150 мл 3%-ного раствора бикарбоната натрия, насыщенного хлористым натрием, затем 150 мл водного насыщенного раствора хлористого натрия. После обезвоживания бензольного раствора над безводным сульфатом магния растворитель выпарили сначала при атмосферном давлении, а затем под давлением, создаваемым водоструйным насосом. Указанное в названии соединение получили в виде светло-желтого маслянистого продукта с выходом 55,6 г (89,4%). Молекулярный вес: 495,4. Цвет и форма: светло-желтое масло. / /D20 -12о (ядро)/ поместили в трехгорлую колбу, снабженную мешалкой, капельной воронкой и обратным холодильником. После охлаждения гомогенного раствора до 10оС к нему по каплям добавили раствор 51,8 г (0,1252 моль) 2-бром-5-(2-хлор-4-трифторметилфенокси) бензоил хлорида в 100 мл бензола, одновременно перемешивая смесь и обеспечивая внешнее охлаждение для поддержания температуры реакционной среды и дефлегмировали при этой же температуре в течение 6 ч при перемешивании. После охлаждения в реакционную смесь добавили 200 мл 3%-ного раствора соляной кислоты. После кратковременного перемешивания органическую фазу отделили и последовательно промыли 150 мл 3%-ного раствора бикарбоната натрия, насыщенного хлористым натрием, затем 150 мл водного насыщенного раствора хлористого натрия. После обезвоживания бензольного раствора над безводным сульфатом магния растворитель выпарили сначала при атмосферном давлении, а затем под давлением, создаваемым водоструйным насосом. Указанное в названии соединение получили в виде светло-желтого маслянистого продукта с выходом 55,6 г (89,4%). Молекулярный вес: 495,4. Цвет и форма: светло-желтое масло. / 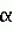 /D20= +7,77о (с 5,66 бензол). nD20 1,5324. Масс-спектрографические данные указанного в названии соединения показывают изотропическое отношение, характеризующее соединения, содержащие один атом хлора и один атом брома. m/e(r.i)=496(230)=F3C(Cl)C6H3OC6H3(Br)COOCH(CH3)COOC2H5 494(180)=F3C(Cl)C6H3OC6H3(Br)COOCH(CH3)COOC2H5 381(260) F3C(Cl)C6H3OC6H3BrCO 379(1000) F3C(Cl)C6H3OC6H3BrCO 377(710) F3C(Cl)C6H3OC6H3BrCO 1Н ЯМР (СDCl3): /D20= +7,77о (с 5,66 бензол). nD20 1,5324. Масс-спектрографические данные указанного в названии соединения показывают изотропическое отношение, характеризующее соединения, содержащие один атом хлора и один атом брома. m/e(r.i)=496(230)=F3C(Cl)C6H3OC6H3(Br)COOCH(CH3)COOC2H5 494(180)=F3C(Cl)C6H3OC6H3(Br)COOCH(CH3)COOC2H5 381(260) F3C(Cl)C6H3OC6H3BrCO 379(1000) F3C(Cl)C6H3OC6H3BrCO 377(710) F3C(Cl)C6H3OC6H3BrCO 1Н ЯМР (СDCl3): 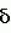 1,23 (т, 3Н), 1,55 (д, 3Н), 4,16 (к, 2Н), 5,24 (к, 1Н), 6,85-7,2 млн.д. (комплекс м, 6Н). 13С ЯМР (СDCl3): 155,0 (с, С-1) 126,2 (с, С-2) 128,5 (к, J(FCCC) 3,6 Гц, С-3), 125,6 (к, J(FCCC) 3,61 Гц, С-5) 120,1 (с, С-6) 155,0 (с, С-1"), 122,0 (с, С-2") 136,1 (с, С-3") 116,5 (с, С-4") 133,3 (с, С-5) 123,1 (с, С-6) 170,2 (с, СООСН, 164,5 (с, СООС2Н5) 61,6 (с, ОСН2) 14,1 (с, СН3СН2) 16,9 (с, СН3) 70,1 млн.д. (с, СН). П р и м е р 3. Получение (R)-1"-(метоксикарбонил)этила 2-бром-5-(2-хлор-4-трифтор-метилфенокси)-бензоата (соединение Д). Это соединение получили по методике примера 1 из метила (R)-лактата вместо метила (S)-лактата с выходом 92,7% Мол.м. 481,4. Цвет и форма: светло-желтое масло. / 1,23 (т, 3Н), 1,55 (д, 3Н), 4,16 (к, 2Н), 5,24 (к, 1Н), 6,85-7,2 млн.д. (комплекс м, 6Н). 13С ЯМР (СDCl3): 155,0 (с, С-1) 126,2 (с, С-2) 128,5 (к, J(FCCC) 3,6 Гц, С-3), 125,6 (к, J(FCCC) 3,61 Гц, С-5) 120,1 (с, С-6) 155,0 (с, С-1"), 122,0 (с, С-2") 136,1 (с, С-3") 116,5 (с, С-4") 133,3 (с, С-5) 123,1 (с, С-6) 170,2 (с, СООСН, 164,5 (с, СООС2Н5) 61,6 (с, ОСН2) 14,1 (с, СН3СН2) 16,9 (с, СН3) 70,1 млн.д. (с, СН). П р и м е р 3. Получение (R)-1"-(метоксикарбонил)этила 2-бром-5-(2-хлор-4-трифтор-метилфенокси)-бензоата (соединение Д). Это соединение получили по методике примера 1 из метила (R)-лактата вместо метила (S)-лактата с выходом 92,7% Мол.м. 481,4. Цвет и форма: светло-желтое масло. /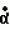 /D20 -7,83о (с 4,91 бензол)nD20 1,5424. Масс-спектрометрические данные указанного в названии продукта, данные 1Н ЯМР и 13С ЯМР совпадают с данными (S)-энантиомера, полученного в примере 1. П р и м е р 4. Получение (R)-1"-этоксикарбонил)этил-2-бром-5-(2-хлор-4-трифтор- метилфенокси)-бензоата (соединение Е). Это соединение получили по методике примера 2, используя этил (R)-лактат вместо этил (S)-лактата, с выходом 88,7% Молекулярный вес: 495,4. Цвет и форма: желтое масло./ /D20 -7,83о (с 4,91 бензол)nD20 1,5424. Масс-спектрометрические данные указанного в названии продукта, данные 1Н ЯМР и 13С ЯМР совпадают с данными (S)-энантиомера, полученного в примере 1. П р и м е р 4. Получение (R)-1"-этоксикарбонил)этил-2-бром-5-(2-хлор-4-трифтор- метилфенокси)-бензоата (соединение Е). Это соединение получили по методике примера 2, используя этил (R)-лактат вместо этил (S)-лактата, с выходом 88,7% Молекулярный вес: 495,4. Цвет и форма: желтое масло./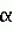 / D20 7,70о (с 4,96 бензол) nD20= 1,5352. Данные масс-спектрометрии, 1Н ЯМР и 13С ЯМР соответствуют данным (S)-энантиомера, полученного в примере 2. П р и м е р 5. а) Получение эмульгируемого концентрата (20 ЭК), мас. Соединение 2 20 2-Этоксиэтанол 10 Циклогексанон 35 Эмульсоген ЕL 360 (1) 7 Тенсиофикс СД 5 (2) 3 Ксилол 25 (1) этилоксилированное касторовое масло; (2) этилоксилированный коксовый спирт. Эмульсоген ЕL 360 и тенсиофикс СД 5 растворили в смеси 2-этоксиэтанола, циклогексанона и ксилола и затем ввели в смесь соединения 2 и перемешивали раствор в течение 2 ч. Композиции, содержащие соединение 1, соединения А, В, С, Д и Е можно получить таким же образом. в) получение эмульгируемого концентрата (35,ЭК), мас. Соединение 1 35 Циклогексанон 10 Тенсиофикс СД 21 (1) 2 Тенсиофикс В 7453 (2) 8 Ксилол 45 (1) смесь этоксилированного жирного спирта, этоксилированного нонилфенола и их фосфатов; (2) раствор кальция додецилбензолсульфоната, этоксилированного нонилфенола и этоксилированного-пропоксилированного нонилфенола в н-бутаноле. Повторили процесс, описанный в пункте а). Композиции, содержащие соединение 2, соединения А, В, С, Д и Е можно получить аналогичным способом. П р и м е р 6. Получение микрогранул, мас. Соединение 2 0,1 Циклогексанон 5,0 Бентонит 94,9 Раствор, содержащий соединение 2 в циклогексаноне, набрызгали на бентонит, предварительно измельченный до частиц размером 50 мкм и помещенный во вращающийся барабан. Перемешивание продолжали в течение 1 ч до тех пор, пока циклогексанон не испарился. Композицию, содержащую соединение 1, соединения А, В, С, Д и Е можно получить аналогично. П р и м е р 7. Получение диспергируемых в воде гранул (ДВГ), мас. Соединение 1 50 Саb-0-Sil M5 (1) 5 Атлокс 4862 (2) 3 Полифон 0 (3) 6 Геропон 1N (4) 5 Каолин 31 (1) аморфная двуокись кремния; (2) продукт конденсации нафталинсульфоната с формальдегидом; (3) связующий материал (лигнинсульфонат натрия); (4) изопропилнафталинсульфонат. Активный ингредиент смешали в измельченный раствор вместе с аморфной двуокисью кремния, атлоксом 4862 (диспергирующим агентом) и геропоном 1N (смачивающим материалом), а также с каолином. Смесь измельчили таким образом, что часть частиц размером больше 44 мкм диаметром стала меньше 0,5% Смесь смешали в месильной машине с водным раствором полифона О (связующего реагента) и затем с помощью экструдера получили гранулы диаметром 1 мм. Эти гранулы сушили в потоке воздуха. Композицию, содержащую соединение 2, соединения А, В, С, Д и Е можно получить аналогично. П р и м е р 8. Биологические испытания. Гербицидную активность и селективность соединений по изобретению сравнили с родственными по строению (R)-антиподом (соединение Д) и (RS)-1"-метоксикарбонилэтилом 2-бром-5-(2-хлор-4-трифторметилфенокси)бензоатом (соединение А), а также с (R)-антиподом (соединение Е) и (RS)-1"-этоксикарбонилэтилом 2-бром-5-(2-хлор-4-трифторметилфенокси)бензоатом (соединение В) и с имеющимся на рынке (RS)-1"-этоксикарбонилэтилом 5-(2-хлор-4-трифторметилфенокси)-2-нитро-бензоатом (соединение С) как ссылочными (стандартными) соединениями. В зависимости от вида растений равное количество (20-50) зерен каждого посадили в пластмассовые сосуды для культивирования на глубину 0,5 см, затем почву опрыскали при возникновении необходимости и сосуды содержали при оптимальной температуре и освещении. После достижения сорняками фазы 2-4 настоящих листьев или достижения культивируемыми растениями фазы 3-6 настоящих листьев, соответственно опрыскивание провели растворами с содержанием активного ингредиента 5, 15, 45, 135, 405 или 1215 г/га, соответственно. Оценку провели на 10-ый день после обработки путем определения процента поражения (L. Banki Bioassay, of Pesticides in Laboratory, Akademiai Kiado, Budapest, Hungary, 1978) и определения, таким образом, доз, необходимых для уничтожения 90% сорняков путем использования пробит-анализа (D.I.Finney: Probit-analysis, Cambridge University Press 2nd Ed. 1964). Одновременно определяли порог селективности культивируемых растений, т.е. наивысшую дозу, к которой растения устойчивы. Результаты представлены в табл. 1 и 2: а) ширина колосистая Amaranthus rehoflexus в) паслен черный Solanum nigrum c) портулак огородный Portulaca oleraceae d) непахучая матрикария Matricaria modora e) лекарственный паслен Datura shamonium f) марь белая Сhenopodium album g) Lamiem purpureum h) Vida arvensis i) рис Oryza sativa j) озимая пшеница Triticum vulgare k) озимый ячмень Hordeum vulgare e) соя Glycine soja П р и м е р 9. Полевые испытания. Это испытание провели, используя соединения 1 и 2, соответственно по изобретению и ссылочные соединения А, В, С, Д и Е, соответственно на озимой пшенице сорта Аврора на делянках в 20 м2 при четырехкратном повторении. Соединения, используемые в этих экспериментах, ввели в композиции, как описано в п.а) в примере 5. На этих делянках были следующие сорняки: Anthemis arvensis, Convolvulus arvensis, Matricaria modora, Veronica hederifolia и Stellaria media. Опрыскивание проводили 23 марта, когда Stellaria media зацветает, а другие сорняки достигли фазы развития в 10 см. Гербицидная активность указанных композиций определялась в конце 3-ей недели после опрыскивания (L. Banke: Bioassay of Pesticides in the Laboratory, Akademiai Kiado, Budapest, 1978). За исключением Stellaria media 100% сорняков были уничтожены при всех обработках. Важное отличие, касающееся гербицидной активности нa Stellaria media наблюдалось между соединениями по настоящему изобретению и ссылочными соединениями. Stellaria media уничтожалась преимущественно соединениями по настоящему изобретению, в то время как ссылочные соединения были неактивны. Уничтожение Stellaria media на полях, обработанных в дозе 50 г/га ссылочными соединениями, достигало 50% Значительное различие существует между фитотоксичностью по отношению к озимой пшенице у соединений по изобретению и ссылочных соединений. Данные, полученные на озимой пшенице и Stellaria media приведены в табл. 3. / D20 7,70о (с 4,96 бензол) nD20= 1,5352. Данные масс-спектрометрии, 1Н ЯМР и 13С ЯМР соответствуют данным (S)-энантиомера, полученного в примере 2. П р и м е р 5. а) Получение эмульгируемого концентрата (20 ЭК), мас. Соединение 2 20 2-Этоксиэтанол 10 Циклогексанон 35 Эмульсоген ЕL 360 (1) 7 Тенсиофикс СД 5 (2) 3 Ксилол 25 (1) этилоксилированное касторовое масло; (2) этилоксилированный коксовый спирт. Эмульсоген ЕL 360 и тенсиофикс СД 5 растворили в смеси 2-этоксиэтанола, циклогексанона и ксилола и затем ввели в смесь соединения 2 и перемешивали раствор в течение 2 ч. Композиции, содержащие соединение 1, соединения А, В, С, Д и Е можно получить таким же образом. в) получение эмульгируемого концентрата (35,ЭК), мас. Соединение 1 35 Циклогексанон 10 Тенсиофикс СД 21 (1) 2 Тенсиофикс В 7453 (2) 8 Ксилол 45 (1) смесь этоксилированного жирного спирта, этоксилированного нонилфенола и их фосфатов; (2) раствор кальция додецилбензолсульфоната, этоксилированного нонилфенола и этоксилированного-пропоксилированного нонилфенола в н-бутаноле. Повторили процесс, описанный в пункте а). Композиции, содержащие соединение 2, соединения А, В, С, Д и Е можно получить аналогичным способом. П р и м е р 6. Получение микрогранул, мас. Соединение 2 0,1 Циклогексанон 5,0 Бентонит 94,9 Раствор, содержащий соединение 2 в циклогексаноне, набрызгали на бентонит, предварительно измельченный до частиц размером 50 мкм и помещенный во вращающийся барабан. Перемешивание продолжали в течение 1 ч до тех пор, пока циклогексанон не испарился. Композицию, содержащую соединение 1, соединения А, В, С, Д и Е можно получить аналогично. П р и м е р 7. Получение диспергируемых в воде гранул (ДВГ), мас. Соединение 1 50 Саb-0-Sil M5 (1) 5 Атлокс 4862 (2) 3 Полифон 0 (3) 6 Геропон 1N (4) 5 Каолин 31 (1) аморфная двуокись кремния; (2) продукт конденсации нафталинсульфоната с формальдегидом; (3) связующий материал (лигнинсульфонат натрия); (4) изопропилнафталинсульфонат. Активный ингредиент смешали в измельченный раствор вместе с аморфной двуокисью кремния, атлоксом 4862 (диспергирующим агентом) и геропоном 1N (смачивающим материалом), а также с каолином. Смесь измельчили таким образом, что часть частиц размером больше 44 мкм диаметром стала меньше 0,5% Смесь смешали в месильной машине с водным раствором полифона О (связующего реагента) и затем с помощью экструдера получили гранулы диаметром 1 мм. Эти гранулы сушили в потоке воздуха. Композицию, содержащую соединение 2, соединения А, В, С, Д и Е можно получить аналогично. П р и м е р 8. Биологические испытания. Гербицидную активность и селективность соединений по изобретению сравнили с родственными по строению (R)-антиподом (соединение Д) и (RS)-1"-метоксикарбонилэтилом 2-бром-5-(2-хлор-4-трифторметилфенокси)бензоатом (соединение А), а также с (R)-антиподом (соединение Е) и (RS)-1"-этоксикарбонилэтилом 2-бром-5-(2-хлор-4-трифторметилфенокси)бензоатом (соединение В) и с имеющимся на рынке (RS)-1"-этоксикарбонилэтилом 5-(2-хлор-4-трифторметилфенокси)-2-нитро-бензоатом (соединение С) как ссылочными (стандартными) соединениями. В зависимости от вида растений равное количество (20-50) зерен каждого посадили в пластмассовые сосуды для культивирования на глубину 0,5 см, затем почву опрыскали при возникновении необходимости и сосуды содержали при оптимальной температуре и освещении. После достижения сорняками фазы 2-4 настоящих листьев или достижения культивируемыми растениями фазы 3-6 настоящих листьев, соответственно опрыскивание провели растворами с содержанием активного ингредиента 5, 15, 45, 135, 405 или 1215 г/га, соответственно. Оценку провели на 10-ый день после обработки путем определения процента поражения (L. Banki Bioassay, of Pesticides in Laboratory, Akademiai Kiado, Budapest, Hungary, 1978) и определения, таким образом, доз, необходимых для уничтожения 90% сорняков путем использования пробит-анализа (D.I.Finney: Probit-analysis, Cambridge University Press 2nd Ed. 1964). Одновременно определяли порог селективности культивируемых растений, т.е. наивысшую дозу, к которой растения устойчивы. Результаты представлены в табл. 1 и 2: а) ширина колосистая Amaranthus rehoflexus в) паслен черный Solanum nigrum c) портулак огородный Portulaca oleraceae d) непахучая матрикария Matricaria modora e) лекарственный паслен Datura shamonium f) марь белая Сhenopodium album g) Lamiem purpureum h) Vida arvensis i) рис Oryza sativa j) озимая пшеница Triticum vulgare k) озимый ячмень Hordeum vulgare e) соя Glycine soja П р и м е р 9. Полевые испытания. Это испытание провели, используя соединения 1 и 2, соответственно по изобретению и ссылочные соединения А, В, С, Д и Е, соответственно на озимой пшенице сорта Аврора на делянках в 20 м2 при четырехкратном повторении. Соединения, используемые в этих экспериментах, ввели в композиции, как описано в п.а) в примере 5. На этих делянках были следующие сорняки: Anthemis arvensis, Convolvulus arvensis, Matricaria modora, Veronica hederifolia и Stellaria media. Опрыскивание проводили 23 марта, когда Stellaria media зацветает, а другие сорняки достигли фазы развития в 10 см. Гербицидная активность указанных композиций определялась в конце 3-ей недели после опрыскивания (L. Banke: Bioassay of Pesticides in the Laboratory, Akademiai Kiado, Budapest, 1978). За исключением Stellaria media 100% сорняков были уничтожены при всех обработках. Важное отличие, касающееся гербицидной активности нa Stellaria media наблюдалось между соединениями по настоящему изобретению и ссылочными соединениями. Stellaria media уничтожалась преимущественно соединениями по настоящему изобретению, в то время как ссылочные соединения были неактивны. Уничтожение Stellaria media на полях, обработанных в дозе 50 г/га ссылочными соединениями, достигало 50% Значительное различие существует между фитотоксичностью по отношению к озимой пшенице у соединений по изобретению и ссылочных соединений. Данные, полученные на озимой пшенице и Stellaria media приведены в табл. 3.
ФОРМУЛА ИЗОБРЕТЕНИЯПроизводные (S)-энантиомера 2-бром-5-(2-хлор-4-трифторметилфенокси)бензоата общей формулы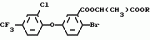 где R метил или этил, обладающие гербицидной активностью. где R метил или этил, обладающие гербицидной активностью.Популярные патенты: 2067832 Способ борьбы с грибковыми инфекциями растений ... тионила затем испаряют при пониженном давлении и остаток переносят в пиридин (15 мл). Полученный раствор охлаждают до 0oC и к нему медленно по каплям прибавляют раствор N-2-(1,1,2,2-тетрафторэтокси)этил-N-[2-(2,4,6-трихлорфенокси)этил] амина (2,5 г) в пиридине (5 мл). Смесь перемешивают 18 ч при комнатной температуре, затем переносят в воду и экстрагируют хлористым метиленом. Органическую фазу сушат над сульфатом натрия и испаряют при пониженном давлении. Полученный сырой продукт очищают хроматографированием на окиси кремния использованием в качестве элюента смеси CH2Cl2 MeOH (97:3 об./об.). Получено 0,85 г твердого вещества, спектральные характеристики соответствуют ... 2015633 Способ переработки отходов животноводческих комплексов и устройство для его осуществления ... известный способ обладает недостаточно высокой эффективностью. Изобретение направлено на разрешение следующей задачи. Предлагается высокоэффективный экологически чистый и безотходный способ переработки отходов животноводческих комплексов за счет извлечения воды путем кипения под воздействием разрежения (вакуума), организованного в виде непрерывного цикла. При этом за счет сбора и сжигания дурнопахнущих соединений в топке котельной установки обеспечивается улучшение условий труда обслуживающего персонала и сохранение экологической ситуации в месте эксплуатации предложенного решения. Благодаря утилизации и возможности повторного использования сконденсированных паров воды на ... 2239968 Способ предпосевной обработки семян овощных культур ... обработка 75% концентрацией рассола бишофита. Вес 10 растений при такой обработке составил 380 мг (табл.5). Изучение эффективности предпосевной обработки семян на урожайность перца, баклажана и свеклы показало, что в среднем за два года наиболее высокая урожайность перца сорта Подарок Молдовы, баклажана сорта Альбатрос и свеклы сорта Бордо формируется при предпосевной обработке семян 80% раствором рассола бишофита и соответственно составляет 4,61; 13,3 и 26,9 т/га (табл.6).Эффективность предпосевной обработки семян томата сорта Новичок, как показывают данные табл.7, во многом зависит от правильно выбранной концентрации бишофита. Так, наиболее высокий урожай томата при лучшем ... 2485083 Способ получения замещенных пиримидин-5-илкарбоновых кислот ... промывали диоксаном и перекристаллизовывали из диоксана.Выход 81%, т.пл. 240-242°С. Найдено (%):C, 48,81; H, 3,60; N, 18,87. C18H 16N6O2S3. Вычислено (%):C, 48,63; H, 3,63; N, 18,90. Спектр ЯМР1Н 1.44 (3H, т, CH2CH3, J=8.0); 4.46 (2H, кв, CH2CH3, J=12.5); 4.99 (2H, с, SCH 2); 7.02 (1H, т, 1CH-бенз, J=7.8); 7.19 (1H, т, 1CH-бенз, J=7.8); 7.58 (2H, м, 2CH-бенз.); 8.73 (1H, с, CH-пиримид.); 10.15 (1H, с, NH). Масс-спектр, m/z 444 [M]+. 0.06 моль этилового эфира 4-(5-метил[1,3,4]тиадиазол-2-илтиометил)-2-(бензтиазол-2-иламино)-пиримидин-5-илкарбоновой кислоты смачивали этиловым спиртом, добавляли 0.15 моль раствора гидроксида натрия (7%) и кипятили 1 час. После ... 2434381 Технологическая линия для приготовления и раздачи влажных кормов ... крана. Для уменьшения скорости истечения сухого комбикорма в нижней части дозатора уставлен спиральный трубопровод. Ниже спирального трубопровода выполнен усеченный конус, кольцевой трубопровод и рассекатель. Кольцевой трубопровод и рассекатель предназначены для равномерного рассекания жидкостью потока сухого концентрированного корма. Ниже дозатора установлен спиральный трубопровод. Усеченный конус установлен сверху кольцевого трубопровода и предназначен для направления потока сухого комбикорма в кольцевой трубопровод. Кольцевой трубопровод представляет собой два цилиндра разного диаметра и одинаковой высоты. Цилиндр меньшего диаметра - внутренний помещен в цилиндр большего ... |
Еще из этого раздела: 2399194 Способ и устройство контроля воздушного режима в корнеобитаемой среде 2482660 Способ выращивания рапса ярового на семена 2293463 Способ разработки лесосек 2399203 Способ оценки физиологического состояния организма цыплят 2218756 Способ изготовления антипаразитарного ошейника 2271096 Способ прогнозирования урожайности озимых зерновых культур в условиях засушливого климата 2454055 Устройство для ротационного внутрипочвенного рыхления с механическим приводом 2197817 Поплавок для рыболовных удочек и снастей 2162635 Устройство для аэрозольного распыления (варианты) 2465767 Оросительный мат для распределения воды на большой площади |
Изобретения в сельском хозяйстве
Обработка почвы в сельском и лесном хозяйствах
Посадка, посев, удобрение
Уборка урожая, жатва
Обработка и хранение продуктов полеводства и садоводства
Садоводство, разведение овощей, цветов, риса, фруктов, винограда, лесное хозяйство
Новые виды растений или способы их выращивания
Производство молочных продуктов
Животноводство, разведение и содержание птицы, рыбы, насекомых, рыбоводство, рыболовство
Поимка, отлов или отпугивание животных
Консервирование туш животных, или растений или их частей
Биоцидная, репеллентная, аттрактантная или регулирующая рост растений активность химических соединений или препаратов
Хлебопекарные печи, машины и прочее оборудование для хлебопечения
Машины или оборудование для приготовления или обработки теста
Обработка муки или теста для выпечки, способы выпечки, мучные изделия
|
|
||