Производное триазола, способы его получения и афицидное средство на его основеПатент на изобретение №: 2101282 Автор: Масами Озаки[JP], Рейдзиро Хонами[JP], Такаси Юмита[JP], Ацухико Икеда[JP], Наоказу Миногути[JP], Норихико Изава[JP], Тадайоси Хирано[JP] Патентообладатель: Кумиаи Кемикал Индастри Ко., Лтд. (JP), Ихара Кемикал Индастри, Ко., Лтд. (JP) Дата публикации: 10 Января, 1998 Адрес для переписки: подача заявки03.03.1993 публикация патента10.01.1998 Изображения  Сущность изобретения: 1. Производное триазола общей формулы I 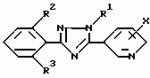 где R1 - низший алкил; R2 и R3- независимо галоид; X - хлор в 2- или 6-положении. 2. Афицидное средство на основе производного триазола общей формулы (I). 3. Способы получения производного триазола общей формулы (I) или: а/ путем взаимодействия соединения общей формулы II где R1 - низший алкил; R2 и R3- независимо галоид; X - хлор в 2- или 6-положении. 2. Афицидное средство на основе производного триазола общей формулы (I). 3. Способы получения производного триазола общей формулы (I) или: а/ путем взаимодействия соединения общей формулы II 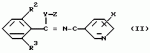 с гидразином R1-NHNH2; или б/ путем взаимодействия соединения общей формулы III: с гидразином R1-NHNH2; или б/ путем взаимодействия соединения общей формулы III: 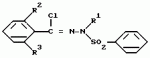 с производным бензонитрила формулы с производным бензонитрила формулы 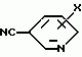 в присутствии кислоты Льюиса; или в/ путем взаимодействия соединения общей формулы IV: в присутствии кислоты Льюиса; или в/ путем взаимодействия соединения общей формулы IV: 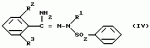 с соединением формулы с соединением формулы 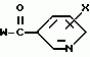 Использование - в сельском хозяйстве. 3 с. и 4 з.п.ф-лы, 5 табл.
, Использование - в сельском хозяйстве. 3 с. и 4 з.п.ф-лы, 5 табл.
, ОПИСАНИЕ ИЗОБРЕТЕНИЯ К ПАТЕНТУИзобретение имеет отношение к новому производному триазола, используемому как инсектицид, также как и к инсектициду, содержащему его в качестве активного ингредиента. Известно, что производные триазола, такие, как 3-хлорофенил-5-хлоропиридил-1-метил-1Н-1,2,4-триазол и ему подобные, эффективны для контроля численности клещей и кровососущих насекомых (описание исследования RD 278004). В этой литературе нет описания того, какая концентрация выше названного производного является эффективной по отношению к какому виду вредных насекомых, а также не ясно происхождение этого производного. Более того описанные в названной литературе конкретные соединения обладают недостаточными характеристиками с точки зрения системного перемещения и системного проникновения и едва ли могут быть удовлетворительными инсектицидами. Насекомые вредители продуктов сада и фермы относятся к тлям, таким, как хлопковая тля, тля зеленых персиков, тля наперстянки и т.п. Эти тли поедают растения в точках роста и сильно повреждают продукты садов и ферм, а также вносят вирусы. Поэтому необходимо контролировать размножение тлей. Нарастающая устойчивость вредных насекомых к существующим инсектицидам и акарицидам делает такой контроль еще более серьезным. В этой связи химикаты для контроля вредителей должны обладать негативными свойствами системного переноса и проникновения. Изобретатели синтезировали различные производные триазола, чтобы предложить инсектицид, применимый для контролирования выше названных вредных насекомых, и провели исследование их физиологической активности. В результате изобретатели нашли, что новые соединения с общей формулой (I), приведенной ниже, имеют прекрасные данные системного перемещения и по системному проникновению и обнаруживают превосходную инсектицидную активность по отношению к различным вредным насекомым и акаридам по сравнению с теми конкретными соединениями, которые описаны в вышеупомянутой литературе. Согласно изобретению, предлагается триазольное производное с общей формулой (1)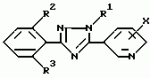 где R1 группа низшего алкила, а R2 и R3 - одинаковые или различные атомы галогенов; X атом хлора, находящийся в 2 - или 6-положении). Согласно изобретению данные производные триазола имеют особенно улучшенную активность по активному перемещению и проникновению благодаря тому, что как R2, так и R3 заместители бензольного кольца, связанного с 3-им положением триазольного цикла, являются атомами галогена. Более того триазольные производные, имеющие два заместителя в бензольном кольце, связанном с 3-им положением триазольного кольца, и алкильный заместитель в 1-м положении триазольного кольца, могут быть синтезированы новыми методами. В общей формуле (I) группа низшего алкила R1 включает метильную группу, этильную группу, пропильную группу, изопропильную группу, бутильную группу, изобутильную группу, трет-бутильную группу, втор-бутильную группу и т.п. а атом галогена R2 и R3 это фтор, хлор, бром и иод. Среди соединений общей формулы (I) соединение, в котором R1 метильная или этильная группа, а X атом хлора, находящийся во 2- или 6-м положении, является предпочтительным. Соединения общей формулы (I), соответствующие изобретению, приведены в табл.1. Нумерация соединения соответствует их дальнейшему описанию. Соединения, соответствующие изобретению, могут быть получены следующими методами, но не ограничиваются этими методами. Способ получения 1-1 Соединение общей формулы (I) может быть получено при взаимодействии алкил-N-ациламидатного производного или алкил-N-ацилтиоамидатного производного, представленных общей формулой (II), с производным гидразина общей формулы (III) в инертном растворителе согласно следующей системе реакции: где R1 группа низшего алкила, а R2 и R3 - одинаковые или различные атомы галогенов; X атом хлора, находящийся в 2 - или 6-положении). Согласно изобретению данные производные триазола имеют особенно улучшенную активность по активному перемещению и проникновению благодаря тому, что как R2, так и R3 заместители бензольного кольца, связанного с 3-им положением триазольного цикла, являются атомами галогена. Более того триазольные производные, имеющие два заместителя в бензольном кольце, связанном с 3-им положением триазольного кольца, и алкильный заместитель в 1-м положении триазольного кольца, могут быть синтезированы новыми методами. В общей формуле (I) группа низшего алкила R1 включает метильную группу, этильную группу, пропильную группу, изопропильную группу, бутильную группу, изобутильную группу, трет-бутильную группу, втор-бутильную группу и т.п. а атом галогена R2 и R3 это фтор, хлор, бром и иод. Среди соединений общей формулы (I) соединение, в котором R1 метильная или этильная группа, а X атом хлора, находящийся во 2- или 6-м положении, является предпочтительным. Соединения общей формулы (I), соответствующие изобретению, приведены в табл.1. Нумерация соединения соответствует их дальнейшему описанию. Соединения, соответствующие изобретению, могут быть получены следующими методами, но не ограничиваются этими методами. Способ получения 1-1 Соединение общей формулы (I) может быть получено при взаимодействии алкил-N-ациламидатного производного или алкил-N-ацилтиоамидатного производного, представленных общей формулой (II), с производным гидразина общей формулы (III) в инертном растворителе согласно следующей системе реакции: 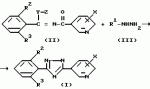 где Y атом серы или атом кислорода; Z группа низшего алкила; R1, R2, R3 и X то же, что указано выше. В качестве инертного растворителя может использоваться любой, не препятствующий реакции, такой как спирт: метанол, этанол и т.п. эфир, напр. диэтиловый эфир, тетрагидрофуран, диоксан диглим и т.п. алифатический углеводород, такой как пентан, гексан, петролейный эфир и т.п. галогенированный углеводород, такой как дихлорметан, дихлорэтан, хлороформ, четыреххлористый углерод и т.п. нитрил, такой как ацетонитрил и т.п. N,N-диметилформамид, N,N-диметилацетамид, диметилсульфоксид, вода и их смеси. Кроме того, производное гидразина (III) обычно используется в количестве 1-5 моль на 1 моль алкил-N-ациламидатного производного или алкил-N-ацилтиоимидатного производного или алкил-N-ацилтиоимидатного эфирного производного (II). Температуру реакции возможно поддерживать в пределах от 0oC до точки кипения используемого растворителя, но лучше в пределах от 0oC до 50oC. Время реакции зависит от взятых исходных веществ, но обычно в пределах 1-72 ч. Конкретный пример такой реакции приводится, например, в Synthesis 483 (1983). Алкил-N-ацил/тио/имидатное производное (II) как исходное соединение может быть получено следующим методом. Способ получения 1-2 Алкил-N-ацил/тио/имидатное производное, представленное общей формулой (II), может быть получено путем взаимодействия бензимидатного производного, представленного общей формулой (V) в инертном растворителе в присутствии основания согласно следующей схеме реакции: где Y атом серы или атом кислорода; Z группа низшего алкила; R1, R2, R3 и X то же, что указано выше. В качестве инертного растворителя может использоваться любой, не препятствующий реакции, такой как спирт: метанол, этанол и т.п. эфир, напр. диэтиловый эфир, тетрагидрофуран, диоксан диглим и т.п. алифатический углеводород, такой как пентан, гексан, петролейный эфир и т.п. галогенированный углеводород, такой как дихлорметан, дихлорэтан, хлороформ, четыреххлористый углерод и т.п. нитрил, такой как ацетонитрил и т.п. N,N-диметилформамид, N,N-диметилацетамид, диметилсульфоксид, вода и их смеси. Кроме того, производное гидразина (III) обычно используется в количестве 1-5 моль на 1 моль алкил-N-ациламидатного производного или алкил-N-ацилтиоимидатного производного или алкил-N-ацилтиоимидатного эфирного производного (II). Температуру реакции возможно поддерживать в пределах от 0oC до точки кипения используемого растворителя, но лучше в пределах от 0oC до 50oC. Время реакции зависит от взятых исходных веществ, но обычно в пределах 1-72 ч. Конкретный пример такой реакции приводится, например, в Synthesis 483 (1983). Алкил-N-ацил/тио/имидатное производное (II) как исходное соединение может быть получено следующим методом. Способ получения 1-2 Алкил-N-ацил/тио/имидатное производное, представленное общей формулой (II), может быть получено путем взаимодействия бензимидатного производного, представленного общей формулой (V) в инертном растворителе в присутствии основания согласно следующей схеме реакции: 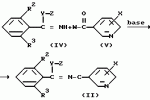 в которой W атом галогена, а R2, R3, X, Y и Z те же, что указаны выше). Кроме того, бензимидатное производное общей формулы (IV) может использоваться в виде кислотно-аддитивной соли. В этом случае тетрафторид был хлористый водород, бромистый водород, йодистый водород и т.п. могут быть использованы. В качестве основания могут быть использованы неорганические основания, такие как карбонат натрия, карбонат калия, бикарбонат иодид гидроксид натрия, гидроксид калия и т.п. они органические основания, такие как диэтиламин, триэтиламин, пиридин, 4-N,N-диметиламинопиридин и т.п. В качестве растворителя следует упомянуть кетон, такой как ацетон, метилэтилкетон и т.п. как эфир диэтиловый эфир, тетрагидрофуран, диоксан, диглим и т.п. ароматический углеводород, такой как бензол, толуол, хлорбензол и т.п. алифатический углеводород, такой как пентан, гексан, петролейный эфир и т.п. галогенированный углеводород, такой как дихлорметан, дихлорэтан, хлороформ, четыреххлористый углерод или т.п. нитрил, такой как ацетонитрил или подобные ему; диметилформамид, диметилацетамид, диметилсульфоксид и их смеси. В общем галогенангидрид никотиновой кислоты (V) используют в количестве 0,8-1,3 моль на 1 моль бензимидатного производного (IV). Количество применяемого основания равно 1,0- 2,0 моль-эквивалента на 1 моль бензимидатного производного (IV). Время реакции зависит от используемых исходных соединений, но обычно в пределах 1-24 часа, температура реакции в пределах от 0oC до точки кипения используемого растворителя. Способ получения 2 Соединение общей формулы (I) в соответствии с изобретением может быть получено с помощью реакции N-/фенилсульфонил/бензгидразоноилхлоридного производного, представленного общей формулой (VI) с 3-цианопиридиновым производным, представленным общей формулой (VII) в инертном растворителе в присутствии кислоты Льюиса в соответствии со следующей схемой реакции: в которой W атом галогена, а R2, R3, X, Y и Z те же, что указаны выше). Кроме того, бензимидатное производное общей формулы (IV) может использоваться в виде кислотно-аддитивной соли. В этом случае тетрафторид был хлористый водород, бромистый водород, йодистый водород и т.п. могут быть использованы. В качестве основания могут быть использованы неорганические основания, такие как карбонат натрия, карбонат калия, бикарбонат иодид гидроксид натрия, гидроксид калия и т.п. они органические основания, такие как диэтиламин, триэтиламин, пиридин, 4-N,N-диметиламинопиридин и т.п. В качестве растворителя следует упомянуть кетон, такой как ацетон, метилэтилкетон и т.п. как эфир диэтиловый эфир, тетрагидрофуран, диоксан, диглим и т.п. ароматический углеводород, такой как бензол, толуол, хлорбензол и т.п. алифатический углеводород, такой как пентан, гексан, петролейный эфир и т.п. галогенированный углеводород, такой как дихлорметан, дихлорэтан, хлороформ, четыреххлористый углерод или т.п. нитрил, такой как ацетонитрил или подобные ему; диметилформамид, диметилацетамид, диметилсульфоксид и их смеси. В общем галогенангидрид никотиновой кислоты (V) используют в количестве 0,8-1,3 моль на 1 моль бензимидатного производного (IV). Количество применяемого основания равно 1,0- 2,0 моль-эквивалента на 1 моль бензимидатного производного (IV). Время реакции зависит от используемых исходных соединений, но обычно в пределах 1-24 часа, температура реакции в пределах от 0oC до точки кипения используемого растворителя. Способ получения 2 Соединение общей формулы (I) в соответствии с изобретением может быть получено с помощью реакции N-/фенилсульфонил/бензгидразоноилхлоридного производного, представленного общей формулой (VI) с 3-цианопиридиновым производным, представленным общей формулой (VII) в инертном растворителе в присутствии кислоты Льюиса в соответствии со следующей схемой реакции: 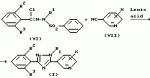 где R1, R2, R3 и X те же, что упомянуты выше. В качестве инертного растворителя можно взять любой, не мешающий реакции, например эфир, такой как диэтиловый эфир, тетрагидрофуран, диоксан, диглим и т.п. ароматический углеводород, такой как бензол, толуол, хлорбензол, дихлорбензол и т.п. алифатический углеводород, такой как пентан, гексан, петролейный эфир и т.п. галогенированный углеводород, такой как дихлорметан, дихлорэтан, хлороформ, четыреххлористый углерод, и т.п. диметилформамид, диметилацетамид, диметилсульфоксид или их смесь. В общем, 3-цианопиридиновое производное (VII) и кислота Льюиса используются в количестве 1,0 2,0 моль на 1 моль N-/фенилсульфонил/бензгидразоноилхлоридного производного (VI) соответственно. Температуру реакции возможно поддерживать в диапазоне от 0oC до точки кипения используемого растворителя, лучше в пределах 50 -150oC. Время реакции зависит от взятых исходных веществ, но обычно в пределах от 30 мин до 5 ч. Конкретный пример этой реакции приводится, например, в Bulletin of Chemical society of Japan, vol.56 pages 545-548 (1983). 545-545 (1983). Способ получения 3 Соединение общей формулы (I) в соответствии с изобретением может быть получено путем реакции N-/фенилсульфонил/бензамидразонового производного, представленного общей формулой (VIII) с галогенангидридом никотиновой кислоты производным общей формулы (V) в инертном растворителе согласно следующей реакции: где R1, R2, R3 и X те же, что упомянуты выше. В качестве инертного растворителя можно взять любой, не мешающий реакции, например эфир, такой как диэтиловый эфир, тетрагидрофуран, диоксан, диглим и т.п. ароматический углеводород, такой как бензол, толуол, хлорбензол, дихлорбензол и т.п. алифатический углеводород, такой как пентан, гексан, петролейный эфир и т.п. галогенированный углеводород, такой как дихлорметан, дихлорэтан, хлороформ, четыреххлористый углерод, и т.п. диметилформамид, диметилацетамид, диметилсульфоксид или их смесь. В общем, 3-цианопиридиновое производное (VII) и кислота Льюиса используются в количестве 1,0 2,0 моль на 1 моль N-/фенилсульфонил/бензгидразоноилхлоридного производного (VI) соответственно. Температуру реакции возможно поддерживать в диапазоне от 0oC до точки кипения используемого растворителя, лучше в пределах 50 -150oC. Время реакции зависит от взятых исходных веществ, но обычно в пределах от 30 мин до 5 ч. Конкретный пример этой реакции приводится, например, в Bulletin of Chemical society of Japan, vol.56 pages 545-548 (1983). 545-545 (1983). Способ получения 3 Соединение общей формулы (I) в соответствии с изобретением может быть получено путем реакции N-/фенилсульфонил/бензамидразонового производного, представленного общей формулой (VIII) с галогенангидридом никотиновой кислоты производным общей формулы (V) в инертном растворителе согласно следующей реакции: 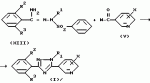 где R1, R2, R3 и X то же самое, что упомянуто выше. В качестве инертного растворителя можно использовать любой из растворителей, не мешающих реакции, которые включают эфир, такой как диэтиловый эфир, тетрагидрофуран, диоксан, диглим и т.п. ароматический углеводород, такой как бензол, толуол, хлорбензол, и т.п. алифатический углеводород, такой как пентан, гексан, петролейный эфир, и т.п. галогенированный углеводород, такой как дихлорметан, дихлорэтан, хлороформ, четыреххлористый углерод и т.п. диметилформамид, диметилацетамид, диметилсульфоксид или их смесь. В общем, никотиноилгалоидное производное (V) (галогенангидридное производное) используют в количестве 1,0 2,0 моль на 1 моль N-/фенилсульфенил) бензамидгидразонового производного (VIII). Температуру реакции возможно поддерживать в пределах от 0oC до точки кипения используемого растворителя, но лучше в пределах от 50oC до 200oC. Время реакции зависит от взятых исходных веществ, но обычно в пределах от 30 мин до 5 ч. Конкретный пример этой реакции раскрывается, например, в Bulletin of the chemical society of Japan, vol. 56, page 545-548, 1983. Кроме того, N-/фенилсульфонил/бензамидразоновое производное (VIII) как исходное соединение может быть получено следующим методом. Способ получения 3-2 N-/фенилсульфонил/бензамидразоновое производное, представленное общей формулой (VIII) может быть получено с помощью реакции N-/фенилсульфонил/бензгидразоноилхлоридного производного общей формулы (VI) с газообразным аммиаком в инертном растворителе в соответствии со следующей реакцией: где R1, R2, R3 и X то же самое, что упомянуто выше. В качестве инертного растворителя можно использовать любой из растворителей, не мешающих реакции, которые включают эфир, такой как диэтиловый эфир, тетрагидрофуран, диоксан, диглим и т.п. ароматический углеводород, такой как бензол, толуол, хлорбензол, и т.п. алифатический углеводород, такой как пентан, гексан, петролейный эфир, и т.п. галогенированный углеводород, такой как дихлорметан, дихлорэтан, хлороформ, четыреххлористый углерод и т.п. диметилформамид, диметилацетамид, диметилсульфоксид или их смесь. В общем, никотиноилгалоидное производное (V) (галогенангидридное производное) используют в количестве 1,0 2,0 моль на 1 моль N-/фенилсульфенил) бензамидгидразонового производного (VIII). Температуру реакции возможно поддерживать в пределах от 0oC до точки кипения используемого растворителя, но лучше в пределах от 50oC до 200oC. Время реакции зависит от взятых исходных веществ, но обычно в пределах от 30 мин до 5 ч. Конкретный пример этой реакции раскрывается, например, в Bulletin of the chemical society of Japan, vol. 56, page 545-548, 1983. Кроме того, N-/фенилсульфонил/бензамидразоновое производное (VIII) как исходное соединение может быть получено следующим методом. Способ получения 3-2 N-/фенилсульфонил/бензамидразоновое производное, представленное общей формулой (VIII) может быть получено с помощью реакции N-/фенилсульфонил/бензгидразоноилхлоридного производного общей формулы (VI) с газообразным аммиаком в инертном растворителе в соответствии со следующей реакцией: 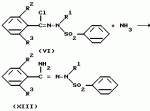 где R1, R2, R3- те же, как указано выше. В качестве инертного растворителя можно использовать любой, не мешающий реакции, напр. эфир, такой как диэтиловый эфир, тетрагидрофуран, диоксан, диглим и т. п. ароматический углеводород, такой как бензол, толуол, хлорбензол и т. п. и алифатический углеводород, такой как пентан, гексан, петролейный эфир и т.п. галогенированный углеводород, такой как дихлорметан, дихлорэтан, хлороформ, четыреххлористый углерод и т.п. диметилформамид, диметилацетамид, диметилсульфоксид или их смесь. В общем, аммиак и используют в количестве 5,0 10,0 моль на 1 моль N-/фенилсульфонил/бензгидразоноилхлоридного производного (VI). Температура реакции возможна в пределах от 0oC до точки кипения используемого растворителя, но предпочтительно в пределах 50 150oC. Время реакции зависит от используемых исходных веществ, но обычно в пределах 5 20 ч. Конкретный пример этой реакции раскрывается, например, в Bulletin of the chemical society of Japan, vol. 56, page 547,1983. Следующие примеры даются в качестве иллюстрации, но не для ограничения изобретения. Пример получения 1. 5-/2-хлорпиридин-3-ил/-3-/2,6-дифторфенил/-1-метил-1Н-1,2,4-триазол (соединение 1) В 100 мл толуола растворяли в 1,9 г этил-2,6-дифторбензимидата и 1,2 г триэтиламина, к которым добавляли по каплям 1,8 г 2-хлороникотиноилхлорида в диапазоне температур 5-10oC при перемешивании. Полученный раствор перемешивали при комнатной температуре в течение 6 ч. После завершения реакции раствор промывали водным раствором соли, затем водой и образующийся толуольный слой высушивали сульфатом натрия. К толуольному слою добавляли 0,5 г монометилгидразина, который реагировал при комнатной температуре в течение 8 ч. После завершения реакции раствор промывали разбавленным раствором соляной кислоты, затем водой, а затем толуольный слой высушивали над безводным сульфатом магния и концентрировали при пониженном давлении. Полученный концентрат хроматографировали на силикагеле /торговая марка: Wakogel C-200), используя для проявления смешанный раствор гексана и этилацетата, чтобы получить 0,8 г /выход 25,8%) целевых желтых гранулированных кристаллов/точка плавления: 167-171,0oC). Данные ЯМР (60 МГц CDCl3 растворитель, величина) 3,95 (s, 3Н) 6,80 7,68 (m, 4Н) 7,05 (dd, 1Н) 8,55 (dd, 1Н) Пример 2. 3-(2,6-дихлорфенил)-5-(2-хлорпиридил-3-ил)-1-метил-1Н-1,2,4-триазол (соединение 3) 5,7 г N-метил-N- фецилсульфонил-2,6-дихлорбензогидразоноил хлорида и 2,3 г 2-хлор-З-цианопиридина растворили в 50 мл дихлорбензол и к полученному раствору добавили при перемешивании 2,2 г безводного хлорида алюминия при комнатной температуре. Полученный раствор нагревали до 120-140oC на масляной бане при перемешивании в течение 4 ч. После завершения реакции реакционный раствор промывали разбавленным раствором щелочи, а затем разбавленным раствором соляной кислоты. После промывки водой органический слой сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Результирующий концентрат хроматографировали на силикагеле (торговая марка: Wakogel C-200), используя для заявления смешанный раствор гексана и этилацетата с получением 1,9 г (выход 37,3%) целевых светлокоричневых кристаллов в виде гранул (т.п. 133,0-135,5oC) ЯМР: 160 МГц, CDCl3, б): 3,93 (с, 3Н), 7,30-7,63 (м, 4Н), 7,95 (dd, 1Н), 8,55 (dd, 1Н) Пример 3. 3-/2-хлор-6-фторфенил)-5- (6-хлорпиридин-3-ил)-1-метил-1Н-1,2,4-триазол (соединение 7) N-метил-N-фенилсульфонил-2-хлоро-6-фторбензамидразон и 4,5 г 6-хлорпикопитиноилхлорида растворили в 50 мл 1-метил-2-пирролидина (NMP). Полученный раствор нагревали до 110-120oC на масляной бане и перемешивали 4 ч. После завершения реакции добавили 200 мл хлороформа и промывали водой. Полученный органический слой сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Результирующий концентрат хроматографировали на силикагеле (торговая марка Wakogel C-200), используя для проявления смешанный раствор гексана и этилацетата с получением 2,0 г (выход 35,5%) желтых кристаллических гранул (т.пл. 118,5-120,5oC). ЯМР (60 МГц, CDCl3, где R1, R2, R3- те же, как указано выше. В качестве инертного растворителя можно использовать любой, не мешающий реакции, напр. эфир, такой как диэтиловый эфир, тетрагидрофуран, диоксан, диглим и т. п. ароматический углеводород, такой как бензол, толуол, хлорбензол и т. п. и алифатический углеводород, такой как пентан, гексан, петролейный эфир и т.п. галогенированный углеводород, такой как дихлорметан, дихлорэтан, хлороформ, четыреххлористый углерод и т.п. диметилформамид, диметилацетамид, диметилсульфоксид или их смесь. В общем, аммиак и используют в количестве 5,0 10,0 моль на 1 моль N-/фенилсульфонил/бензгидразоноилхлоридного производного (VI). Температура реакции возможна в пределах от 0oC до точки кипения используемого растворителя, но предпочтительно в пределах 50 150oC. Время реакции зависит от используемых исходных веществ, но обычно в пределах 5 20 ч. Конкретный пример этой реакции раскрывается, например, в Bulletin of the chemical society of Japan, vol. 56, page 547,1983. Следующие примеры даются в качестве иллюстрации, но не для ограничения изобретения. Пример получения 1. 5-/2-хлорпиридин-3-ил/-3-/2,6-дифторфенил/-1-метил-1Н-1,2,4-триазол (соединение 1) В 100 мл толуола растворяли в 1,9 г этил-2,6-дифторбензимидата и 1,2 г триэтиламина, к которым добавляли по каплям 1,8 г 2-хлороникотиноилхлорида в диапазоне температур 5-10oC при перемешивании. Полученный раствор перемешивали при комнатной температуре в течение 6 ч. После завершения реакции раствор промывали водным раствором соли, затем водой и образующийся толуольный слой высушивали сульфатом натрия. К толуольному слою добавляли 0,5 г монометилгидразина, который реагировал при комнатной температуре в течение 8 ч. После завершения реакции раствор промывали разбавленным раствором соляной кислоты, затем водой, а затем толуольный слой высушивали над безводным сульфатом магния и концентрировали при пониженном давлении. Полученный концентрат хроматографировали на силикагеле /торговая марка: Wakogel C-200), используя для проявления смешанный раствор гексана и этилацетата, чтобы получить 0,8 г /выход 25,8%) целевых желтых гранулированных кристаллов/точка плавления: 167-171,0oC). Данные ЯМР (60 МГц CDCl3 растворитель, величина) 3,95 (s, 3Н) 6,80 7,68 (m, 4Н) 7,05 (dd, 1Н) 8,55 (dd, 1Н) Пример 2. 3-(2,6-дихлорфенил)-5-(2-хлорпиридил-3-ил)-1-метил-1Н-1,2,4-триазол (соединение 3) 5,7 г N-метил-N- фецилсульфонил-2,6-дихлорбензогидразоноил хлорида и 2,3 г 2-хлор-З-цианопиридина растворили в 50 мл дихлорбензол и к полученному раствору добавили при перемешивании 2,2 г безводного хлорида алюминия при комнатной температуре. Полученный раствор нагревали до 120-140oC на масляной бане при перемешивании в течение 4 ч. После завершения реакции реакционный раствор промывали разбавленным раствором щелочи, а затем разбавленным раствором соляной кислоты. После промывки водой органический слой сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Результирующий концентрат хроматографировали на силикагеле (торговая марка: Wakogel C-200), используя для заявления смешанный раствор гексана и этилацетата с получением 1,9 г (выход 37,3%) целевых светлокоричневых кристаллов в виде гранул (т.п. 133,0-135,5oC) ЯМР: 160 МГц, CDCl3, б): 3,93 (с, 3Н), 7,30-7,63 (м, 4Н), 7,95 (dd, 1Н), 8,55 (dd, 1Н) Пример 3. 3-/2-хлор-6-фторфенил)-5- (6-хлорпиридин-3-ил)-1-метил-1Н-1,2,4-триазол (соединение 7) N-метил-N-фенилсульфонил-2-хлоро-6-фторбензамидразон и 4,5 г 6-хлорпикопитиноилхлорида растворили в 50 мл 1-метил-2-пирролидина (NMP). Полученный раствор нагревали до 110-120oC на масляной бане и перемешивали 4 ч. После завершения реакции добавили 200 мл хлороформа и промывали водой. Полученный органический слой сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Результирующий концентрат хроматографировали на силикагеле (торговая марка Wakogel C-200), используя для проявления смешанный раствор гексана и этилацетата с получением 2,0 г (выход 35,5%) желтых кристаллических гранул (т.пл. 118,5-120,5oC). ЯМР (60 МГц, CDCl3, 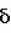 ): 4,03 (С, 3Н), 6,83-7,80 (т, 4Н), 8,05 (дд. 1Н), 8,75 (дд. 1Н). Пример 4. 3-/2-хлоро-6-фторфенил/-5-6-хлоропиридин-3-ил)-1-изопропил- 1Н-1,2,4-триазол (соединение 11) В 20 мл дихлорбензола растворяли 5,8 г N-метил-N-фенилсульфонил-2-хлоро-6-фторбензогидразоноилхлорида и 2,3 г 6-хлоро-З-цианопиридина, к которым добавляли 2,2 г безводного алюминия хлорида при комнатной температуре при перемешивании. Образующийся раствор нагревали до 140o на масляной бане и перемешивали в течение 30 мин. После завершения реакции реакционный раствор растворяли в 200 мл хлороформа. Раствор в хлороформе промывали разбавленным щелочным раствором, а затем разбавленным раствором соляной кислоты, после промывания водой органический слой высушивали над безводным сульфатом магния и концентрировали при пониженном давлении. Полученный концентрат хроматографировали на силикагеле (торговая марка: Wakogel C-200), используя смешанный раствор гексана и этилацетата в качестве элюирующего растворителя, и получили продукт в виде коричневой вязкой жидкости (показатель преломления ( n2D0 )- измерение невозможно). Данные ЯМР (60 МГц, CDCl3 растворитель, величина ): 4,03 (С, 3Н), 6,83-7,80 (т, 4Н), 8,05 (дд. 1Н), 8,75 (дд. 1Н). Пример 4. 3-/2-хлоро-6-фторфенил/-5-6-хлоропиридин-3-ил)-1-изопропил- 1Н-1,2,4-триазол (соединение 11) В 20 мл дихлорбензола растворяли 5,8 г N-метил-N-фенилсульфонил-2-хлоро-6-фторбензогидразоноилхлорида и 2,3 г 6-хлоро-З-цианопиридина, к которым добавляли 2,2 г безводного алюминия хлорида при комнатной температуре при перемешивании. Образующийся раствор нагревали до 140o на масляной бане и перемешивали в течение 30 мин. После завершения реакции реакционный раствор растворяли в 200 мл хлороформа. Раствор в хлороформе промывали разбавленным щелочным раствором, а затем разбавленным раствором соляной кислоты, после промывания водой органический слой высушивали над безводным сульфатом магния и концентрировали при пониженном давлении. Полученный концентрат хроматографировали на силикагеле (торговая марка: Wakogel C-200), используя смешанный раствор гексана и этилацетата в качестве элюирующего растворителя, и получили продукт в виде коричневой вязкой жидкости (показатель преломления ( n2D0 )- измерение невозможно). Данные ЯМР (60 МГц, CDCl3 растворитель, величина 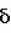 ) 1,60 (д, 6Н) 4,45-4,95 (м, 1Н) 6,95 7,55 (m, 4Н) 7,95 (дд, 1Н) 8,65 (д, 13) Инсектицид в соответствии с изобретением содержит производное триазола, представленное общей формулой (I) в качестве активного ингредиента. Когда триазольные соединения, соответствующие изобретению, используются как активный ингредиент инсектицидов, эти соединения могут применяться сами по себе отдельно или совместно с носителем, поверхностно-активным веществом, диспергирующим агентом или любой добавкой, чтобы получить порошки, смачиваемый порошок, эмульсию, тонкоразмельченный порошок, гранулы и т.п. В качестве носителя для получения сельскохозяйственных химикатов могут быть упомянуты такие твердые носители как зиклит, тальк, бентонит, глина, каолин, диамотовая земля, белый уголь, вермикулит, гидроксид кальция, кварцевый песок, сульфат аммония, мочевина и т.п. а жидкие носители изопропиловый спирт, ксилол, циклогексанон, метилнафталин, и т.п. Как поверхностно-активные и диспергирующие агенты могут быть упомянуты металлические соли алкилбензолсульфокислоты, динафтил метандисульфоновой кислоты, эфира спирта и серной кислоты, алкиларилсульфонат, лигносульфонат, полиоксиэтиленгликолевый эфир, полиоксиэтиленалкилариловый эфир, полиоксиэтиленсорбитанмоноалкилат и т.п. В качестве добавки следует упомянуть карбоксиметилцеллюлозу, полиэтиленгликоль, гуммиарабик и т.п. При составлении композиций количество используемого активного ингредиента может быть выбрано соответственно составленной цели, но подходящим является вызов в пределах 0,05 20% по весу, преимущественно 0,1 10% по весу в случае порошков и гранул. В случае эмульсий и смачиваемых порошков количество активного ингредиента лучше выбирать в пределах 0,5-8,0% по весу, лучше 1-6% по весу. Инсектицид, соответствующий изобретению, может применяться путем распыления на стебли и листья, внесения в почву, внесения в ящики для рассады, распыления над поверхностью воды и т.п. При употреблении инсектицид непосредственно наносится или распыляется после разведения до подходящей концентрации. Количество наносимого инсектицида зависит от вида соединения, используемого в качестве активного ингредиента, от вредного насекомого, против которого оно применяется, от направленности и степени вреда, наносимого насекомым, от условий окружающей среды, от вида используемой формы инсектицида и т. п. Когда инсектицид, соответствующий изобретению, непосредственно используется как порошок или гранулы, количество активного ингредиента обычно выбирается в пределах 0,05 г 5 кг, предпочтительно 0,1 1 кг на 10 ар. Более того, когда он используется в виде жидкой эмульсии или смачиваемого порошка, количество активного ингредиента стоит выбрать в пределах 0,1 5000 ч. на 1 млн. лучше 1-1000 ч. на 1 млн. Кроме того, инсектицид, соответствующий изобретению, можно использовать в смеси с другими инсектицидом, фунгицидом, удобрениями, регулятором роста растений и т.п. Составление композиций будет далее описано на конкретных примерах. В этом случае вид соединений и добавок и их соотношения не ограничиваются этими примерами и могут изменяться в широких пределах. Кроме того, указаны весовые проценты, если специально не оговорено. Пример получения состава 1. Эмульсия Эмульсия была приготовлена равномерным растворением 30% соединения 6, 20% циклогексанона, 11% полиоксиэтиленалкиларилового эфира, 4% алкилбензолсульфоната кальция и 35% метилнафталина. Пример получения состава 2. Смачиваемый порошок Смачиваемый порошок готовили равномерным смешиванием и измельчением в порошок 40% соединения 3, 15% диатомовой земли, 15% глины, 5% белого угля, 2% натрийдинафтилметандисульфоната и 3% натрийлигнинсульфоната. Пример получения состава 3. Порошок Порошок готовили равномерным смешиванием и измельчением 2% соединения 1,5% диатомовой земли и 93% глины. Пример получения состава 4. Гранулы 5% соединения 7, 2% натриевой соли эфира лаурилового спирта и серной кислоты, 5% натрий-лигнин-сульфоната, 2% карбоксиметилцеллюлоза и 86% глины, которые были равномерно смешаны и измельчены. Затем 100 ч. по весу полученной смеси добавили к 20 ч. воды (по весу) и месили и придавали форму гранул размером 14-24 меш, пропуская через гранулирующую машину путем выдавливания и высушивали, чтобы получить гранулы. Триазольные производные, соответствующие изобретению, эффективны для контроля численности тлей, таких как хлопковая тля, тля зеленых персиков, капустная тля и т.п. цикадки, такие как коричневые цикадки и т.п. листовые цикады, такие как зеленая рисовая цикада, чайная зеленая цикада и т.п. белокрылки, такие как белокрылка тепличная и т.п. парнокрылые вредные насекомые, такие как тутовый шелкопряд, рисовый клоп и т.п. чешуекрылые вредные насекомые, такие как капустная моль, бобовая бабочка-совка, табачная бабочка-совка и т.п. двукрылые вредные насекомые, такие как домашняя муха, москиты и т.п. жесткокрылые вредные насекомые, такие как рисовый долгоносик, соевый долгоносик, тыквенный листоед и т.п. тараканы, такие как Американский таракан, паровая муха, и т.п. клещи, такие как двухпятнистый клещик паутинный, паутинный клещ канзава, красный лимонный клещ и т.п. В особенности инсектицид, соответствующий изобретению, оказывает очень выраженное действие на контролирование численности тлей, таких как хлопковая тля, тля зеленых персиков, кукурузная тля и т.п. дельфацидов, таких как вьюнковая тля, капустная тля и т.п. белокрылок, таких как тепличная белокрылка, белокрылка сладкого картофеля и т.п. парнокрылых вредных насекомых, таких как тутовый шелкопряд и т.п. трипсов, таких как южный желтый трипс и т.п. клещей, таких как двухпятнистый клещик паутинный, паутинный клещ канзава, цитрусовый красный клещ и т.п. Действие соединений, соответствующих изобретению, будет описано в соответствии со следующими примерами испытаний. Более того следующие соединения использовали как сравнительные агенты. Сравнительные агенты от A до C это соединения, опубликованные в Research Disclosure RD 278004, и используются в такой же форме, которая описана выше, тогда как сравнительные химикаты D и E это коммерческие продукты, обычно применяемые для борьбы с тлями. Сравнительный агент A: 3-/2/хлорофенил/-5-/2-хлоропиридин-3-ил/-1-метил-1Н-1,2,4-триазол, Сравнительный агент B: 3-/2/хлорофенил/-5-/6-хлоропиридин-3-ил/-1-метил-1Н-1,2,4-триазол, Сравнительный агент C: 3-/2-хлоро-4-фторфенил/-5-/6-хлоропиридиы-3-ил/-1-метил-1Н-1,2,4-триазол; Сравнительный агент D: 45% смачиваемый порошок метомил Сравнительный агент E: 50% эмульсия этиофенкарб Пример испытаний 1. Проверка инсектицида методом погружения Смачиваемый порошок, приготовленный в соответствии с примером получения состава 2, разводили водой так, чтобы концентрация активного ингредиента была 0,8 ч. на 1 млн. или 0,16 ч. на 1 млн. В полученный разбавленный увлажняемый порошок погружали проростки огурца, предварительно зараженные личинками хлопковой тли, и затем высушивали на воздухе. После высушивания проростки огурцов помещали в термостатированную камеру при 25oC на 3 дня и после этого подсчитывали число погибших личинок, чтобы определить процент их гибели. Тест проводили в двух сериях. Результаты приведены в табл.2. Пример испытаний 2. Проверка инсектицида методом введения Смачиваемый порошок, полученный в соответствии с примером приготовления 2, разводили водой так, чтобы концентрация активного ингредиента была 0,8 ч. на 1 млн. или 0,16 ч. на 1 млн. Полученный разбавленный смачиваемый порошок вносили в горшок, содержащий проростки огурца, предварительно зараженные личинками хлопковой тли. После введения инсектицида проростки огурца помещали в термостат при 25oC на 3 дня и затем подсчитывали число погибших личинок, чтобы определить процент гибели. Тест проводили в двух сериях. Результаты приведены в табл.3. Пример испытания 3. Тест на проверку системного перемещения в почве, улучшающий процесс обработки Гранулы, приготовленные в соответствии с примером приготовления 4/0,5 кг на 10 ар, наносили на стержневые корни проростков огурца, растущих в горшке и предварительно зараженных личинками тли. После такой обработки горшок помещали в теплицу, где число живых взрослых особей и личинок подсчитывали каждые 7 дней. Тест выполняли тремя параллельными сериями. Результаты показаны в табл.4. Пример теста 4. Тест для контроля системного перемещения путем распыления на стебли и листья Смачиваемый порошок, приготовленный в соответствии с примером приготовления 2, разводили водой так, чтобы концентрация активного ингредиента была 100 ч. на 1 млн. Полученный разбавленный смачиваемый порошок распыляли только на верхнюю часть листьев сеянцев огурца, посаженных в горшок и предварительно зараженных с нижней стороны личинками тли, причем нижняя сторона не опрыскивалась. После обработки горшок помещали в теплицу и каждые 5 дней подсчитывали количество взрослых особей и живых личинок на нижней стороне. Тест проводили с тремя параллельными сериями. Результаты приведены в табл.5. ) 1,60 (д, 6Н) 4,45-4,95 (м, 1Н) 6,95 7,55 (m, 4Н) 7,95 (дд, 1Н) 8,65 (д, 13) Инсектицид в соответствии с изобретением содержит производное триазола, представленное общей формулой (I) в качестве активного ингредиента. Когда триазольные соединения, соответствующие изобретению, используются как активный ингредиент инсектицидов, эти соединения могут применяться сами по себе отдельно или совместно с носителем, поверхностно-активным веществом, диспергирующим агентом или любой добавкой, чтобы получить порошки, смачиваемый порошок, эмульсию, тонкоразмельченный порошок, гранулы и т.п. В качестве носителя для получения сельскохозяйственных химикатов могут быть упомянуты такие твердые носители как зиклит, тальк, бентонит, глина, каолин, диамотовая земля, белый уголь, вермикулит, гидроксид кальция, кварцевый песок, сульфат аммония, мочевина и т.п. а жидкие носители изопропиловый спирт, ксилол, циклогексанон, метилнафталин, и т.п. Как поверхностно-активные и диспергирующие агенты могут быть упомянуты металлические соли алкилбензолсульфокислоты, динафтил метандисульфоновой кислоты, эфира спирта и серной кислоты, алкиларилсульфонат, лигносульфонат, полиоксиэтиленгликолевый эфир, полиоксиэтиленалкилариловый эфир, полиоксиэтиленсорбитанмоноалкилат и т.п. В качестве добавки следует упомянуть карбоксиметилцеллюлозу, полиэтиленгликоль, гуммиарабик и т.п. При составлении композиций количество используемого активного ингредиента может быть выбрано соответственно составленной цели, но подходящим является вызов в пределах 0,05 20% по весу, преимущественно 0,1 10% по весу в случае порошков и гранул. В случае эмульсий и смачиваемых порошков количество активного ингредиента лучше выбирать в пределах 0,5-8,0% по весу, лучше 1-6% по весу. Инсектицид, соответствующий изобретению, может применяться путем распыления на стебли и листья, внесения в почву, внесения в ящики для рассады, распыления над поверхностью воды и т.п. При употреблении инсектицид непосредственно наносится или распыляется после разведения до подходящей концентрации. Количество наносимого инсектицида зависит от вида соединения, используемого в качестве активного ингредиента, от вредного насекомого, против которого оно применяется, от направленности и степени вреда, наносимого насекомым, от условий окружающей среды, от вида используемой формы инсектицида и т. п. Когда инсектицид, соответствующий изобретению, непосредственно используется как порошок или гранулы, количество активного ингредиента обычно выбирается в пределах 0,05 г 5 кг, предпочтительно 0,1 1 кг на 10 ар. Более того, когда он используется в виде жидкой эмульсии или смачиваемого порошка, количество активного ингредиента стоит выбрать в пределах 0,1 5000 ч. на 1 млн. лучше 1-1000 ч. на 1 млн. Кроме того, инсектицид, соответствующий изобретению, можно использовать в смеси с другими инсектицидом, фунгицидом, удобрениями, регулятором роста растений и т.п. Составление композиций будет далее описано на конкретных примерах. В этом случае вид соединений и добавок и их соотношения не ограничиваются этими примерами и могут изменяться в широких пределах. Кроме того, указаны весовые проценты, если специально не оговорено. Пример получения состава 1. Эмульсия Эмульсия была приготовлена равномерным растворением 30% соединения 6, 20% циклогексанона, 11% полиоксиэтиленалкиларилового эфира, 4% алкилбензолсульфоната кальция и 35% метилнафталина. Пример получения состава 2. Смачиваемый порошок Смачиваемый порошок готовили равномерным смешиванием и измельчением в порошок 40% соединения 3, 15% диатомовой земли, 15% глины, 5% белого угля, 2% натрийдинафтилметандисульфоната и 3% натрийлигнинсульфоната. Пример получения состава 3. Порошок Порошок готовили равномерным смешиванием и измельчением 2% соединения 1,5% диатомовой земли и 93% глины. Пример получения состава 4. Гранулы 5% соединения 7, 2% натриевой соли эфира лаурилового спирта и серной кислоты, 5% натрий-лигнин-сульфоната, 2% карбоксиметилцеллюлоза и 86% глины, которые были равномерно смешаны и измельчены. Затем 100 ч. по весу полученной смеси добавили к 20 ч. воды (по весу) и месили и придавали форму гранул размером 14-24 меш, пропуская через гранулирующую машину путем выдавливания и высушивали, чтобы получить гранулы. Триазольные производные, соответствующие изобретению, эффективны для контроля численности тлей, таких как хлопковая тля, тля зеленых персиков, капустная тля и т.п. цикадки, такие как коричневые цикадки и т.п. листовые цикады, такие как зеленая рисовая цикада, чайная зеленая цикада и т.п. белокрылки, такие как белокрылка тепличная и т.п. парнокрылые вредные насекомые, такие как тутовый шелкопряд, рисовый клоп и т.п. чешуекрылые вредные насекомые, такие как капустная моль, бобовая бабочка-совка, табачная бабочка-совка и т.п. двукрылые вредные насекомые, такие как домашняя муха, москиты и т.п. жесткокрылые вредные насекомые, такие как рисовый долгоносик, соевый долгоносик, тыквенный листоед и т.п. тараканы, такие как Американский таракан, паровая муха, и т.п. клещи, такие как двухпятнистый клещик паутинный, паутинный клещ канзава, красный лимонный клещ и т.п. В особенности инсектицид, соответствующий изобретению, оказывает очень выраженное действие на контролирование численности тлей, таких как хлопковая тля, тля зеленых персиков, кукурузная тля и т.п. дельфацидов, таких как вьюнковая тля, капустная тля и т.п. белокрылок, таких как тепличная белокрылка, белокрылка сладкого картофеля и т.п. парнокрылых вредных насекомых, таких как тутовый шелкопряд и т.п. трипсов, таких как южный желтый трипс и т.п. клещей, таких как двухпятнистый клещик паутинный, паутинный клещ канзава, цитрусовый красный клещ и т.п. Действие соединений, соответствующих изобретению, будет описано в соответствии со следующими примерами испытаний. Более того следующие соединения использовали как сравнительные агенты. Сравнительные агенты от A до C это соединения, опубликованные в Research Disclosure RD 278004, и используются в такой же форме, которая описана выше, тогда как сравнительные химикаты D и E это коммерческие продукты, обычно применяемые для борьбы с тлями. Сравнительный агент A: 3-/2/хлорофенил/-5-/2-хлоропиридин-3-ил/-1-метил-1Н-1,2,4-триазол, Сравнительный агент B: 3-/2/хлорофенил/-5-/6-хлоропиридин-3-ил/-1-метил-1Н-1,2,4-триазол, Сравнительный агент C: 3-/2-хлоро-4-фторфенил/-5-/6-хлоропиридиы-3-ил/-1-метил-1Н-1,2,4-триазол; Сравнительный агент D: 45% смачиваемый порошок метомил Сравнительный агент E: 50% эмульсия этиофенкарб Пример испытаний 1. Проверка инсектицида методом погружения Смачиваемый порошок, приготовленный в соответствии с примером получения состава 2, разводили водой так, чтобы концентрация активного ингредиента была 0,8 ч. на 1 млн. или 0,16 ч. на 1 млн. В полученный разбавленный увлажняемый порошок погружали проростки огурца, предварительно зараженные личинками хлопковой тли, и затем высушивали на воздухе. После высушивания проростки огурцов помещали в термостатированную камеру при 25oC на 3 дня и после этого подсчитывали число погибших личинок, чтобы определить процент их гибели. Тест проводили в двух сериях. Результаты приведены в табл.2. Пример испытаний 2. Проверка инсектицида методом введения Смачиваемый порошок, полученный в соответствии с примером приготовления 2, разводили водой так, чтобы концентрация активного ингредиента была 0,8 ч. на 1 млн. или 0,16 ч. на 1 млн. Полученный разбавленный смачиваемый порошок вносили в горшок, содержащий проростки огурца, предварительно зараженные личинками хлопковой тли. После введения инсектицида проростки огурца помещали в термостат при 25oC на 3 дня и затем подсчитывали число погибших личинок, чтобы определить процент гибели. Тест проводили в двух сериях. Результаты приведены в табл.3. Пример испытания 3. Тест на проверку системного перемещения в почве, улучшающий процесс обработки Гранулы, приготовленные в соответствии с примером приготовления 4/0,5 кг на 10 ар, наносили на стержневые корни проростков огурца, растущих в горшке и предварительно зараженных личинками тли. После такой обработки горшок помещали в теплицу, где число живых взрослых особей и личинок подсчитывали каждые 7 дней. Тест выполняли тремя параллельными сериями. Результаты показаны в табл.4. Пример теста 4. Тест для контроля системного перемещения путем распыления на стебли и листья Смачиваемый порошок, приготовленный в соответствии с примером приготовления 2, разводили водой так, чтобы концентрация активного ингредиента была 100 ч. на 1 млн. Полученный разбавленный смачиваемый порошок распыляли только на верхнюю часть листьев сеянцев огурца, посаженных в горшок и предварительно зараженных с нижней стороны личинками тли, причем нижняя сторона не опрыскивалась. После обработки горшок помещали в теплицу и каждые 5 дней подсчитывали количество взрослых особей и живых личинок на нижней стороне. Тест проводили с тремя параллельными сериями. Результаты приведены в табл.5.
ФОРМУЛА ИЗОБРЕТЕНИЯ1. Производное триазола общей формулы I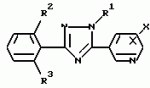 где R1 низшая алкильная группа; R2 и R3 одинаковые или различные атомы галогенов; X хлор, расположенный в 2-м или 6-м положении. 2. Производное по п. 1, где R1 выбирают из метильной, этильной или изопропильной группы, а каждый из R2 и R3 выбирают из фтора, хлора или иода. 3. Производное по п.1, где R1 метильная или этильная группа. 4. Афицидное средство, включающее активный ингредиент и целевые добавки, отличающееся тем, что в качестве активного ингредиента оно содержит соединение формулы I по п.1 в эффективном количестве. 5. Способ получения производного триазола общей формулы I где R1 низшая алкильная группа; R2 и R3 одинаковые или различные атомы галогенов; X хлор, расположенный в 2-м или 6-м положении. 2. Производное по п. 1, где R1 выбирают из метильной, этильной или изопропильной группы, а каждый из R2 и R3 выбирают из фтора, хлора или иода. 3. Производное по п.1, где R1 метильная или этильная группа. 4. Афицидное средство, включающее активный ингредиент и целевые добавки, отличающееся тем, что в качестве активного ингредиента оно содержит соединение формулы I по п.1 в эффективном количестве. 5. Способ получения производного триазола общей формулы I 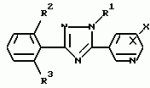 где R1 низшая алкильная группа; R2 и R3 одинаковые или различные атомы галогенов; X хлор, находящийся во 2-м или 6-м положении, отличающийся тем, что включает взаимодействие соединения общей формулы II где R1 низшая алкильная группа; R2 и R3 одинаковые или различные атомы галогенов; X хлор, находящийся во 2-м или 6-м положении, отличающийся тем, что включает взаимодействие соединения общей формулы II 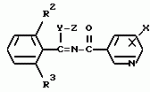 где Y сера или кислород; Z низшая алкильная группа; R2, R3 и X имеют указанные значения, с производным гидразина общей формулы III R1 NHNH2, где R1 имеет указанное значение. 6. Способ получения производного триазола общей формулы I где Y сера или кислород; Z низшая алкильная группа; R2, R3 и X имеют указанные значения, с производным гидразина общей формулы III R1 NHNH2, где R1 имеет указанное значение. 6. Способ получения производного триазола общей формулы I 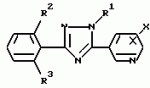 где R1 низшая алкильная группа; R2 и R3 одинаковые или различные атомы галогенов; X хлор, расположенный во 2-м или 6-м положении, отличающийся тем, что включает взаимодействие соединения общей формулы VI где R1 низшая алкильная группа; R2 и R3 одинаковые или различные атомы галогенов; X хлор, расположенный во 2-м или 6-м положении, отличающийся тем, что включает взаимодействие соединения общей формулы VI 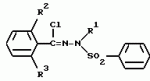 где R1, R2 и R3 имеют указанные значения, с производным бензонитрила общей формулы VII где R1, R2 и R3 имеют указанные значения, с производным бензонитрила общей формулы VII 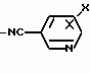 где X имеет указанное значение в присутствии кислоты Льюиса. 7. Способ получения производного триазола общей формулы I где X имеет указанное значение в присутствии кислоты Льюиса. 7. Способ получения производного триазола общей формулы I 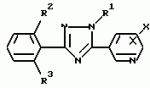 где R1 низшая алкильная группа; R2 и R3 одинаковые или различные атомы галогена; X хлор, находящийся во 2-м или 6-м положении, отличающийся тем, что включает взаимодействие соединения общей формулы VIII где R1 низшая алкильная группа; R2 и R3 одинаковые или различные атомы галогена; X хлор, находящийся во 2-м или 6-м положении, отличающийся тем, что включает взаимодействие соединения общей формулы VIII 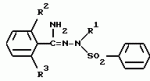 где R1, R2 и R3 имеют указанные значения, с соединением общей формулы V где R1, R2 и R3 имеют указанные значения, с соединением общей формулы V 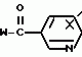 где W галоген; X имеет указанное значение. где W галоген; X имеет указанное значение.Популярные патенты: 2411718 Устройство для внутрипочвенного импульсного дискретного полива растений ... шасси, снабженного внутренней замкнутой полостью, соединенной с блоком подачи воды, шприцевого элемента для импульсной подачи воды внутрь почвы 7, установленного по внешней окружности диска в направлении внешней стороны диска под углом в сторону вращения диска, направленного от центра диска под углом в сторону вращения диска, механической направляющей системы в виде корпуса 11 выдвижного шприца 10 с боковым отверстием 12 для воды и цилиндрическим каналом с гидравлическим уплотнительным кольцом 14, на конце, в котором с возможностью продольного перемещения установлен выдвижной шприц 10, упругой эластичной муфты 8 с внутренним каналом 9, соединяющей механическую направляющую систему ... 2060624 Валкообразующий транспортер жатки-накопителя ... массу по мере ее поступления от переднего к заднему краю валкообразующего транспортера 4. Так как слой растений не имеет сопротивления своему продвижению на всей длине тpанспоpтеpа, то он будет продвигаться в принципе без существенного уплотнения, что важно для обеспечения равномерной и хорошо аэрируемой структуры валка. В отличие от слоя взаимосвязанных растений, одиночные растения, наличие которых на транспортере нельзя исключать априори, могут взаимодействовать с одним (а не с несколькими) грузонесущим элементом. Вынос за пределы заявляемого транспортера и потери таких растений предотвращаются: спереди подпором пальцев мотовила 2 и слоем накопленной на транспортере массы, а сзади ... 2218755 Способ длительного клонирования пайзы (echinochloa frumentacea link) ... А и Б со среды 2КС на среду MS (без регуляторов роста) приводил к затуханию пролиферации каллусной массы и умножению числа побегов без корней по типу кущения. Стоит отметить, что растения без корневой системы, полученные на среде MS, плохо переносили перевод в нестерильные условия. Как правило, в почвенную культуру переводили регенерантные растения со слабой корневой системой, полученные на среде 2КС. Для того чтобы получить растения с корешками, пригодные для перевода в нестерильные условия, проводили пересадки с интервалом, превышающим 35 суток. Таким образом, периодический перенос организованных участков каллусов типа А и Б на свежие среды 2КС обеспечил воспроизводство ... 2265314 Устройство системы зашторивания теплиц с регулируемым ходом ... теплиц с регулируемым ходом, содержащее не связанные с приводом дополнительные штанги с закрепленной на них балкой зашторивания уменьшенного пролета теплицы, установленные с возможностью поступательного движения параллельно направлению движения зашторивания, причем на каждой из дополнительных штанг имеется по два регулируемых упора, между которыми располагается поводок, закрепленный на балке зашторивания предыдущего пролета теплицы и поочередно входящий в контакт при своем движении с упорами, расстояние между которыми обеспечивает свободный ход поводка, уменьшающий ход балки зашторивания уменьшенного пролета теплицы, отличающееся тем, что поводок выполнен в виде поддерживающего ... 2154939 Способ выращивания кроликов и устройство для его осуществления ... и трудозатраты. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Способ выращивания кроликов, включающий кормление и поение, организацию случек и окролов, по крайней мере, одной крольчихи, которую проводят путем регулирования автономных контактов с самцом при содержании ее в клетке, имеющей лазы с задвижками, затем после случки переводят самку в гнездовое отделение, в котором проводят окрол с последующим в нем содержанием крольчихи с крольчатами до достижения последними 15-дневного возраста, после чего крольчат временно, не более чем на час, изолируют в гнезде, а самку допускают к случке, при этом на 30 день производят отъем крольчат от крольчихи и перемещение их в выростное отделение, а затем ... |
Еще из этого раздела: 2188534 Способ уборки льна-долгунца 2421965 Способ возделывания зерновых колосовых культур 2189736 Способ отбора гибридов кукурузы, устойчивых к засухе и стеблевым гнилям 2262844 Способ повышения эффективности воспроизводства икры и численности осетрообразных рыб 2182420 Устройство для перерезания стволов деревьев 2502259 Способ получения водорастворимого бактерицидного препарата 2415552 Питатель молотилки зерноуборочного комбайна 2019938 Рабочий орган почвообрабатывающей машины 2217912 Способ проведения контрольного лова молоди пелагических рыб, в частности лососевых, и обкидной невод 2450135 Двигатель самоходной машины |
Изобретения в сельском хозяйстве
Обработка почвы в сельском и лесном хозяйствах
Посадка, посев, удобрение
Уборка урожая, жатва
Обработка и хранение продуктов полеводства и садоводства
Садоводство, разведение овощей, цветов, риса, фруктов, винограда, лесное хозяйство
Новые виды растений или способы их выращивания
Производство молочных продуктов
Животноводство, разведение и содержание птицы, рыбы, насекомых, рыбоводство, рыболовство
Поимка, отлов или отпугивание животных
Консервирование туш животных, или растений или их частей
Биоцидная, репеллентная, аттрактантная или регулирующая рост растений активность химических соединений или препаратов
Хлебопекарные печи, машины и прочее оборудование для хлебопечения
Машины или оборудование для приготовления или обработки теста
Обработка муки или теста для выпечки, способы выпечки, мучные изделия
|
|
||