N-(4-пиридил- или 4-хинолинил)арилацетамидные производныеПатент на изобретение №: 2055070 Автор: Рональд Э.Хэклер[US], Глен П.Джордан[US], Питер Л.Джонсон[US], Брайен Р.Торин[US], Джек Г.Самаритони[US] Патентообладатель: Дауэланко (US) Дата публикации: 27 Февраля, 1996 Адрес для переписки: подача заявки02.09.1992 публикация патента27.02.1996 Изображения  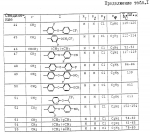 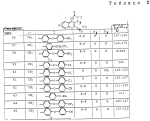 Использование: в химии гетероциклических веществ, в частности в способе получения N-(4-пиридил-или 4-хинолинил)арилацетамидных производных. Сущность изобретения: продукт N-(4-пиридил- или 4-хинолил)арилацетамидные производные ф-лы 1: (CR2 двойная связь CR1 - N двойная связь CR3 - CR4 двойная связь C (вторая связь с CR2) - NR - C(O) - Y"Z), где R - водород и R1, R2, R3 и R4 имеют одно из следующих значений: а) R3 и R4 - водород, а R1 и R2 - независимы, галоген или C1 - C4-алкил; б) один из R1, R2, R3 и R4 - C1 - C4-алкил, а другие - водород; в) R1, R2, R3 и R4 независимы, водород или галоген; г) R1 и R2 - вместе образуют цепь: (-СН двойная связь СН-СН двойная связь СН-), которая может быть замещена атомом фтора, а R3 и R4 - водородом; Y"Z - вместе образуют неразветвленную или разветвленную насыщенную углеводородную C4 - C1-цепь или Y - метиленовая группа, а Z - фенил, моно- или дизамещенный C1 - C6-алкилом, галогеном, трифторметилом, C1 - C4-алкокси группа, которая м. б. замещена фтором, фенилом, феноксигруппой, которая может иметь один или два заместителя, выбранные из C1 - C4-алкокси, галогена, трифторметила, циано, нитро, или группой трифторметилфенилмеркапто; бета-нафтил или группа: /-(С6 Н4)-4-О-С1-С4-фторзамещенный алкил. Реагент 1: 4-аминопиридин. Реагент 2: 4-бифенилуксусная кислота. Реагент 3: 1,3-дициклогексилкарбодиимид. Условия реакции: в среде метиленхлорида, а при выделении целевого продукта перекристаллизация из смеси гексана и этилацетата. 5 табл. , , , , , , , , , ОПИСАНИЕ ИЗОБРЕТЕНИЯ К ПАТЕНТУИзобретение относится к новым соединениям, которые могут быть использованы в качестве нематоцидов, инсектицидов, акарицидов и растительных фунгицидов, а также к способам борьбы с нематодами, насекомыми, клещами и грибками. Существует крайняя необходимость в получении новых нематоцидов, инсектицидов, акарицидов и растительных фунгицидов. Имеющиеся нематоциды, как правило обладают очень высокой токсичностью по отношению к млекопитающим, и их использование требует очень больших доз. Значительную ценность могли бы представлять нематоциды, которые можно было бы использовать в более низких дозах и которые имели бы меньшую токсичность по отношению к млекопитающим. Клещи и насекомые обладают способностью вырабатывать устойчивость к используемым в настоящее время акарицидам и инсектицидам. Резистентность к инсектицидам у anthropods является широко распространенным явлением, например, по крайней мере 400 видов являются резистентными к одному или нескольким инсектицидам. Выработка устойчивости к некотоpым видам давно использующихся инсектицидов, таких как ДДТ, карбаматы, и органофосфаты, является хорошо известным фактором. Однако наблюдается резистентность даже к новым пиретроидным инсектицидам и акарицидам. Аналогичным образом целевые патогены быстро вырабатывают устойчивость к используемым в настоящее время фунгицидам. По крайней мере 50 видов грибков обладают приобретенной устойчивостью к бензимидазоловым фунгицидам. Даже недавно полученные фунгициды, такие как ацилаланины, которые считались прекрасным средством борьбы против фитофтороза картофеля и ложной мучнистой росы винограда в полевых условиях, дают меньшую эффективность из-за приобретенной резистентности указанных возбудителей. Поэтому получение новых инсектицидов, акарицидов и фунгицидов, а особенно соединений с новым или атипичным механизмом воздействия, является крайне необходимым. Настоящее изобретение относится к соединениям формулы I: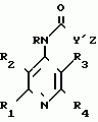 (I) и к их N-оксидам и солям, где R является Н, (С1-С4)алкилом, или бензилом; R1, R2, R3 и R4 имеют одно из следующих значений: а) R3 и R4 являются Н, а R1 и R2 независимо являются: галогеном, (С1-С4)-алкилом, галоген (С1-С4)алкилом, (С3-С4)разветвленным алкилом, (С1-С4)циклоалкилом, (С1-С4)алкокси или галоген(С1-С4)алкокси; b) один из R1, R2, R3 и R4 является (С1-С4)алкилом, (С3-С4)разветвленным алкилом, (С1-С4)алкокси, галоген(С1-С4)алкилом, галоген(С1-С4)алкокси, (С1-С4)алкилтио, (С1-С4)алкилсульфинилом, (С1-С4)алкилсульфонилом, арилом или замещенной аминогруппой, а остальные являются Н; с) R1, R2, R3 и R4 независимо являются Н или галогеном; d) R1 и R2 вместе взятые образуют (С5-С6)насыщенное или ненасыщенное карбокцилическое кольцо, которое является необязательно замещенным одной или двумя группами, выбранными из галогена, (С1-С4)алкила, (С1-С4)разветвленного алкила, галоген(С1-С4)алкила, (С3-С7)циклоалкила, (С1-С4)алкокси, галоген(С1-С4)алкокси или NO2, a R3и R4 являются Н; R5 является Н, (С1-С4)алкилом или (С1-С4)ацилом; R6 и R7 независимо представляют собой (С1-С4)алкил, (С3-С4)разветвленный алкил; фенил или замещенный фенил; Y"Z, взятые вместе, образуют (С4-С11)насыщенную или ненасыщенную углеводородную цепь, которая может быть прямой или разветвленной и которая может (но необязательно) включать в себя гетероатом, выбранный из 0, NR5r, S, SO, SO2 или Si R6R7, где R6 и R7 определены выше, и которая необязательно является замещенной одной или несколькими группами, независимо выбранными из (С1-С4)алкила, (С2-С4)алкенила, (С2-С4)алкинила, разветвленного (С3-С7)алкила, (С3-С7)циклоалкила, (С3-С7)циклоалкенила, галогена, галоген (С1-С4)алкила, галоген (С1-С4)алкокси, гидрокси или (С1-С4)ацила; или Y" представляет собой связь или двухвалентный углеводородный радикал, имеющий 1-5 атомов углерода и необязательно замещенный (С1-С4)алкилом, (С2-С4)алкенилом, (С2-С4)алкинилом, разветвленным (С3-С7)алкилом, (С3-С7)циклоалкилом, или (С3-С7)циклоалкенилом, галогеном, галоген (С1-С4)алкилом, галоген (С1-С4)алкокси, гидрокси, CN, или (С1-С4)ацилом; и Z представляет собой: a) арил, или b) (С3-С8)циклоалкил или циклоалкенил, не обязательно замещенный одной или несколькими группами, независимо выбранными из (С1-С4)алкила, (С1-С4)алкокси, галоген (С1-С4)алкила, галоген(С1-С4)алкокси, галогена, гидрокси, или (С1-С4)ацила, где: арил представляет собой: а) фенильную группу, не обязательно замещенную одной или несколькими группами, независимо выбранными из: галогена, I, (C3-C8)циклоалкила, (С3-С8)циклоалкенила, фенокси, замещенной фенокси, фенилтио, замещенной фенилтио, фенила, NO2, - (I) и к их N-оксидам и солям, где R является Н, (С1-С4)алкилом, или бензилом; R1, R2, R3 и R4 имеют одно из следующих значений: а) R3 и R4 являются Н, а R1 и R2 независимо являются: галогеном, (С1-С4)-алкилом, галоген (С1-С4)алкилом, (С3-С4)разветвленным алкилом, (С1-С4)циклоалкилом, (С1-С4)алкокси или галоген(С1-С4)алкокси; b) один из R1, R2, R3 и R4 является (С1-С4)алкилом, (С3-С4)разветвленным алкилом, (С1-С4)алкокси, галоген(С1-С4)алкилом, галоген(С1-С4)алкокси, (С1-С4)алкилтио, (С1-С4)алкилсульфинилом, (С1-С4)алкилсульфонилом, арилом или замещенной аминогруппой, а остальные являются Н; с) R1, R2, R3 и R4 независимо являются Н или галогеном; d) R1 и R2 вместе взятые образуют (С5-С6)насыщенное или ненасыщенное карбокцилическое кольцо, которое является необязательно замещенным одной или двумя группами, выбранными из галогена, (С1-С4)алкила, (С1-С4)разветвленного алкила, галоген(С1-С4)алкила, (С3-С7)циклоалкила, (С1-С4)алкокси, галоген(С1-С4)алкокси или NO2, a R3и R4 являются Н; R5 является Н, (С1-С4)алкилом или (С1-С4)ацилом; R6 и R7 независимо представляют собой (С1-С4)алкил, (С3-С4)разветвленный алкил; фенил или замещенный фенил; Y"Z, взятые вместе, образуют (С4-С11)насыщенную или ненасыщенную углеводородную цепь, которая может быть прямой или разветвленной и которая может (но необязательно) включать в себя гетероатом, выбранный из 0, NR5r, S, SO, SO2 или Si R6R7, где R6 и R7 определены выше, и которая необязательно является замещенной одной или несколькими группами, независимо выбранными из (С1-С4)алкила, (С2-С4)алкенила, (С2-С4)алкинила, разветвленного (С3-С7)алкила, (С3-С7)циклоалкила, (С3-С7)циклоалкенила, галогена, галоген (С1-С4)алкила, галоген (С1-С4)алкокси, гидрокси или (С1-С4)ацила; или Y" представляет собой связь или двухвалентный углеводородный радикал, имеющий 1-5 атомов углерода и необязательно замещенный (С1-С4)алкилом, (С2-С4)алкенилом, (С2-С4)алкинилом, разветвленным (С3-С7)алкилом, (С3-С7)циклоалкилом, или (С3-С7)циклоалкенилом, галогеном, галоген (С1-С4)алкилом, галоген (С1-С4)алкокси, гидрокси, CN, или (С1-С4)ацилом; и Z представляет собой: a) арил, или b) (С3-С8)циклоалкил или циклоалкенил, не обязательно замещенный одной или несколькими группами, независимо выбранными из (С1-С4)алкила, (С1-С4)алкокси, галоген (С1-С4)алкила, галоген(С1-С4)алкокси, галогена, гидрокси, или (С1-С4)ацила, где: арил представляет собой: а) фенильную группу, не обязательно замещенную одной или несколькими группами, независимо выбранными из: галогена, I, (C3-C8)циклоалкила, (С3-С8)циклоалкенила, фенокси, замещенной фенокси, фенилтио, замещенной фенилтио, фенила, NO2, -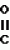 -R8, где R8 представляет собой (С1-С7)алкил, галоген(С3-С7)алкил, (С3-С7) разветвленный алкил, галоген(С3-С7)разветвленный алкил, (С3-С7)циклоалкил, галоген(С3-С7)циклоалкил, (С1-С7)алкокси, фенил, или замещенный фенил, ацетокси, ОН, CN, Si R9R10R11 или OSi R9R10R11, где R9, R10 и R11 независимо являются (С1-С4)алкилом, (С3-С4)разветвленным алкилом, фенилом, или замещенным фенилом, N R12R13, где R12 и R13 независимо являются Н, (С1-С4)алкилом, или (С1-С4)ацилом, S(0)R14, SO2R14, где R14 является (С1-С10)алкилом, фенилом, или замещенным фенилом; (С1-С12) насыщенной или ненасыщенной углеводородной цепи прямой или разветвленной, которая не обязательно включает в себя гетероатом, выбранный из O, S, SO,SO2, NR5, или Si R6R7, где R5,R6 и R7 определены выше, и которая не обязательно является замещенной галогеном, галоген(С1-С4)алкокси, гидрокси, (С3-С8) циклоалкилом или циклоалкенилом, (С1-С4)ацилом, фенокси, замещенным фенокси, фенилом, замещенным фенилом, фенилтио, или замещенной фенилтио; (С1-С7)алкокси, не обязательно замещенной галогеном, фенилом, замещенным фенилом, (С3-С8)циклоалкилом или циклоалкенилом, фенокси, или замещенной фенокси; (С1-С7)алкилтио, не обязательно замещенной галогеном, фенилом, замещенным фенилом, (С3-С8)циклоалкилом или циклоалкенилом, фенокси или замещенной фенокси; b) фурильную группу формулы III; -R8, где R8 представляет собой (С1-С7)алкил, галоген(С3-С7)алкил, (С3-С7) разветвленный алкил, галоген(С3-С7)разветвленный алкил, (С3-С7)циклоалкил, галоген(С3-С7)циклоалкил, (С1-С7)алкокси, фенил, или замещенный фенил, ацетокси, ОН, CN, Si R9R10R11 или OSi R9R10R11, где R9, R10 и R11 независимо являются (С1-С4)алкилом, (С3-С4)разветвленным алкилом, фенилом, или замещенным фенилом, N R12R13, где R12 и R13 независимо являются Н, (С1-С4)алкилом, или (С1-С4)ацилом, S(0)R14, SO2R14, где R14 является (С1-С10)алкилом, фенилом, или замещенным фенилом; (С1-С12) насыщенной или ненасыщенной углеводородной цепи прямой или разветвленной, которая не обязательно включает в себя гетероатом, выбранный из O, S, SO,SO2, NR5, или Si R6R7, где R5,R6 и R7 определены выше, и которая не обязательно является замещенной галогеном, галоген(С1-С4)алкокси, гидрокси, (С3-С8) циклоалкилом или циклоалкенилом, (С1-С4)ацилом, фенокси, замещенным фенокси, фенилом, замещенным фенилом, фенилтио, или замещенной фенилтио; (С1-С7)алкокси, не обязательно замещенной галогеном, фенилом, замещенным фенилом, (С3-С8)циклоалкилом или циклоалкенилом, фенокси, или замещенной фенокси; (С1-С7)алкилтио, не обязательно замещенной галогеном, фенилом, замещенным фенилом, (С3-С8)циклоалкилом или циклоалкенилом, фенокси или замещенной фенокси; b) фурильную группу формулы III; 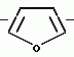 R15 (III) где R15 является Н, галогеном, галогенметилом, CN, NO2, (C1-С4)алкилом, (С3-С4)разветвленным алкилом, фенилом, (С1-С4)алкокси, галоген (С1-С4)алкокси; с) тиениловую группу формулы IV; R15 (III) где R15 является Н, галогеном, галогенметилом, CN, NO2, (C1-С4)алкилом, (С3-С4)разветвленным алкилом, фенилом, (С1-С4)алкокси, галоген (С1-С4)алкокси; с) тиениловую группу формулы IV; 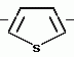 R16 (IV) где R16 является Н, галогеном, галогенметилом, CN. NO2, (C1-С4)алкилом, (С3-С4)разветвленным алкилом, фенилом, (С1-С4) алкокси, галоген(С1-С4)алкокси или тиенилом; d) группу формулы V или VI: R16 (IV) где R16 является Н, галогеном, галогенметилом, CN. NO2, (C1-С4)алкилом, (С3-С4)разветвленным алкилом, фенилом, (С1-С4) алкокси, галоген(С1-С4)алкокси или тиенилом; d) группу формулы V или VI: 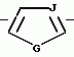 R15 (V), R15 (V), 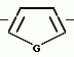 R15 (VI) где R15 определен в параграфе (b), J является N или СН, а G является O,N R17, или S, при условии, что, если J не является N, то G является NR, где R17 представляет собой Н, (С1-С4)алкил, (С1-С4)ацил, фенилсульфонил или замещенный фенил или замещенный фенилсульфонил; е) группу, выбранную из: не обязательно замещенного нафтила, дигидронафтила, тетрагидронафтила и декагидронафтила; не обязательно замещенного индолила; 1,3-бензодиоксолила; 2,6-диметил-4-морфолинила; 1-адамантила; (f) группу формулы: R15 (VI) где R15 определен в параграфе (b), J является N или СН, а G является O,N R17, или S, при условии, что, если J не является N, то G является NR, где R17 представляет собой Н, (С1-С4)алкил, (С1-С4)ацил, фенилсульфонил или замещенный фенил или замещенный фенилсульфонил; е) группу, выбранную из: не обязательно замещенного нафтила, дигидронафтила, тетрагидронафтила и декагидронафтила; не обязательно замещенного индолила; 1,3-бензодиоксолила; 2,6-диметил-4-морфолинила; 1-адамантила; (f) группу формулы: 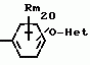 где m=4, R20 является независимо Н, галогеном, низшим алкилом, низшей алкоксигруппой, галогеналкилом, галогеналкокси, NO2, CN, низшим алкилкарбонилом, фенокси, или замещенной фенокси при условии, что по крайней мере два из R20 выбирают из Н и F; а Het представляет собой пиридил, пиразинил, пиримидилин, или пиридазинил, не обязательно замещенный одной или несколькими группами, выбранными из галогена, низшего алкила, низшей алкокси-группы, галогеналкила, галогеналкокси, NO2, CN и низшей алкилкарбонильной группы; g) группу формулы: где m=4, R20 является независимо Н, галогеном, низшим алкилом, низшей алкоксигруппой, галогеналкилом, галогеналкокси, NO2, CN, низшим алкилкарбонилом, фенокси, или замещенной фенокси при условии, что по крайней мере два из R20 выбирают из Н и F; а Het представляет собой пиридил, пиразинил, пиримидилин, или пиридазинил, не обязательно замещенный одной или несколькими группами, выбранными из галогена, низшего алкила, низшей алкокси-группы, галогеналкила, галогеналкокси, NO2, CN и низшей алкилкарбонильной группы; g) группу формулы:  R21 где один из Х2 и Х3 является N, а другой является СН; R21 является -Z-R22, фенилом, или замещенным фенилом; Z является О или S; R22 является (С1-С4)алкилом, (С3-С7) разветвленным алкилом галогеном(С1-С7)алкилом, галоген(С3-С7)разветвленным алкилилом, (С1-С4)алкокси замещенным (С1-С4)алкилом, или нафтилом или фенилом, любой из которых может быть (но не обязательно) замещенным одной, двумя или тремя группами, выбранными из галогена, (С1-С10)алкила, разветвленного (С3-С7)алкила, галоген(С1-С7)алкила, гидрокси (С1-С7)алкила, (С1-С4)алкокси, галоген(С1-С4)алкокси, фенокси, замешенной феноксигруппы, фенила, замещенного фенила, CN, NO2, OH, (C1-C4)алканоилокси, или бензилокси. Настоящее изобретение также относится к новым соединениям формулы IA: R21 где один из Х2 и Х3 является N, а другой является СН; R21 является -Z-R22, фенилом, или замещенным фенилом; Z является О или S; R22 является (С1-С4)алкилом, (С3-С7) разветвленным алкилом галогеном(С1-С7)алкилом, галоген(С3-С7)разветвленным алкилилом, (С1-С4)алкокси замещенным (С1-С4)алкилом, или нафтилом или фенилом, любой из которых может быть (но не обязательно) замещенным одной, двумя или тремя группами, выбранными из галогена, (С1-С10)алкила, разветвленного (С3-С7)алкила, галоген(С1-С7)алкила, гидрокси (С1-С7)алкила, (С1-С4)алкокси, галоген(С1-С4)алкокси, фенокси, замешенной феноксигруппы, фенила, замещенного фенила, CN, NO2, OH, (C1-C4)алканоилокси, или бензилокси. Настоящее изобретение также относится к новым соединениям формулы IA: 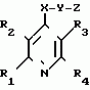 (IA) и их N-оксидам и солям, где R1,R2,R3 и R4 имеют одно из следующих определений: а) R3 и R4 являются Н, а R1 и R2 являются независимо галогеном, (С1-С4)-алкилом, галоген(С1-С4)алкилом, (С3-С4)разветвленным алкилом, (С1-С4)циклоалкилом, (С1-С4)алкокси, или галоген(С1-С4)алкокси; b) один из R1,R2,R3 и R4 является (С1-С4)алкилом, (С3-С4)разветвленным алкилом, (С1-С4)алкокси, галоген(С1-С4)алкилом, галоген(С1-С4)алкокси, (С1-С4)алкилтио, (С1-С4) алкилсульфинилом, (С1-С4)алкилсульфонилом, арилом, или замещенной аминогруппой; а остальные являются Н; или с) R1, R2, R3 и R4 являются независимо галогеном или Н; Х является O,S, или NR5; R5 является Н, (С1-С4)алкилом или (С1-С4)ацилом; R6 и R7 независимо являются (С1-С4)алкилом, (С3-С4)разветвленным алкилом, фенилом, или замещенным фенилом; YZ, взятые вместе образуют (С5-С12)насыщенную или ненасыщенную углеводородную цепь, прямую или разветвленную, которая не обязательно включает в себя гетероатом, выбранный из О,NR5, S, SO, SO2 или SiR6R7, где R5, R6 и R7 определены выше, и которая является не обязательно замещенной одной или несколькими группами, независимо выбранными из (С1-С4)алкила, (С2-С4)алкенила, (С2-С4)алкинила, разветвленного (С3-С7)алкила, (С3-С7)циклоалкила, (С3-С7)циклоалкенила, галогена, галоген(С1-С4)алкила, галоген(С1-С4)алкокси, гидрокси, или (С1-С4)ацила, или Y представляет собой связь или двухвалентный углеводородный радикал, имеющий 1-6 атомов углерода, и не обязательно замещенный одной или несколькими группами, независимо выбранными из (С1-С4)алкила, (С2-С4)алкенила или (С3-С7)алкинила, разветвленого (С3-С7)алкила, (С3-С7)циклоалкила, (С3-С7)циклоалкенила, галогена, галоген(С1-С4)алкила, галоген(С1-С4)алкокси, гидрокси, или (С1-С4)ацила; и Z представляет собой а) арил, или b) (С3-С8)циклоалкил или циклоалкенил, не обязательно замещенный одной или несколькими группами, независимо выбранными из (С1-С4)алкила, (С1-С4)алкокси, галоген(С1-С4)алкила, галоген(С1-С4)алкокси, галогена, гидрокси, или (С1-С4)ацила; где арил представляет собой: а) фенильную группу, не обязательно замещенную одной или несколькими группами, независимо выбранными из: галогена, J, (C3-C8)циклоалкила, (С3-С8)циклоалкенила, фенокси, замещенной фенокси, фенилтио, замещенной фенилтио, фенила, замещенного фенила, NO2 O -C-R8, где R8 представляет собой (С1-С7)алкил, галоген(С1-С7)алкил, (С3-С7)разветвленный алкил, галоген(С3-С7)раз- ветвленный алкил, (С3-С7)циклоалкил, галоген(С3-С7)циклоалкил, (С1-С7)алкокси, фенил, или замещенный фенил; ацетокси, ОН, СN, SiR9R10R11 или OSiR9R10R11, где R9, R10 или R11 являются независимо (С1-С4)алкилом, (С3-С4)разветвленным алкилом, фенилом или замещенным фенилом, NR12R13, где R12 и R13 являются Н, (С1-С4)-алкилом, или (С1-С4)ацилом, S(O)R14, или SO2R14, где R14 является (С1-С10)алкилом, фенилом, или замещенным фенилом; (С1-С12)насыщенной или ненасыщенной углеводородной цепи, прямой или разветвленной, которая необязательно включает в себя гетероатом, выбранный из O, S, SO, SO2, NR5, или SiR6R7, где R5,R6 и R7 определены выше, и которая является не обязательно замещенной галогеном, галоген(С1-С4)алкокси, гидрокси, (С3-С8)циклоалкилом или циклоалкенилом, (С1-С4)-ацилом, фенокси, замещенной феноксигруппой, фенилтио, или замещенной фенилтиогруппой; (С1-С7)алкокси, не обязательно замещенной галогеном, фенилом, замещенным фенилом, (С3-С8)циклоалкилом или циклоалкенилом, фенокси, или замещенной фенокси; или (С1-С7)алкилтио, не обязательно замещенной галогеном, фенилом, замещенным фенилом, (С3-С8)циклоалкилом или циклоалкенилом, фенокси, или замещенной фенокси; b) фурильную группу формулы III: (IA) и их N-оксидам и солям, где R1,R2,R3 и R4 имеют одно из следующих определений: а) R3 и R4 являются Н, а R1 и R2 являются независимо галогеном, (С1-С4)-алкилом, галоген(С1-С4)алкилом, (С3-С4)разветвленным алкилом, (С1-С4)циклоалкилом, (С1-С4)алкокси, или галоген(С1-С4)алкокси; b) один из R1,R2,R3 и R4 является (С1-С4)алкилом, (С3-С4)разветвленным алкилом, (С1-С4)алкокси, галоген(С1-С4)алкилом, галоген(С1-С4)алкокси, (С1-С4)алкилтио, (С1-С4) алкилсульфинилом, (С1-С4)алкилсульфонилом, арилом, или замещенной аминогруппой; а остальные являются Н; или с) R1, R2, R3 и R4 являются независимо галогеном или Н; Х является O,S, или NR5; R5 является Н, (С1-С4)алкилом или (С1-С4)ацилом; R6 и R7 независимо являются (С1-С4)алкилом, (С3-С4)разветвленным алкилом, фенилом, или замещенным фенилом; YZ, взятые вместе образуют (С5-С12)насыщенную или ненасыщенную углеводородную цепь, прямую или разветвленную, которая не обязательно включает в себя гетероатом, выбранный из О,NR5, S, SO, SO2 или SiR6R7, где R5, R6 и R7 определены выше, и которая является не обязательно замещенной одной или несколькими группами, независимо выбранными из (С1-С4)алкила, (С2-С4)алкенила, (С2-С4)алкинила, разветвленного (С3-С7)алкила, (С3-С7)циклоалкила, (С3-С7)циклоалкенила, галогена, галоген(С1-С4)алкила, галоген(С1-С4)алкокси, гидрокси, или (С1-С4)ацила, или Y представляет собой связь или двухвалентный углеводородный радикал, имеющий 1-6 атомов углерода, и не обязательно замещенный одной или несколькими группами, независимо выбранными из (С1-С4)алкила, (С2-С4)алкенила или (С3-С7)алкинила, разветвленого (С3-С7)алкила, (С3-С7)циклоалкила, (С3-С7)циклоалкенила, галогена, галоген(С1-С4)алкила, галоген(С1-С4)алкокси, гидрокси, или (С1-С4)ацила; и Z представляет собой а) арил, или b) (С3-С8)циклоалкил или циклоалкенил, не обязательно замещенный одной или несколькими группами, независимо выбранными из (С1-С4)алкила, (С1-С4)алкокси, галоген(С1-С4)алкила, галоген(С1-С4)алкокси, галогена, гидрокси, или (С1-С4)ацила; где арил представляет собой: а) фенильную группу, не обязательно замещенную одной или несколькими группами, независимо выбранными из: галогена, J, (C3-C8)циклоалкила, (С3-С8)циклоалкенила, фенокси, замещенной фенокси, фенилтио, замещенной фенилтио, фенила, замещенного фенила, NO2 O -C-R8, где R8 представляет собой (С1-С7)алкил, галоген(С1-С7)алкил, (С3-С7)разветвленный алкил, галоген(С3-С7)раз- ветвленный алкил, (С3-С7)циклоалкил, галоген(С3-С7)циклоалкил, (С1-С7)алкокси, фенил, или замещенный фенил; ацетокси, ОН, СN, SiR9R10R11 или OSiR9R10R11, где R9, R10 или R11 являются независимо (С1-С4)алкилом, (С3-С4)разветвленным алкилом, фенилом или замещенным фенилом, NR12R13, где R12 и R13 являются Н, (С1-С4)-алкилом, или (С1-С4)ацилом, S(O)R14, или SO2R14, где R14 является (С1-С10)алкилом, фенилом, или замещенным фенилом; (С1-С12)насыщенной или ненасыщенной углеводородной цепи, прямой или разветвленной, которая необязательно включает в себя гетероатом, выбранный из O, S, SO, SO2, NR5, или SiR6R7, где R5,R6 и R7 определены выше, и которая является не обязательно замещенной галогеном, галоген(С1-С4)алкокси, гидрокси, (С3-С8)циклоалкилом или циклоалкенилом, (С1-С4)-ацилом, фенокси, замещенной феноксигруппой, фенилтио, или замещенной фенилтиогруппой; (С1-С7)алкокси, не обязательно замещенной галогеном, фенилом, замещенным фенилом, (С3-С8)циклоалкилом или циклоалкенилом, фенокси, или замещенной фенокси; или (С1-С7)алкилтио, не обязательно замещенной галогеном, фенилом, замещенным фенилом, (С3-С8)циклоалкилом или циклоалкенилом, фенокси, или замещенной фенокси; b) фурильную группу формулы III: 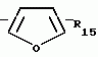 (III) где R15 является Н, галогеном, галогенметилом, СN, NO2, (C1-С4)алкилом, разветвленным (С3-С4)алкилом, фенилом, (С1-С4)-алко- кси, или галоген (С1-С4)алкокси; с) тиенильную группу формулы IV: (III) где R15 является Н, галогеном, галогенметилом, СN, NO2, (C1-С4)алкилом, разветвленным (С3-С4)алкилом, фенилом, (С1-С4)-алко- кси, или галоген (С1-С4)алкокси; с) тиенильную группу формулы IV: 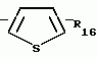 (IV) где R16 является Н, галогеном, галогенметилом, CN, NO2, (C1-С4)алкилом, разветвленным (С3-С4)алкилом, фенилом, (С1-С4)ал- кокси, галоген(С1-С4)алкокси, или тиенилом; d) группу формулы V или VI: (IV) где R16 является Н, галогеном, галогенметилом, CN, NO2, (C1-С4)алкилом, разветвленным (С3-С4)алкилом, фенилом, (С1-С4)ал- кокси, галоген(С1-С4)алкокси, или тиенилом; d) группу формулы V или VI: 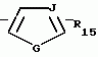 (V), (V) (V), (V) 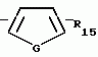 (VI) (VI) где R15 определен в параграфе (b), N является N или СН, а G является О, NR17 или S, при условии, что, если J не является J, то G является NR, где R17 представляет собой Н, (С1-С4)алкил, (С1-С4)ацил, фенилсульфонил, или замещенный фенилсульфонил; е) группу, выбранную из: не обязательно замещенного нафтила, дигидронафтила, тетрагидронафтила, и декагидронафтила; не обязательно замещенного пиридила; не обязательно замещенного индолила; 1,3-бензодиоксолила; 2,6-диметил-4-морфолинила; и 1-адамантила. Изобретение также относится к способу борьбы с популяцией нематод, заключающемуся в том, что очаг заражения нематодами обрабатывают некоторым инактивирующим нематоды количеством соединения формулы I, определенным выше. Кроме того, изобретение относится к способу борьбы с популяцией насекомых или клещей, заключающемуся в том, что очаг заражения насекомыми или клещами обрабатывают некоторым количеством соединения формулы I, эффективным для инактивации насекомых или клещей. Изобретение также относится к способу борьбы с растительными патогенами, заключающемуся в том, что очаг заражения указанными патогенами обрабатывают эффективным количеством соединения формулы I. В данном описании все температуры даются в градусах Цельсия, а все процентные содержания в мас. если это не оговорено особо. Термин "галоген", относится к атому фтора, хлора или брома. Термины "алкокси". "галогеналкил", "алкилсульфинил" и "алкилсульфонил" относятся к группам с прямой и разветвленной цепью. Термины "замещенный фенил", "замещенная феноксигруппа", "замещенная фенилтиогруппа" и "замещенный фенилсульфонил" относятся к таким группам, в которых фенильное кольцо является замещенным одной, двумя или тремя группами, независимо выбранными из галогена, J, (C1-С10)алкила, разветвленного (С3-С6)алкила, галоген(С1-С7)алкила, гидрокси(С1-С7)алкила, (С1-С7)алкокси, галоген(С1-С7) алкокси, фенокси, замещенной фенокси, фенила, замещенного фенила, NO2, OH, CN, (С1-С4)алканоила, бензоила, (С1-С4)алканоилокси, (С1-С4)алкоксикарбонила, феноксикарбонила или бензоилокси. Термины "замещенный нафтил" и "замещенный индолил" относятся к циклическим системам, замещенным одной или несколькими группами, независимо выбранными из галогена, галоген(С1-С4)алкила, СN, NO2, (C1-C4)алкила, разветвленного (С3-С4)алкила, фенила, (С1-С4)алкокси или галоген(С1-С4)алкокси. Термин "карбоциклическое ядро" относится к насыщенному или ненасыщенному углеродному кольцу, содержащему пять или шесть атомов углерода. Термин "ненасыщенная углеводородная цепь" относится к углеводородной цепи, содержащей один или несколько участков ненасыщенности. Термин "ЖХВД" означает жидкостную хроматографию высокого давления. Термин "двухвалентный углеводородный радикал" относится к двухвалентным радикалам, полученным из нормальных алканов путем удаления атомов водорода от каждого из двух концевых атомов углерода цепи, например таким, как метилен, этилен, триметилен, тетраметилен и т.п. Термин "замещенная аминогруппа" относится к аминогруппе, замещенной одной или двумя (С1-С4)алкильными группами или одной (С1-С4)алканоильной группой. Термин "низший алкил" относится к прямым (С1-С6)углеводородным цепям и к разветвленным и циклическим (С3-С6)углеводородным группам. Термины "низший алкенил" и "низший алкинил" относятся к прямым (С2-С6)углеводородным цепям и к разветвленным (С3-С6)углеводородным группам, содержащим по крайней мере одну ненасыщенную связь. Термины "низшие алкокси" и "низшие алкилтио" относятся к О-низшим алкильным и S-низшим алкильным группам. Термин "галогеналкил" относится к низшим алкильным группам, замещенным одним или несколькими атомами галогена. Термин "галогеналкокси" относится к низшим алкоксигруппам, замещенным одним или несколькими атомами галогена. Если это не оговорено особо, то указание на то, что группа может быть замещенной одним или несколькими заместителями, выбранными из определенного класса групп, означает, что эти заместители могут быть независимо выбранными из указанного класса. Предпочтительными соединениями формулы I являются соединения следующих классов: а) соединения формулы I, где Y является -СН2-; b) соединения формулы I, где Z является фенилом; с) соединения формулы I, где Z является замещенной фенильной группой, определенной в параграфе а) в характеризации "арила"; d) соединения формулы I, где Z является фенильной группой, замещенной (С2-С4)алкоксигруппой; е) соединения формул I, где Z является фенильной группой, замещенной разветвленной С3-С7алкоксигруппой; f) соединения формулы I, где Z является фенильной группой, замещенной галогеном(С2-С4)алкоксигруппой; g) соединения формулы I, где Z является фенильной группой, замещенной разветвленной галоген(С3-С7)алкоксигруппой; h) соединения формулы I, где Z является фенильной группой, замещенной феноксигруппой, или замещенной феноксигруппой. i) соединения любой из вышеуказанных групп (c)-(h), где фенильная группа является однозамещенной в 4 положении; j) соединения формулы I, где R1 является (С1-С4)-алкилом, а R2является галогеном; l) соединения формулы I, где R1 является этилом, а R2 является хлором; m) соединения формулы I, где R1 и R2, взятые вместе, образуют R (VI) (VI) где R15 определен в параграфе (b), N является N или СН, а G является О, NR17 или S, при условии, что, если J не является J, то G является NR, где R17 представляет собой Н, (С1-С4)алкил, (С1-С4)ацил, фенилсульфонил, или замещенный фенилсульфонил; е) группу, выбранную из: не обязательно замещенного нафтила, дигидронафтила, тетрагидронафтила, и декагидронафтила; не обязательно замещенного пиридила; не обязательно замещенного индолила; 1,3-бензодиоксолила; 2,6-диметил-4-морфолинила; и 1-адамантила. Изобретение также относится к способу борьбы с популяцией нематод, заключающемуся в том, что очаг заражения нематодами обрабатывают некоторым инактивирующим нематоды количеством соединения формулы I, определенным выше. Кроме того, изобретение относится к способу борьбы с популяцией насекомых или клещей, заключающемуся в том, что очаг заражения насекомыми или клещами обрабатывают некоторым количеством соединения формулы I, эффективным для инактивации насекомых или клещей. Изобретение также относится к способу борьбы с растительными патогенами, заключающемуся в том, что очаг заражения указанными патогенами обрабатывают эффективным количеством соединения формулы I. В данном описании все температуры даются в градусах Цельсия, а все процентные содержания в мас. если это не оговорено особо. Термин "галоген", относится к атому фтора, хлора или брома. Термины "алкокси". "галогеналкил", "алкилсульфинил" и "алкилсульфонил" относятся к группам с прямой и разветвленной цепью. Термины "замещенный фенил", "замещенная феноксигруппа", "замещенная фенилтиогруппа" и "замещенный фенилсульфонил" относятся к таким группам, в которых фенильное кольцо является замещенным одной, двумя или тремя группами, независимо выбранными из галогена, J, (C1-С10)алкила, разветвленного (С3-С6)алкила, галоген(С1-С7)алкила, гидрокси(С1-С7)алкила, (С1-С7)алкокси, галоген(С1-С7) алкокси, фенокси, замещенной фенокси, фенила, замещенного фенила, NO2, OH, CN, (С1-С4)алканоила, бензоила, (С1-С4)алканоилокси, (С1-С4)алкоксикарбонила, феноксикарбонила или бензоилокси. Термины "замещенный нафтил" и "замещенный индолил" относятся к циклическим системам, замещенным одной или несколькими группами, независимо выбранными из галогена, галоген(С1-С4)алкила, СN, NO2, (C1-C4)алкила, разветвленного (С3-С4)алкила, фенила, (С1-С4)алкокси или галоген(С1-С4)алкокси. Термин "карбоциклическое ядро" относится к насыщенному или ненасыщенному углеродному кольцу, содержащему пять или шесть атомов углерода. Термин "ненасыщенная углеводородная цепь" относится к углеводородной цепи, содержащей один или несколько участков ненасыщенности. Термин "ЖХВД" означает жидкостную хроматографию высокого давления. Термин "двухвалентный углеводородный радикал" относится к двухвалентным радикалам, полученным из нормальных алканов путем удаления атомов водорода от каждого из двух концевых атомов углерода цепи, например таким, как метилен, этилен, триметилен, тетраметилен и т.п. Термин "замещенная аминогруппа" относится к аминогруппе, замещенной одной или двумя (С1-С4)алкильными группами или одной (С1-С4)алканоильной группой. Термин "низший алкил" относится к прямым (С1-С6)углеводородным цепям и к разветвленным и циклическим (С3-С6)углеводородным группам. Термины "низший алкенил" и "низший алкинил" относятся к прямым (С2-С6)углеводородным цепям и к разветвленным (С3-С6)углеводородным группам, содержащим по крайней мере одну ненасыщенную связь. Термины "низшие алкокси" и "низшие алкилтио" относятся к О-низшим алкильным и S-низшим алкильным группам. Термин "галогеналкил" относится к низшим алкильным группам, замещенным одним или несколькими атомами галогена. Термин "галогеналкокси" относится к низшим алкоксигруппам, замещенным одним или несколькими атомами галогена. Если это не оговорено особо, то указание на то, что группа может быть замещенной одним или несколькими заместителями, выбранными из определенного класса групп, означает, что эти заместители могут быть независимо выбранными из указанного класса. Предпочтительными соединениями формулы I являются соединения следующих классов: а) соединения формулы I, где Y является -СН2-; b) соединения формулы I, где Z является фенилом; с) соединения формулы I, где Z является замещенной фенильной группой, определенной в параграфе а) в характеризации "арила"; d) соединения формулы I, где Z является фенильной группой, замещенной (С2-С4)алкоксигруппой; е) соединения формул I, где Z является фенильной группой, замещенной разветвленной С3-С7алкоксигруппой; f) соединения формулы I, где Z является фенильной группой, замещенной галогеном(С2-С4)алкоксигруппой; g) соединения формулы I, где Z является фенильной группой, замещенной разветвленной галоген(С3-С7)алкоксигруппой; h) соединения формулы I, где Z является фенильной группой, замещенной феноксигруппой, или замещенной феноксигруппой. i) соединения любой из вышеуказанных групп (c)-(h), где фенильная группа является однозамещенной в 4 положении; j) соединения формулы I, где R1 является (С1-С4)-алкилом, а R2является галогеном; l) соединения формулы I, где R1 является этилом, а R2 является хлором; m) соединения формулы I, где R1 и R2, взятые вместе, образуют R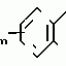 т.е. соединения формулы XII: R т.е. соединения формулы XII: R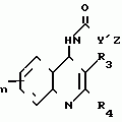 (XII) где Y" и Z определены выше для формулы I, n 1 или 2, R независимо выбирают из галогена, (С1-С4)алкила, разветвленного (С3-С4)алкила, галоген(С1-С4)алкила, (С3-С7)циклоалкила, (С1-С4)алкокси, галоген(С1-С4)алкокси или NO2, a R3 и R4 являются Н; n) соединения, определенные в параграфе (m), где n 0, либо n 1, a R является 8-фторо. о) соединения формулы I, где Z является группой формулы (XII) где Y" и Z определены выше для формулы I, n 1 или 2, R независимо выбирают из галогена, (С1-С4)алкила, разветвленного (С3-С4)алкила, галоген(С1-С4)алкила, (С3-С7)циклоалкила, (С1-С4)алкокси, галоген(С1-С4)алкокси или NO2, a R3 и R4 являются Н; n) соединения, определенные в параграфе (m), где n 0, либо n 1, a R является 8-фторо. о) соединения формулы I, где Z является группой формулы  R21 Соединения предлагаемого изобретения могут быть получены в соответствии с хорошо известными способами химического синтеза. Все необходимые для этого исходные материалы выпускаются промышленностью, либо могут быть получены традиционными методами. Соединения формулы I могут быть получены в соответствии с представленной ниже схемой: R21 Соединения предлагаемого изобретения могут быть получены в соответствии с хорошо известными способами химического синтеза. Все необходимые для этого исходные материалы выпускаются промышленностью, либо могут быть получены традиционными методами. Соединения формулы I могут быть получены в соответствии с представленной ниже схемой: 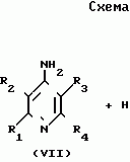 O- O- -Y -Y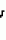 -Z -Z 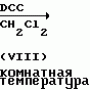 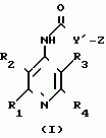 (I) В указанной процедуре, производное кислоты VIII в СН2Сl2 смешивают при комнатной температуре с эквимолярным количеством 4-аминопиридинового производного VII. К полученному раствору добавляют эквимолярное количество 1,3-дициклогексил-карбодиимида. Смесь размешивают около 20 ч, а затем фильтруют. Остаток растворяют в метиленхлориде и снова фильтруют для удаления любой остаточной 1,3-дициклогексилмочевины. Cоединения формулы I могут быть также получены с использованием процедур, проиллюстрированных в схемах 2 и 3. Схема 2 HO- (I) В указанной процедуре, производное кислоты VIII в СН2Сl2 смешивают при комнатной температуре с эквимолярным количеством 4-аминопиридинового производного VII. К полученному раствору добавляют эквимолярное количество 1,3-дициклогексил-карбодиимида. Смесь размешивают около 20 ч, а затем фильтруют. Остаток растворяют в метиленхлориде и снова фильтруют для удаления любой остаточной 1,3-дициклогексилмочевины. Cоединения формулы I могут быть также получены с использованием процедур, проиллюстрированных в схемах 2 и 3. Схема 2 HO-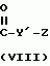 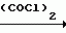  Cl- Cl-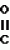 -Y -Y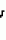 -Z -Z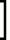 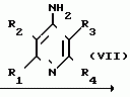 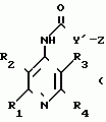 I) В процедуре, проиллюстрированной в схеме 2, слегка избыточное количество оксалилхлорида по капле добавляют к раствору карбоновой кислоты VIII в соответствующем органическом растворителе, таком как ТГФ, метиленхлорид, или ксилол, при комнатной температуре и в присутствии азота. Эта смесь может также включать в себя 1-2 эквивалента пиридина или триэтиламина. После размешивания указанной смеси в течение примерно 30 мин 2 ч по капле добавляют амин в виде раствора в соответствующем органическом растворителе, таком как ТГФ, метиленхлорид, или ксилол. Полученную смесь нагревают при температуре перегонки в течение 8-24 ч, а затем оставляют охлаждаться до комнатной температуры и распределяют между 1 н. гидроксидом натрия и этиловым эфиром. Водную фазу экстрагируюют этиловым эфиром. Объединенные органические фракции промывают водой и насыщенным раствором хлорида натрия, а затем осушают, фильтруют и концентрируют. Схема 3 HO- I) В процедуре, проиллюстрированной в схеме 2, слегка избыточное количество оксалилхлорида по капле добавляют к раствору карбоновой кислоты VIII в соответствующем органическом растворителе, таком как ТГФ, метиленхлорид, или ксилол, при комнатной температуре и в присутствии азота. Эта смесь может также включать в себя 1-2 эквивалента пиридина или триэтиламина. После размешивания указанной смеси в течение примерно 30 мин 2 ч по капле добавляют амин в виде раствора в соответствующем органическом растворителе, таком как ТГФ, метиленхлорид, или ксилол. Полученную смесь нагревают при температуре перегонки в течение 8-24 ч, а затем оставляют охлаждаться до комнатной температуры и распределяют между 1 н. гидроксидом натрия и этиловым эфиром. Водную фазу экстрагируюют этиловым эфиром. Объединенные органические фракции промывают водой и насыщенным раствором хлорида натрия, а затем осушают, фильтруют и концентрируют. Схема 3 HO-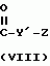 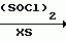  Cl- Cl-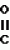 -Y -Y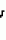 -Z -Z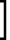 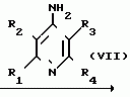 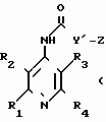 I) В процедуре, проиллюстрированной в схеме 3, производное кислоты VIII нагревают с обратным холодильником в течение I) В процедуре, проиллюстрированной в схеме 3, производное кислоты VIII нагревают с обратным холодильником в течение  2 ч в избыточном количестве тионилхлорида. Затем это избыточное количество тионилхлорида удаляют при пониженном давлении. После этого к полученному остатку добавляют раствор аминопиридина VII и не обязательно около двух эквивалентов триэтиламина в соответствующем органическом растворителе, таком как ацетонитрил, толуол, или ксилол. Полученную смесь нагревают с обратным холодильником в течение 8-24 ч, а затем оставляют для охлаждения до комнатной температуры и распределяют между 1 н. гидроксидом натрия и этиловым эфиром. Водную фазу экстрагируют этиловым эфиром. Объединенные органические фракции промывают водой и насыщенным раствором хлорида натрия, а затем осушают, фильтруют и концентрируют. Соединения формулы VII могут быть получены стандартными способами. Например, получение производных 2-алкил-4-амино-3-бромопиридина и 2-алкил-4- амино-3-хлоропиридина описано в I. Med.Chem. vol. 32, c.1970-77 (1989). В работе I. Prakt. Chem. vol. 331, c.369-374 (1989) описывается бромирование аминопиколинов при получении других нужных исходных материалов. Соединения формулы VII могут быть также получены путем восстановления соответствующих азидов способом, аналогичным описанному в I.Prakt, Chem. vol.327, c.521-522 (1985). Производные карбоновой кислоты формулы VIII, где Z является фенилом или замещенным фенилом, могут быть получены с использованием известных процедур, проиллюстрированных в схеме 4. Производные карбоновой кислоты формулы VIII, где Z является группой формулы 2 ч в избыточном количестве тионилхлорида. Затем это избыточное количество тионилхлорида удаляют при пониженном давлении. После этого к полученному остатку добавляют раствор аминопиридина VII и не обязательно около двух эквивалентов триэтиламина в соответствующем органическом растворителе, таком как ацетонитрил, толуол, или ксилол. Полученную смесь нагревают с обратным холодильником в течение 8-24 ч, а затем оставляют для охлаждения до комнатной температуры и распределяют между 1 н. гидроксидом натрия и этиловым эфиром. Водную фазу экстрагируют этиловым эфиром. Объединенные органические фракции промывают водой и насыщенным раствором хлорида натрия, а затем осушают, фильтруют и концентрируют. Соединения формулы VII могут быть получены стандартными способами. Например, получение производных 2-алкил-4-амино-3-бромопиридина и 2-алкил-4- амино-3-хлоропиридина описано в I. Med.Chem. vol. 32, c.1970-77 (1989). В работе I. Prakt. Chem. vol. 331, c.369-374 (1989) описывается бромирование аминопиколинов при получении других нужных исходных материалов. Соединения формулы VII могут быть также получены путем восстановления соответствующих азидов способом, аналогичным описанному в I.Prakt, Chem. vol.327, c.521-522 (1985). Производные карбоновой кислоты формулы VIII, где Z является фенилом или замещенным фенилом, могут быть получены с использованием известных процедур, проиллюстрированных в схеме 4. Производные карбоновой кислоты формулы VIII, где Z является группой формулы 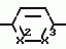 R21 могут быть получены с использованием аналогичной процедуры. Производные карбоновой кислоты формулы VIII, где Z является группой формулы: R21 могут быть получены с использованием аналогичной процедуры. Производные карбоновой кислоты формулы VIII, где Z является группой формулы: 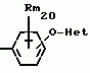 могут быть получены с помощью реакции n-гидроксифенилуксусной кислоты с соответствующим хлорозамещенным гетероциклическим соединением в соответствии с описанием, приведенным ниже. N-оксиды и соли соединений формулы I получают традиционным способом. П р и м е р ы. Представленные ниже табл.1 и 2 идентифицируют соединения формулы I, которые были получены способами, проиллюстрированными в указанных схемах. Подробные примеры получения типичных соединений. П р и м е р 1. N-(4-пиридил)-4-бифенилацетамид (соединение 4) могут быть получены с помощью реакции n-гидроксифенилуксусной кислоты с соответствующим хлорозамещенным гетероциклическим соединением в соответствии с описанием, приведенным ниже. N-оксиды и соли соединений формулы I получают традиционным способом. П р и м е р ы. Представленные ниже табл.1 и 2 идентифицируют соединения формулы I, которые были получены способами, проиллюстрированными в указанных схемах. Подробные примеры получения типичных соединений. П р и м е р 1. N-(4-пиридил)-4-бифенилацетамид (соединение 4) 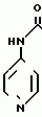 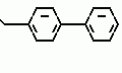 К раствору 0,941 г (10 мм) 4-аминопиридина и 2,123 г 4-бифенилуксусной кислоты в 50 мл метиленхлорида добавляют 2,063 г 1,3-дициклогексилкарбодиимида. После размешивания смеси при комнатной температуре в течение 24 ч смесь фильтровали и концентрировали. Полученный остаток растворяли в метиленхлориде, фильтровали и концентрировали, в результате чего получали 2,997 г хлопьевидного твердого вещества светло-зеленого цвета. Это вещество перекристаллизовывали из смеси гексана и этилацетата, осушали в вакууме, получали 2,138 г светло-зеленого твердого продукта. Выход 74% Т.пл. 145,3оС. П р и м е р 2. N-(3-хлоро-2-этил-4-пиридил) (4-изопропилфенил)ацетамид. (Соединение 23) К раствору 0,941 г (10 мм) 4-аминопиридина и 2,123 г 4-бифенилуксусной кислоты в 50 мл метиленхлорида добавляют 2,063 г 1,3-дициклогексилкарбодиимида. После размешивания смеси при комнатной температуре в течение 24 ч смесь фильтровали и концентрировали. Полученный остаток растворяли в метиленхлориде, фильтровали и концентрировали, в результате чего получали 2,997 г хлопьевидного твердого вещества светло-зеленого цвета. Это вещество перекристаллизовывали из смеси гексана и этилацетата, осушали в вакууме, получали 2,138 г светло-зеленого твердого продукта. Выход 74% Т.пл. 145,3оС. П р и м е р 2. N-(3-хлоро-2-этил-4-пиридил) (4-изопропилфенил)ацетамид. (Соединение 23) 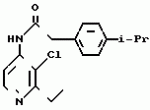 Оксалилхлорид (0,48 мл, 5,50 мМ) добавляли к раствору 4-изопропилфенилуксусной кислоты (0,935 г, 5к,25 мМ) в 20 мл ксилола при комнатной температуре. После размешивания смеси в течение 15 мин добавляли 0,8 мл пиридина. Смесь размешивали еще 30 мин, после чего добавляли 4-амино-3-хлоро-2-этилпиридин (0,783 г, 5,00 мМ). Полученную смесь нагревали до температуры перегонки. После нагревания с обратным холодильником в течение 17 ч смесь оставляли охлаждаться до комнатной температуры, а затем распределяли между 1 н. NaOH (75 мл) и этиловым эфиром (75 мл). Водную фазу экстрагировали этиловым эфиром (75 мл). Объединенные органические фазы промывали водой (1х100 мл) и насыщенным NaCl (1х100 мл), а затем осушали, фильтровали и концентрировали, в результате чего получали 1,71 г маслянистого вещества коричневого цвета. Это маслянистое вещество хроматографировали на силикагеле, элюируя смесью 80% гексана и 20% EtOAc. После выделения основного продукта получали 0,391 г целевого соединения в виде твердого вещества. Т.пл. 90оС. П р и м е р 3. N-(3-хлоро-2-этил-4-пиридил) (4-((-4(трифторометил)-фенил)окси)-фенил)ацетамид (соединение 34) Оксалилхлорид (0,48 мл, 5,50 мМ) добавляли к раствору 4-изопропилфенилуксусной кислоты (0,935 г, 5к,25 мМ) в 20 мл ксилола при комнатной температуре. После размешивания смеси в течение 15 мин добавляли 0,8 мл пиридина. Смесь размешивали еще 30 мин, после чего добавляли 4-амино-3-хлоро-2-этилпиридин (0,783 г, 5,00 мМ). Полученную смесь нагревали до температуры перегонки. После нагревания с обратным холодильником в течение 17 ч смесь оставляли охлаждаться до комнатной температуры, а затем распределяли между 1 н. NaOH (75 мл) и этиловым эфиром (75 мл). Водную фазу экстрагировали этиловым эфиром (75 мл). Объединенные органические фазы промывали водой (1х100 мл) и насыщенным NaCl (1х100 мл), а затем осушали, фильтровали и концентрировали, в результате чего получали 1,71 г маслянистого вещества коричневого цвета. Это маслянистое вещество хроматографировали на силикагеле, элюируя смесью 80% гексана и 20% EtOAc. После выделения основного продукта получали 0,391 г целевого соединения в виде твердого вещества. Т.пл. 90оС. П р и м е р 3. N-(3-хлоро-2-этил-4-пиридил) (4-((-4(трифторометил)-фенил)окси)-фенил)ацетамид (соединение 34) 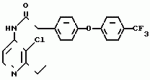 Смесь (4-((-4трифторометил)-фенил)окси)фенил) уксусной кислоты (1,05к г, 3,5 мМ) и 20 мл тионилхлорида нагревали с обратным холодильником. После 2-х часового нагрева с обратным холодильником избыток тионилхлорида удаляли при пониженном давлении. Полученный остаток обрабатывали раствором 4-амино-3-хлоро-2-этил-пиридина и 1 мл триэтиламина в 20 мл ацетонитрила. Смесь нагревали и оставляли при нагреве с обратным холодильником в течение около 24 ч, а затем охлаждали до комнатной температуры и распределяли между 1 н.NaOH (75 мл) и этиловым эфиром (75 мл). Водную фазу экстрагировали этиловым эфиром (75 мл). Объединенные органические фазы промывали водой (1х75 мл), насыщенным NaCl (1х75 мл), а затем осушали, фильтровали и концентрировали, в результате чего получали 1,32 г желтого маслянистого вещества. Это вещество хроматографировали на силикагеле, элюируя смесью 80% гексана и 20% EtOAc. После выделения основного продукта получали 0,202 г целевого соединения в виде твердого вещества. Т.пл. 101,3оС. Препаративный пример 1. 4-азидо-8-фторохинолин. Смесь 2,08 г (0,0114 М) 4-хлоро-8-фторохинолина, 1,12 г (0,0172 М) азида натрия и 4,10 г (0,0127 М) бромида тетрабутиламмония в 70 мл дихлорметана и 25 мл воды нагревали с обратным холодильником в течение ночи. Затем слои отделяли. Органический слой промывали один раз водой, пропускали через фазо-разделяющую бумагу и концентрировали, в результате чего получали маслянистое вещество, которое растирали с эфиром. Полученное твердое вещество фильтровали, фильтрат концентрировали. В результате получали 2,0 г целевого продукта. Препаративный пример 2. 4-амино-8-фторохинолин. К раствору 4-азидо-8-фторохинолина в 12 мл абсолютного этанола при 15-20оС добавляли часть 0,57 г (0,015 М) борогидрида натрия. В результате наблюдалась сильная экзотермическая реакция с энергичным выделением газа. Полученный раствор охлаждали на льду, и в течение 5 мин небольшими порциями добавляли остаток гидрида. После этого ледяную баню удаляли. Примерно через 2 ч смесь выливали в Смесь (4-((-4трифторометил)-фенил)окси)фенил) уксусной кислоты (1,05к г, 3,5 мМ) и 20 мл тионилхлорида нагревали с обратным холодильником. После 2-х часового нагрева с обратным холодильником избыток тионилхлорида удаляли при пониженном давлении. Полученный остаток обрабатывали раствором 4-амино-3-хлоро-2-этил-пиридина и 1 мл триэтиламина в 20 мл ацетонитрила. Смесь нагревали и оставляли при нагреве с обратным холодильником в течение около 24 ч, а затем охлаждали до комнатной температуры и распределяли между 1 н.NaOH (75 мл) и этиловым эфиром (75 мл). Водную фазу экстрагировали этиловым эфиром (75 мл). Объединенные органические фазы промывали водой (1х75 мл), насыщенным NaCl (1х75 мл), а затем осушали, фильтровали и концентрировали, в результате чего получали 1,32 г желтого маслянистого вещества. Это вещество хроматографировали на силикагеле, элюируя смесью 80% гексана и 20% EtOAc. После выделения основного продукта получали 0,202 г целевого соединения в виде твердого вещества. Т.пл. 101,3оС. Препаративный пример 1. 4-азидо-8-фторохинолин. Смесь 2,08 г (0,0114 М) 4-хлоро-8-фторохинолина, 1,12 г (0,0172 М) азида натрия и 4,10 г (0,0127 М) бромида тетрабутиламмония в 70 мл дихлорметана и 25 мл воды нагревали с обратным холодильником в течение ночи. Затем слои отделяли. Органический слой промывали один раз водой, пропускали через фазо-разделяющую бумагу и концентрировали, в результате чего получали маслянистое вещество, которое растирали с эфиром. Полученное твердое вещество фильтровали, фильтрат концентрировали. В результате получали 2,0 г целевого продукта. Препаративный пример 2. 4-амино-8-фторохинолин. К раствору 4-азидо-8-фторохинолина в 12 мл абсолютного этанола при 15-20оС добавляли часть 0,57 г (0,015 М) борогидрида натрия. В результате наблюдалась сильная экзотермическая реакция с энергичным выделением газа. Полученный раствор охлаждали на льду, и в течение 5 мин небольшими порциями добавляли остаток гидрида. После этого ледяную баню удаляли. Примерно через 2 ч смесь выливали в  200 мл ледяной воды.Осадок собирали и осушали воздухом в течение ночи. Выход 1,35 г, т.пл. 184-186оС. П р и м е р 4. N-(8-фторо-4-хинолинил)-(4-хлорофенил)окси)фенил)ацетамид (соединение 59) 200 мл ледяной воды.Осадок собирали и осушали воздухом в течение ночи. Выход 1,35 г, т.пл. 184-186оС. П р и м е р 4. N-(8-фторо-4-хинолинил)-(4-хлорофенил)окси)фенил)ацетамид (соединение 59) 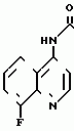 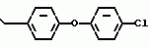 Смесь 0,63 г (0,0024 М) (4-(4-хлорофенил)окси)фенилуксусной кислоты и избыточного количества (10 мл) тионилхлорида нагревали с обратным холодильником в течение 2 ч. Затем избыток тионилхлорида удаляли при пониженном давлении, а остаток растворяли в ксилоле. Добавляли 0,39 г (0,0024 М) 4-амино-8-фторохинолина. Полученную смесь нагревали с обратным холодильником в течение ночи. Затем ксилол удаляли при пониженном давлении, а остаток растворяли в метиленхлориде, после чего полученную смесь один раз промывали водой и один раз 0,1 н. гидроксидом натрия. рН водного слоя доводили до 7, и полученный продукт экстрагировали этилацетатом. Метиленхлоридные и этилацетатные слои объединяли, осушали и концентрировали, в результате чего получали маслянистое вещество. ЯМР показал, что этот продукт представлял собой смесь исходной кислоты и нужного продукта. Указанный продукт растворяли в метиленхлориде, промывали основанием (0,1 н.гидроксидом натрия), осушали и концентрировали, в результате чего получали маслянистое вещество. Это вещество хроматографировали, элюируя градиентом 100% СН2Сl2 ___ Смесь 0,63 г (0,0024 М) (4-(4-хлорофенил)окси)фенилуксусной кислоты и избыточного количества (10 мл) тионилхлорида нагревали с обратным холодильником в течение 2 ч. Затем избыток тионилхлорида удаляли при пониженном давлении, а остаток растворяли в ксилоле. Добавляли 0,39 г (0,0024 М) 4-амино-8-фторохинолина. Полученную смесь нагревали с обратным холодильником в течение ночи. Затем ксилол удаляли при пониженном давлении, а остаток растворяли в метиленхлориде, после чего полученную смесь один раз промывали водой и один раз 0,1 н. гидроксидом натрия. рН водного слоя доводили до 7, и полученный продукт экстрагировали этилацетатом. Метиленхлоридные и этилацетатные слои объединяли, осушали и концентрировали, в результате чего получали маслянистое вещество. ЯМР показал, что этот продукт представлял собой смесь исходной кислоты и нужного продукта. Указанный продукт растворяли в метиленхлориде, промывали основанием (0,1 н.гидроксидом натрия), осушали и концентрировали, в результате чего получали маслянистое вещество. Это вещество хроматографировали, элюируя градиентом 100% СН2Сl2 ___ 10% СН2Сl2/EtOAc с приростом 2%/л, и собирали 0,14 г целевого продукта. Этот продукт смешивали с гексаном и фильтровали, в результате чего получали твердый продукт слегка коричневатого цвета. Выход составил 0,13 г, а т.пл. 169оС. Препаративный пример 3. 4-(3-хлоро-6-пиридазинилокси)фенилуксусная кислота. К смеси 0,54 г (0,013 М, 2,0 экв.) 60% дисперсии гидрида натрия/минерального масла в 10 мл сухого ДМФ по капле при комнатной температуре добавляли раствор 1,02 г (0,0067 М) фенилуксусной кислоты в 2,3 мл ДМФ. Через 15-20 мин образовывалось твердое вещество, которое было трудно размешивать. Затем добавляли пиридазин (1,0 г, 0,0067 М), и полученную смесь нагревали в течение 10% СН2Сl2/EtOAc с приростом 2%/л, и собирали 0,14 г целевого продукта. Этот продукт смешивали с гексаном и фильтровали, в результате чего получали твердый продукт слегка коричневатого цвета. Выход составил 0,13 г, а т.пл. 169оС. Препаративный пример 3. 4-(3-хлоро-6-пиридазинилокси)фенилуксусная кислота. К смеси 0,54 г (0,013 М, 2,0 экв.) 60% дисперсии гидрида натрия/минерального масла в 10 мл сухого ДМФ по капле при комнатной температуре добавляли раствор 1,02 г (0,0067 М) фенилуксусной кислоты в 2,3 мл ДМФ. Через 15-20 мин образовывалось твердое вещество, которое было трудно размешивать. Затем добавляли пиридазин (1,0 г, 0,0067 М), и полученную смесь нагревали в течение  2 ч при 60-65оС, после чего эту смесь оставляли охлаждаться. Затем эту смесь выливали в ледяную воду, и рН доводили до 5 с помощью 2,0 н. НСl, а осадок собирали. Этот продукт растирали с гептаном и получали 880 мг целевого соединения, Т.пл. 124-127оС. Использование в качестве инсектицидов и акарицидов Соединения формулы I обнаруживают активность против ряда насекомых и клещей. В частности, эти соединения обладают активностью против тли хлопковой, которая относится к насекомым отряда Равнокрылых (Homoptera). Другими членами отряда Равнокрылых являются цикадки, дельфациды, медяницы грушевые, медяницы яблонные, щитовки виноградные, белокрылки, пенницы, а также различные другие виды тлей. У указанных соединений наблюдается также активность против трипса оранжерейного, принадлежащего к отряду Трипсов (Thysanoptera). Кроме того, эти соединения обладают активностью против южной капустной совки, которая относится к насекомым отряда Чашуекрылых (Lepidoptera). Другими типичными представителями этого отряда являются плодожорка яблонная, совки, моль платяная, огневка амбарная южная, листовертки, совка хлопковая, мотылек кукурузный, гусеница капустной совки, совка ни, совка хлопковая, мешочница поденкоподобная, коконопряд кольчатый американский, луговые мотыльки и совки травяные. Соединения формулы I могут быть использованы для снижения популяций насекомых и клещей, а также в методах борьбы с популяциями насекомых или клещей, которые заключаются в том, что очаги заражения насекомыми или клещами обрабатывают определенным количеством соединения формулы I, эффективным для инактивации насекомых или клещей. Используемый в настоящем описании термин "очаг заражения насекомыми или клещами" относится к среде, в которой обитают данные насекомые или клещи, или к месту, где имеются их яйца, включая окружающий их воздух, пищу, которой они питаются, или предметы, с которыми они контактируют. Например, для борьбы с насекомыми или клещами, питающимися растениями, активное соединение может быть нанесено на те части растения, которые поедают данные насекомые или клещи, в частности листья. Следует отметить, что указанные соединения могут быть также использованы для защиты текстильных изделий, бумаги, хранящегося зерна или семян путем их обработки активным соединением. Термин "борьба с насекомыми или клещами" означает уменьшение числа живых насекомых или клещей; или снижение числа жизнеспособных яиц насекомых или клещей. Совершенно очевидно, что степень указанного снижения популяции насекомых или клещей зависит от дозы используемого соединения, от природы используемого соединения и от уничтожаемых видов насекомых или клещей. Поэтому, необходимо использовать по крайней мере количество, способствующее инактивации насекомых или клещей. Термины "количество, инактивирующее насекомых" и "количество, инактивирующее клещей" означают количество, достаточное для заметного снижения популяции обрабатываемых насекомых или клещей. В основном это количество составляет 2 ч при 60-65оС, после чего эту смесь оставляли охлаждаться. Затем эту смесь выливали в ледяную воду, и рН доводили до 5 с помощью 2,0 н. НСl, а осадок собирали. Этот продукт растирали с гептаном и получали 880 мг целевого соединения, Т.пл. 124-127оС. Использование в качестве инсектицидов и акарицидов Соединения формулы I обнаруживают активность против ряда насекомых и клещей. В частности, эти соединения обладают активностью против тли хлопковой, которая относится к насекомым отряда Равнокрылых (Homoptera). Другими членами отряда Равнокрылых являются цикадки, дельфациды, медяницы грушевые, медяницы яблонные, щитовки виноградные, белокрылки, пенницы, а также различные другие виды тлей. У указанных соединений наблюдается также активность против трипса оранжерейного, принадлежащего к отряду Трипсов (Thysanoptera). Кроме того, эти соединения обладают активностью против южной капустной совки, которая относится к насекомым отряда Чашуекрылых (Lepidoptera). Другими типичными представителями этого отряда являются плодожорка яблонная, совки, моль платяная, огневка амбарная южная, листовертки, совка хлопковая, мотылек кукурузный, гусеница капустной совки, совка ни, совка хлопковая, мешочница поденкоподобная, коконопряд кольчатый американский, луговые мотыльки и совки травяные. Соединения формулы I могут быть использованы для снижения популяций насекомых и клещей, а также в методах борьбы с популяциями насекомых или клещей, которые заключаются в том, что очаги заражения насекомыми или клещами обрабатывают определенным количеством соединения формулы I, эффективным для инактивации насекомых или клещей. Используемый в настоящем описании термин "очаг заражения насекомыми или клещами" относится к среде, в которой обитают данные насекомые или клещи, или к месту, где имеются их яйца, включая окружающий их воздух, пищу, которой они питаются, или предметы, с которыми они контактируют. Например, для борьбы с насекомыми или клещами, питающимися растениями, активное соединение может быть нанесено на те части растения, которые поедают данные насекомые или клещи, в частности листья. Следует отметить, что указанные соединения могут быть также использованы для защиты текстильных изделий, бумаги, хранящегося зерна или семян путем их обработки активным соединением. Термин "борьба с насекомыми или клещами" означает уменьшение числа живых насекомых или клещей; или снижение числа жизнеспособных яиц насекомых или клещей. Совершенно очевидно, что степень указанного снижения популяции насекомых или клещей зависит от дозы используемого соединения, от природы используемого соединения и от уничтожаемых видов насекомых или клещей. Поэтому, необходимо использовать по крайней мере количество, способствующее инактивации насекомых или клещей. Термины "количество, инактивирующее насекомых" и "количество, инактивирующее клещей" означают количество, достаточное для заметного снижения популяции обрабатываемых насекомых или клещей. В основном это количество составляет 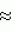 от 1 до 1000 ррm активного соединения. Некоторые из вышеуказанных идентифицированных соединений были проанализированы на инсектицидную, акарицидную и нематицидную активности против восьми видов вредителей. Результаты испытаний представлены в табл. 3, где используются следующие сокращения: ALH цикадка астровая BAW совка малая СА тля хлопковая NEM яванская галловая нематода SCRW южная длинноусая блошка TBW совка TSSM клещик паутинный двупятнистый GECR таракан рыжий пруссак Для проведения оценок инсектицидной активности каждое испытуемое соединение получали в виде 400 ррm-раствора, который затем разводили водой для получения меньших концентраций. Указанный 400 ррm-раствор изготавливали путем смешивания 19,2 мл 0,05%-ного раствора Твина-20 (полиоксиэтилен (20) сорбитанмонолаурата) в воде с 8 мг соединения в 0,8 мл смеси ацетона и EtOH (9/1). Испытания на активность против цикадки астровой (Macrosteles fasсifrons) проводили следующим образом. Тест осуществляли с использованием концентраций 400 ррm и 50 ррm. В пластиковые чашки емкостью 29,5 см3, содержащие ватный тампон, наносили путем распыления с помощью форсунки с плоским факелом распыла 0,4 мл приготовленного материала. Избыток влаги выпаривали. Затем в каждую чашку добавляли 5-10 взрослых цикадок, анестезированных двуокисью углерода. После этого чашки закрывали и держали при комнатной температуре в течение 24 ч. Затем определяли процент погибших насекомых. Активность против совки малой (Spodo-ptera exidna) оценивали следующим образом. Этот тест проводили с использованием концентраций 400 ррm и 50 ррm. Искусственный рацион для чешуекрылых разводили до половинной концентрации 5% -ным непитательным агаром. 8 мл этого рациона распределяли по чашкам емкостью 29,5 см3. За 1 ч до обработки на поверхность с рационом разбрасывали 35-40 яиц. Затем чашки обрабатывали приготовленным составом путем распыления через плоскоструйную форсунку. Обработанные чашки осушали воздухом, а затем герметично закрывали пластмассовыми крышками. Эти чашки выдерживали при комнатной температуре в течение 6 дней. Активность оценивали, исходя из общего числа живых и погибших личинок и размера живых личинок. Активность против тли хлопковой (Aphis gossypii) и клещика паутинного двупятнистого (Tetranychus urticae) оценивали следующим образом. Растения тыквы яйцевидной выращивали до стадии семядоли (околок 6-8 дней). Затем растения заражали тлей хлопковой и двупятнистым паутинным клещиком за 16-24 ч до обработки испытуемым материалом путем переноса нарезанных зараженных листьев из штоковой колонии. Непосредственно перед обработкой испытуемым материалом перенесенную листву удаляли с тыквенных растений. Испытания проводили с использованием концентраций 400 ррm и 50 ррm. Растения обрабатывали испытуемым раствором путем распыления мелкокапельным опрыскивателем при 117,2 кПа. Обе поверхности листьев покрывали раствором до тех пор, пока он не начинал стекать, после чего их оставляли для осушки. Активность каждого соединения определяли через 3 дня после обработки. Активность оценивали как процентное содержание по отношению к количеству клещей/тлей, имеющихся на растениях, опрысканных лишь одним растворителем. Активность против яванской галловой нематоды (Meloidogyne arenaria) оценивали следующим образом. Пять непротравленных семян огурцов помещали на дно прозрачной чашки емкостью 29,5 см3, добавляли 20 г чистого белого песка, и чашки опрыскивали, вращая при этом на подставке, 1,0 мл 400 ррm-раствора, осаждаемого на песок. Затем в каждую чашку вливали 2,5-3,0 мл деионизованной воды, содержащей 300-500 нематод. Эти чашки выдерживали 10-12 дней в камере искусственного климата при температуре 76-85оC и влажности 50-60% Через 10-12 дней чашки оценивали путем их перевертывания и подсчета числа погибших личинок и степени повреждения огуречных растений нематодами. Активность против южной длинноусой блоки (Diabrotica unde cimpuctata howardi) оценивали путем добавления 1 мл испытуемого раствора, содержащего предварительно определенную концентрацию испытуемого соединения, в чашку, содержащую зерна кукурузы в 16 г стерильной почвы. В результате получали почвенную концентрацию 24 ррm. После 1,5-2 ч осушки в отдельные чашки добавляли пять личинок длинноусой блошки на 4 возрастной стадии. Число погибших насекомых определяли через 3-4 дня путем опорожнения чашек на поддон и визуальной оценки почвы на наличие живых блошек. Активность против совки (Heliothis verescens) оценивали следующим образом. Искусственную приманку для чешуекрылых разбавляли до половинной концентрации 5%-ным непитательным агаром. 8 мл этой приманки распределяли по чашкам емкостью 29,5 см3. За 1 ч до обработки на поверхность с приманкой разбрасывали 18-20 яиц. Затем чашки обрабатывали приготовленным составом путем распыления через плоскоструйную форсунку. Испытание проводили с использованием концентраций 400 ррm и 50 ррm. Обработанные чашки осушали воздухом, а затем герметично закрывали пластмассовыми крышками. Эти чашки выдерживали при комнатной температуре в течение 6 дней. Активность оценивали, исходя из общего числа живых и погибших личинок и размера живых личинок. Активность против тараканов-пруссаков (Blattella germanicus) оценивали следующим образом. В чашки емкостью 29,5 см3 вводили 8 мл люцерны в качестве растительного рациона для насекомых. Затем эти чашки обрабатывали приготовленным составом путем распыления через плоскоструйную форсунку. Испытание проводили с использованием концентраций 400 ррm и 50 ррm. Обработанные чашки осушали воздухом в течение 24 ч, а затем в каждую чашку вводили пять пруссаков в конечной третьей или ранней четвертой возрастной стадии. После этого чашки закрывали и в течение 10 дней выдерживали в камере искусственного климата при 76-85оС. Активность оценивали, исходя из общего числа живых и погибших личинок. Использование в качестве нематицидов. Соединения предлагаемого изобретения могут быть использованы для снижения популяций нематод. В соответствии с этим важным аспектом изобретения является способ борьбы с популяциями нематод, заключающийся в том, что очаг заражения нематодами обрабатывают определенным количеством соединения формулы I, эффективным для инактивации нематод. Термин "борьба с нематодами" означает снижение количества живых нематод. Степень снижения популяции нематод с помощью указанного соединения зависит от его дозы, от природы конкретно используемого соединения и от видов уничтожаемых нематод. Поэтому необходимо использовать по крайней мере количество, способствующее инактивации нематод. Термин "нематодо-инактивирующее количество", используемый в настоящем описании, означает количество, достаточное для заметного снижения популяции обрабатываемых нематод. Предлагаемый способ осуществляли в соответствии со стандартной техникой, обычно используемой для работы с нематоцидами. В основном хороший нематоцидный эффект может быть получен при дозах 1,125-11,25 кг/га. Соединение для обработки может быть получено в соответствии с описанием, приведенным ниже. Если нематоциды используются в виде дисперсий, то их обычно вносят как водные составы путем полива почвы вокруг растущих растений или наносят в возрастающем количестве посредством системы орошения. Если нематоциды используются в виде гранул, то они могут быть введены в почву перед посадкой, либо нанесены поверх рассадной грядки, либо нанесены посредством разбрасывания с последующим введением в почву, либо использованы путем межрядовой обработки сельскохозяйственной культуры. Использование в качестве фунгицидов. Соединения предлагаемого изобретения могут быть использованы для борьбы против грибков, в частности против растительных патогенов. Если указанные соединения используются для обработки растений с грибковым заболеванием, то они могут быть нанесены на пораженные растения в фитологически приемлемом количестве, ингибирующем данное заболевание. Термин "фитологически приемлемое количество, ингибирующее заболевание", используемый в настоящем описании, означает количество соединения предлагаемого изобретения, которое способствует устранению или подавлению заболевания растения, причем предпочтительным является устранение данного заболевания при незначительном токсическом воздействии на растение. Это количество обычно составляет от 1 до 1000 ррm, предпочтительно от 10 до 500 ррm. Точная концентрация требуемого соединения зависит от грибкового заболевания, от типа используемого состава для обработки, от способа внесения этого состава, от конкретных видов растений, от климатических условий и т.п. В основном подходящая доза для обработки составляет 0,28-4,5 кг/га. Соединения предлагаемого изобретения могут быть также использованы для защиты зерна, находящегося на хранении, а также других не растительных очагов от заражения грибками. Лабораторные испытания. Описанные ниже эксперименты проводили в лаборатории в целях определения фунгицидной активности соединений предлагаемого изобретения. Испытуемые соединения для обработки получали путем растворения 50 мг соединения в 1,25 мл растворителя. Растворитель получали путем смешивания 50 мл Твина 20 (полиоксиэтилен(20) сорбитанмонолаурата, эмульгатора) с 475 мл ацетона и 475 мл этанола. Раствор растворителя и соединения разводили деионизованной водой до объема 125 мл. Полученный состав содержал 400 ррm испытуемого соединения. Более низкие концентрации получали путем серийного разведения смесью растворителя и поверхностно-активного вещества. Полученные составы испытуемых соединений наносили путем листового опрыскивания. При этом использовались следующие растения и растительные патогены (см. табл. 4). Полученные составы соединений распыляли на все поверхности листьев хозяйских растений (или нарезанные плоды) до тех пор, пока состав не начинал стекать с листьев. Отдельные горшки с каждым растением-хозяином помещали на приподнятые вращающиеся подставки в вытяжном шкафу. Испытуемыми растворами опрыскивали все поверхности листьев. После этого все растения оставляли для осушки, а затем через 2-4 ч инокулировали соответствующими патогенами. В табл. 5 представлена активность типичных соединений предлагаемого изобретения, которая была оценена в описанном выше эксперименте. Оценка активности испытуемых соединений против соответствующих заболеваний растений проводилась по следующей шкале: 0 испытания против данного микроорганизма не проводили; 0-19% уничтожения при 400 ррm; + 20-89% уничтожения при 400 ррm; ++ 90-100% уничтожения при 400 ррm; +++ 90-100% уничтожения при 100 ррm. Композиции. Соединения формулы I используются в виде композиций, которые являются одним из важных вариантов предлагаемого изобретения и которые содержат соединение формулы I и фитологически приемлемый инертный носитель. Эти композиции представляют собой либо концентрированные составы, которые перед их использованием диспергируют в воде, либо порошкообразные или гранулированные препараты, которые применяют без дополнительной обработки. Указанные композиции получают в соответствии со стандартными процедурами и рецептурой, которые обычно используются при изготовлении агрохимикатов, но которые однако являются новыми и ценными из-за наличия в них соединений предлагаемого изобретения. Тем не менее в данном описании будут рассмотрены составы некоторых композиций для того, чтобы облегчить специалистам-агрохимикам получение любой нужной композиции. Дисперсии, в виде которых используются активные соединения, по большей части представляют собой водные суспензии или эмульсии, полученные из концентрированных составов данных соединений. Такие водорастворимые, водосуспендируемые или эмульгируемые составы являются либо твердыми препаратами, обычно такими как смачиваемые порошки, либо жидкими препаратами, такими как эмульгируемые концентраты или водные суспензии. Смачиваемые порошки, которые могут быть спрессованы в вододиспергируемые гранулы, состоят из тщательно размешанной смеси активного соединения, инертного носителя и поверхностно-активных веществ (ПАВ). Концентрация активного соединения обычно составляет от от 1 до 1000 ррm активного соединения. Некоторые из вышеуказанных идентифицированных соединений были проанализированы на инсектицидную, акарицидную и нематицидную активности против восьми видов вредителей. Результаты испытаний представлены в табл. 3, где используются следующие сокращения: ALH цикадка астровая BAW совка малая СА тля хлопковая NEM яванская галловая нематода SCRW южная длинноусая блошка TBW совка TSSM клещик паутинный двупятнистый GECR таракан рыжий пруссак Для проведения оценок инсектицидной активности каждое испытуемое соединение получали в виде 400 ррm-раствора, который затем разводили водой для получения меньших концентраций. Указанный 400 ррm-раствор изготавливали путем смешивания 19,2 мл 0,05%-ного раствора Твина-20 (полиоксиэтилен (20) сорбитанмонолаурата) в воде с 8 мг соединения в 0,8 мл смеси ацетона и EtOH (9/1). Испытания на активность против цикадки астровой (Macrosteles fasсifrons) проводили следующим образом. Тест осуществляли с использованием концентраций 400 ррm и 50 ррm. В пластиковые чашки емкостью 29,5 см3, содержащие ватный тампон, наносили путем распыления с помощью форсунки с плоским факелом распыла 0,4 мл приготовленного материала. Избыток влаги выпаривали. Затем в каждую чашку добавляли 5-10 взрослых цикадок, анестезированных двуокисью углерода. После этого чашки закрывали и держали при комнатной температуре в течение 24 ч. Затем определяли процент погибших насекомых. Активность против совки малой (Spodo-ptera exidna) оценивали следующим образом. Этот тест проводили с использованием концентраций 400 ррm и 50 ррm. Искусственный рацион для чешуекрылых разводили до половинной концентрации 5% -ным непитательным агаром. 8 мл этого рациона распределяли по чашкам емкостью 29,5 см3. За 1 ч до обработки на поверхность с рационом разбрасывали 35-40 яиц. Затем чашки обрабатывали приготовленным составом путем распыления через плоскоструйную форсунку. Обработанные чашки осушали воздухом, а затем герметично закрывали пластмассовыми крышками. Эти чашки выдерживали при комнатной температуре в течение 6 дней. Активность оценивали, исходя из общего числа живых и погибших личинок и размера живых личинок. Активность против тли хлопковой (Aphis gossypii) и клещика паутинного двупятнистого (Tetranychus urticae) оценивали следующим образом. Растения тыквы яйцевидной выращивали до стадии семядоли (околок 6-8 дней). Затем растения заражали тлей хлопковой и двупятнистым паутинным клещиком за 16-24 ч до обработки испытуемым материалом путем переноса нарезанных зараженных листьев из штоковой колонии. Непосредственно перед обработкой испытуемым материалом перенесенную листву удаляли с тыквенных растений. Испытания проводили с использованием концентраций 400 ррm и 50 ррm. Растения обрабатывали испытуемым раствором путем распыления мелкокапельным опрыскивателем при 117,2 кПа. Обе поверхности листьев покрывали раствором до тех пор, пока он не начинал стекать, после чего их оставляли для осушки. Активность каждого соединения определяли через 3 дня после обработки. Активность оценивали как процентное содержание по отношению к количеству клещей/тлей, имеющихся на растениях, опрысканных лишь одним растворителем. Активность против яванской галловой нематоды (Meloidogyne arenaria) оценивали следующим образом. Пять непротравленных семян огурцов помещали на дно прозрачной чашки емкостью 29,5 см3, добавляли 20 г чистого белого песка, и чашки опрыскивали, вращая при этом на подставке, 1,0 мл 400 ррm-раствора, осаждаемого на песок. Затем в каждую чашку вливали 2,5-3,0 мл деионизованной воды, содержащей 300-500 нематод. Эти чашки выдерживали 10-12 дней в камере искусственного климата при температуре 76-85оC и влажности 50-60% Через 10-12 дней чашки оценивали путем их перевертывания и подсчета числа погибших личинок и степени повреждения огуречных растений нематодами. Активность против южной длинноусой блоки (Diabrotica unde cimpuctata howardi) оценивали путем добавления 1 мл испытуемого раствора, содержащего предварительно определенную концентрацию испытуемого соединения, в чашку, содержащую зерна кукурузы в 16 г стерильной почвы. В результате получали почвенную концентрацию 24 ррm. После 1,5-2 ч осушки в отдельные чашки добавляли пять личинок длинноусой блошки на 4 возрастной стадии. Число погибших насекомых определяли через 3-4 дня путем опорожнения чашек на поддон и визуальной оценки почвы на наличие живых блошек. Активность против совки (Heliothis verescens) оценивали следующим образом. Искусственную приманку для чешуекрылых разбавляли до половинной концентрации 5%-ным непитательным агаром. 8 мл этой приманки распределяли по чашкам емкостью 29,5 см3. За 1 ч до обработки на поверхность с приманкой разбрасывали 18-20 яиц. Затем чашки обрабатывали приготовленным составом путем распыления через плоскоструйную форсунку. Испытание проводили с использованием концентраций 400 ррm и 50 ррm. Обработанные чашки осушали воздухом, а затем герметично закрывали пластмассовыми крышками. Эти чашки выдерживали при комнатной температуре в течение 6 дней. Активность оценивали, исходя из общего числа живых и погибших личинок и размера живых личинок. Активность против тараканов-пруссаков (Blattella germanicus) оценивали следующим образом. В чашки емкостью 29,5 см3 вводили 8 мл люцерны в качестве растительного рациона для насекомых. Затем эти чашки обрабатывали приготовленным составом путем распыления через плоскоструйную форсунку. Испытание проводили с использованием концентраций 400 ррm и 50 ррm. Обработанные чашки осушали воздухом в течение 24 ч, а затем в каждую чашку вводили пять пруссаков в конечной третьей или ранней четвертой возрастной стадии. После этого чашки закрывали и в течение 10 дней выдерживали в камере искусственного климата при 76-85оС. Активность оценивали, исходя из общего числа живых и погибших личинок. Использование в качестве нематицидов. Соединения предлагаемого изобретения могут быть использованы для снижения популяций нематод. В соответствии с этим важным аспектом изобретения является способ борьбы с популяциями нематод, заключающийся в том, что очаг заражения нематодами обрабатывают определенным количеством соединения формулы I, эффективным для инактивации нематод. Термин "борьба с нематодами" означает снижение количества живых нематод. Степень снижения популяции нематод с помощью указанного соединения зависит от его дозы, от природы конкретно используемого соединения и от видов уничтожаемых нематод. Поэтому необходимо использовать по крайней мере количество, способствующее инактивации нематод. Термин "нематодо-инактивирующее количество", используемый в настоящем описании, означает количество, достаточное для заметного снижения популяции обрабатываемых нематод. Предлагаемый способ осуществляли в соответствии со стандартной техникой, обычно используемой для работы с нематоцидами. В основном хороший нематоцидный эффект может быть получен при дозах 1,125-11,25 кг/га. Соединение для обработки может быть получено в соответствии с описанием, приведенным ниже. Если нематоциды используются в виде дисперсий, то их обычно вносят как водные составы путем полива почвы вокруг растущих растений или наносят в возрастающем количестве посредством системы орошения. Если нематоциды используются в виде гранул, то они могут быть введены в почву перед посадкой, либо нанесены поверх рассадной грядки, либо нанесены посредством разбрасывания с последующим введением в почву, либо использованы путем межрядовой обработки сельскохозяйственной культуры. Использование в качестве фунгицидов. Соединения предлагаемого изобретения могут быть использованы для борьбы против грибков, в частности против растительных патогенов. Если указанные соединения используются для обработки растений с грибковым заболеванием, то они могут быть нанесены на пораженные растения в фитологически приемлемом количестве, ингибирующем данное заболевание. Термин "фитологически приемлемое количество, ингибирующее заболевание", используемый в настоящем описании, означает количество соединения предлагаемого изобретения, которое способствует устранению или подавлению заболевания растения, причем предпочтительным является устранение данного заболевания при незначительном токсическом воздействии на растение. Это количество обычно составляет от 1 до 1000 ррm, предпочтительно от 10 до 500 ррm. Точная концентрация требуемого соединения зависит от грибкового заболевания, от типа используемого состава для обработки, от способа внесения этого состава, от конкретных видов растений, от климатических условий и т.п. В основном подходящая доза для обработки составляет 0,28-4,5 кг/га. Соединения предлагаемого изобретения могут быть также использованы для защиты зерна, находящегося на хранении, а также других не растительных очагов от заражения грибками. Лабораторные испытания. Описанные ниже эксперименты проводили в лаборатории в целях определения фунгицидной активности соединений предлагаемого изобретения. Испытуемые соединения для обработки получали путем растворения 50 мг соединения в 1,25 мл растворителя. Растворитель получали путем смешивания 50 мл Твина 20 (полиоксиэтилен(20) сорбитанмонолаурата, эмульгатора) с 475 мл ацетона и 475 мл этанола. Раствор растворителя и соединения разводили деионизованной водой до объема 125 мл. Полученный состав содержал 400 ррm испытуемого соединения. Более низкие концентрации получали путем серийного разведения смесью растворителя и поверхностно-активного вещества. Полученные составы испытуемых соединений наносили путем листового опрыскивания. При этом использовались следующие растения и растительные патогены (см. табл. 4). Полученные составы соединений распыляли на все поверхности листьев хозяйских растений (или нарезанные плоды) до тех пор, пока состав не начинал стекать с листьев. Отдельные горшки с каждым растением-хозяином помещали на приподнятые вращающиеся подставки в вытяжном шкафу. Испытуемыми растворами опрыскивали все поверхности листьев. После этого все растения оставляли для осушки, а затем через 2-4 ч инокулировали соответствующими патогенами. В табл. 5 представлена активность типичных соединений предлагаемого изобретения, которая была оценена в описанном выше эксперименте. Оценка активности испытуемых соединений против соответствующих заболеваний растений проводилась по следующей шкале: 0 испытания против данного микроорганизма не проводили; 0-19% уничтожения при 400 ррm; + 20-89% уничтожения при 400 ррm; ++ 90-100% уничтожения при 400 ррm; +++ 90-100% уничтожения при 100 ррm. Композиции. Соединения формулы I используются в виде композиций, которые являются одним из важных вариантов предлагаемого изобретения и которые содержат соединение формулы I и фитологически приемлемый инертный носитель. Эти композиции представляют собой либо концентрированные составы, которые перед их использованием диспергируют в воде, либо порошкообразные или гранулированные препараты, которые применяют без дополнительной обработки. Указанные композиции получают в соответствии со стандартными процедурами и рецептурой, которые обычно используются при изготовлении агрохимикатов, но которые однако являются новыми и ценными из-за наличия в них соединений предлагаемого изобретения. Тем не менее в данном описании будут рассмотрены составы некоторых композиций для того, чтобы облегчить специалистам-агрохимикам получение любой нужной композиции. Дисперсии, в виде которых используются активные соединения, по большей части представляют собой водные суспензии или эмульсии, полученные из концентрированных составов данных соединений. Такие водорастворимые, водосуспендируемые или эмульгируемые составы являются либо твердыми препаратами, обычно такими как смачиваемые порошки, либо жидкими препаратами, такими как эмульгируемые концентраты или водные суспензии. Смачиваемые порошки, которые могут быть спрессованы в вододиспергируемые гранулы, состоят из тщательно размешанной смеси активного соединения, инертного носителя и поверхностно-активных веществ (ПАВ). Концентрация активного соединения обычно составляет от 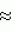 10 до 90 мас. В качестве инертного носителя могут быть использованы аттапульгитовые глины, монтмориллонитовые глины, диатомовая земля или очищенные силикаты. Эффективными ПАВ, составляющими от 10 до 90 мас. В качестве инертного носителя могут быть использованы аттапульгитовые глины, монтмориллонитовые глины, диатомовая земля или очищенные силикаты. Эффективными ПАВ, составляющими от 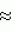 0,5 до 10 мас. смачиваемого порошка, могут быть сульфонированные лигнины, конденсированные нафталинсульфонаты, нафталинсульфонаты, алкилбензолсульфонаты, алкилсульфонаты, неионогенные ПАВ, такие как этиленоксидные аддукты алкилфенолов. Эмульгируемые концентраты включают в себя обычную концентрацию соединения; от 50 до 500 г/л (что эквивалентно от около 0,5 до 10 мас. смачиваемого порошка, могут быть сульфонированные лигнины, конденсированные нафталинсульфонаты, нафталинсульфонаты, алкилбензолсульфонаты, алкилсульфонаты, неионогенные ПАВ, такие как этиленоксидные аддукты алкилфенолов. Эмульгируемые концентраты включают в себя обычную концентрацию соединения; от 50 до 500 г/л (что эквивалентно от около 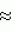 10% до около 50%), растворенного в инертном носителе, который представляет собой либо смешиваемый с водой растворитель, либо смесь не смешиваемого с водой органического растворителя и эмульгаторов. Используемыми органическими растворителями являются ароматические растворители, в частности ксилолы, и нефтяные дистилляты, в частности высококипящие нафталиновые и олефиновые фракции нефти, такие как тяжелый ароматический лигроин. Могут быть также использованы и другие растворители, такие как терпеновые растворители, включая производные канифоли, алифатические кетоны, такие как циклогексанон; и смешанные спирты, такие как 2-этоксиэтанол. Подходящими эмульгаторами для эмульгируемых концентратов являются традиционные неионогенные ПАВ, например такие как ПАВ, описанные выше. Водные суспензии представляют собой суспензии водорастворимых соединений предлагаемого изобретения, диспергированных в водном наполнителе в концентрации 10% до около 50%), растворенного в инертном носителе, который представляет собой либо смешиваемый с водой растворитель, либо смесь не смешиваемого с водой органического растворителя и эмульгаторов. Используемыми органическими растворителями являются ароматические растворители, в частности ксилолы, и нефтяные дистилляты, в частности высококипящие нафталиновые и олефиновые фракции нефти, такие как тяжелый ароматический лигроин. Могут быть также использованы и другие растворители, такие как терпеновые растворители, включая производные канифоли, алифатические кетоны, такие как циклогексанон; и смешанные спирты, такие как 2-этоксиэтанол. Подходящими эмульгаторами для эмульгируемых концентратов являются традиционные неионогенные ПАВ, например такие как ПАВ, описанные выше. Водные суспензии представляют собой суспензии водорастворимых соединений предлагаемого изобретения, диспергированных в водном наполнителе в концентрации  от 5 до 50 мас. Эти суспензии получают путем тонкого измельчения соединения с последующим его тщательным размешиванием с наполнителем, состоящим из воды и ПАВ, выбранных из вышеуказанных типов ПАВ. Для повышения плотности и вязкости водного наполнителя могут быть также добавлены инертные ингредиенты, такие как неорганические соли и синтетические или натуральные камеди. При получении водной смеси часто бывает более эффективно измельчение и смешивание проводить одновременно с использованием таких устройств, как песочная мельница, шаровая мельница или гомогенизатор поршневого типа. Эти соединения могут быть также использованы в виде гранулированных композиций, которые, в частности, предназначены для обработки почвы. В основном гранулированные композиции содержат от 5 до 50 мас. Эти суспензии получают путем тонкого измельчения соединения с последующим его тщательным размешиванием с наполнителем, состоящим из воды и ПАВ, выбранных из вышеуказанных типов ПАВ. Для повышения плотности и вязкости водного наполнителя могут быть также добавлены инертные ингредиенты, такие как неорганические соли и синтетические или натуральные камеди. При получении водной смеси часто бывает более эффективно измельчение и смешивание проводить одновременно с использованием таких устройств, как песочная мельница, шаровая мельница или гомогенизатор поршневого типа. Эти соединения могут быть также использованы в виде гранулированных композиций, которые, в частности, предназначены для обработки почвы. В основном гранулированные композиции содержат  от 0,5 до 10 мас. соединения, диспергированного в инертном носителе, который полностью или по большей части состоит из глины или аналогичного недорогостоящего материала. Указанные композиции обычно получают путем растворения соединения в соответствующем растворителе и введения его в гранулированный носитель, который приготавливают заранее и который имеет соответствующий размер частиц, составляющий в пределах от около 0,5 до 3 мм. Указанные композиции могут быть также получены путем изготовления компаунда или пасты из носителя и соединения с последующими ее измельчением, осушкой и получением гранул с нужным размером частиц. Дусты, содержащие активное соединение, получают путем простого смешивания соединения в форме порошка с соответствующим дустообразным агротехническим носителем, таким как каолиновая глина, измельченная вулканическая порода и т.п. Обычно дусты содержат от 1 до 10% активного соединения. Если необходимо, то с одинаковым успехом может быть использован раствор активного соединения в соответствующем органическом растворителе, обычно легкое минеральное масло, например масло для распыления, которое широко используется в агрохимии. Инсектициды и акарициды в основном используются в виде дисперсии активного ингредиента в жидком носителе. Нужные дозы обработки обычно определяют, исходя из концентрации активного ингредиента в носителе. Наиболее широко используемым носителем является вода. Соединения формулы I могут быть также использованы в виде аэрозольной композиции. Для получения таких композиций активное соединение растворяют или диспергируют в инертном носителе, который представляет собой аэрозольную смесь, создающую повышенное давление. Аэрозольные смеси включают в себя либо низкокипящие углеводороды, которые могут быть смешаны с органическими растворителями, либо водные суспензии с инертными газами или газообразными углеводородами. Затем аэрозольную композицию упаковывают в специальную тару, из которой смесь распрыскивается посредством пульверизатора. Конкретное количество активного соединения, вводимого в очаги заражения насекомыми и клещами, не является критическим параметром и может быть легко определено специалистом на основании вышеприведенных примеров. В общих чертах, хороший эффект можно получить при концентрациях от 10 ррm до 5000 ррm. Причем для большинства соединений достаточно концентраций от 100 до 1500 ррm. Для полевых культур, таких как соя и хлопок, подходящая доза обработки составляет от 0,5 до 10 мас. соединения, диспергированного в инертном носителе, который полностью или по большей части состоит из глины или аналогичного недорогостоящего материала. Указанные композиции обычно получают путем растворения соединения в соответствующем растворителе и введения его в гранулированный носитель, который приготавливают заранее и который имеет соответствующий размер частиц, составляющий в пределах от около 0,5 до 3 мм. Указанные композиции могут быть также получены путем изготовления компаунда или пасты из носителя и соединения с последующими ее измельчением, осушкой и получением гранул с нужным размером частиц. Дусты, содержащие активное соединение, получают путем простого смешивания соединения в форме порошка с соответствующим дустообразным агротехническим носителем, таким как каолиновая глина, измельченная вулканическая порода и т.п. Обычно дусты содержат от 1 до 10% активного соединения. Если необходимо, то с одинаковым успехом может быть использован раствор активного соединения в соответствующем органическом растворителе, обычно легкое минеральное масло, например масло для распыления, которое широко используется в агрохимии. Инсектициды и акарициды в основном используются в виде дисперсии активного ингредиента в жидком носителе. Нужные дозы обработки обычно определяют, исходя из концентрации активного ингредиента в носителе. Наиболее широко используемым носителем является вода. Соединения формулы I могут быть также использованы в виде аэрозольной композиции. Для получения таких композиций активное соединение растворяют или диспергируют в инертном носителе, который представляет собой аэрозольную смесь, создающую повышенное давление. Аэрозольные смеси включают в себя либо низкокипящие углеводороды, которые могут быть смешаны с органическими растворителями, либо водные суспензии с инертными газами или газообразными углеводородами. Затем аэрозольную композицию упаковывают в специальную тару, из которой смесь распрыскивается посредством пульверизатора. Конкретное количество активного соединения, вводимого в очаги заражения насекомыми и клещами, не является критическим параметром и может быть легко определено специалистом на основании вышеприведенных примеров. В общих чертах, хороший эффект можно получить при концентрациях от 10 ррm до 5000 ррm. Причем для большинства соединений достаточно концентраций от 100 до 1500 ррm. Для полевых культур, таких как соя и хлопок, подходящая доза обработки составляет  0,56-1,68 кг/га и обычно наносится в виде 50 гал/акр состава для опрыскивания, содержащего 1200-3600 ррm соединения. Для цитрусовых культур подходящая норма обработки составляет 0,56-1,68 кг/га и обычно наносится в виде 50 гал/акр состава для опрыскивания, содержащего 1200-3600 ррm соединения. Для цитрусовых культур подходящая норма обработки составляет  от 100 до 1500 гал/акр состава для опрыскивания, который содержит 100-1000 ррm соединения. Очагами, обрабатываемыми соединением, могут быть любые места обитания насекомых или клещей, например овощные культуры, фруктовые и ореховые деревья, виноградная лоза и декоративные растения. Поскольку многие виды клещей являются специфичными для каждого конкретного хозяина, то представленный выше перечень отдельных видов клещей дает представление о широком диапазоне возможного применения соединений предлагаемого изобретения. Вследствие специфической способности яиц клещей сохранять устойчивость против токсического действия предпочтительно провести повторные обработки для уничтожения вновь появившихся личинок, это относится также и к другим известным акарицидам. Ниже приводятся конкретные типичные композиции предлагаемого изобретения, которые могут быть использованы на практике, A. 0,75-эмульгируемый концентрат Соединение формулы I 9,38 "Токсимул D" (ТОХIMULD") 2,50 (смесь неионогенного и анионогенного ПАВ) "Токсимул Н" (TOXIMULH) 2,50 (смесь неионогенного и анионогенного ПАВ) "Экзон 200" (ЕХХОN 200) 85,62 (нафталеновый растворитель) В. 1,5-эмульгируемый концентрат Соединение формулы I 18,50 "Токсимул I" 2,50 "Токсимул Н" 2,50 "Экзон 200" 76,50 С. 1,0-эмульгируемый концентрат Соединение формулы I 12,50 N-метилпирролидон 25,00 "Токсимул I" 2,50 "Токсимул Н" 2,50 "Экзон 200" 57,50 D. 1,0-водная суспензия Соединение формулы I 12,00 "Плюроник Р-103" (PLURONIC P-103) 1,50 (блок-сополимер пропилен- оксида и этиленоксида, ПАВ) "Проксель GXI" (PROXEL GXI) 0,05 (биоцид/консервант) "АF-100 0,20 (противовспенивающее средство на основе кремния) "РЕАХ 88В" 1,00 (лигносульфонатное диспергирующее средство) Пропиленгликоль 10,00 Смола veegum 0,75 Ксантановая камедь 0,25 Вода 74,25 Е. 1,0-водная суспензия Соединение формулы I 12,50 "МАКОN10" (10 молей этилен- оксиднонифеноловое ПАВ) 1,00 "ZEOSYL 200" (двуокись кремния) 1,00 "AF-100" 0,20 "AGRIWETFP" (ПАВ) 3,00 2%-ный ксантановый гидрат 10,00 Вода 74,25 Е. 1,0-водная суспензия Соединение формулы I 12,50 "МАКОN 10" 1,50 "ZEOSYL 200" (двуокись кремния) 1,00 "AF-100" 0,20 "POLYFON H" 0,20 (лигносульфонатный диспер- гирующий агент) 2%-ный ксантановый гидрат 10,00 Вода 74,60 G. Смачиваемый порошок. Соединение формулы I 25,80 "POLYFON H" 3,50 "SELLOGEN HR" 5,00 "STEPANOL ME DRY" 1,00 Аравийская камедь 0,50 "HISIL 233" 2,50 Н.Гранулы Соединение формулы I 5,0 Пропиленгликоль 5,0 Еххоn 200 5,0 Гранулированная глина FIorex 30/60 85,0 от 100 до 1500 гал/акр состава для опрыскивания, который содержит 100-1000 ррm соединения. Очагами, обрабатываемыми соединением, могут быть любые места обитания насекомых или клещей, например овощные культуры, фруктовые и ореховые деревья, виноградная лоза и декоративные растения. Поскольку многие виды клещей являются специфичными для каждого конкретного хозяина, то представленный выше перечень отдельных видов клещей дает представление о широком диапазоне возможного применения соединений предлагаемого изобретения. Вследствие специфической способности яиц клещей сохранять устойчивость против токсического действия предпочтительно провести повторные обработки для уничтожения вновь появившихся личинок, это относится также и к другим известным акарицидам. Ниже приводятся конкретные типичные композиции предлагаемого изобретения, которые могут быть использованы на практике, A. 0,75-эмульгируемый концентрат Соединение формулы I 9,38 "Токсимул D" (ТОХIMULD") 2,50 (смесь неионогенного и анионогенного ПАВ) "Токсимул Н" (TOXIMULH) 2,50 (смесь неионогенного и анионогенного ПАВ) "Экзон 200" (ЕХХОN 200) 85,62 (нафталеновый растворитель) В. 1,5-эмульгируемый концентрат Соединение формулы I 18,50 "Токсимул I" 2,50 "Токсимул Н" 2,50 "Экзон 200" 76,50 С. 1,0-эмульгируемый концентрат Соединение формулы I 12,50 N-метилпирролидон 25,00 "Токсимул I" 2,50 "Токсимул Н" 2,50 "Экзон 200" 57,50 D. 1,0-водная суспензия Соединение формулы I 12,00 "Плюроник Р-103" (PLURONIC P-103) 1,50 (блок-сополимер пропилен- оксида и этиленоксида, ПАВ) "Проксель GXI" (PROXEL GXI) 0,05 (биоцид/консервант) "АF-100 0,20 (противовспенивающее средство на основе кремния) "РЕАХ 88В" 1,00 (лигносульфонатное диспергирующее средство) Пропиленгликоль 10,00 Смола veegum 0,75 Ксантановая камедь 0,25 Вода 74,25 Е. 1,0-водная суспензия Соединение формулы I 12,50 "МАКОN10" (10 молей этилен- оксиднонифеноловое ПАВ) 1,00 "ZEOSYL 200" (двуокись кремния) 1,00 "AF-100" 0,20 "AGRIWETFP" (ПАВ) 3,00 2%-ный ксантановый гидрат 10,00 Вода 74,25 Е. 1,0-водная суспензия Соединение формулы I 12,50 "МАКОN 10" 1,50 "ZEOSYL 200" (двуокись кремния) 1,00 "AF-100" 0,20 "POLYFON H" 0,20 (лигносульфонатный диспер- гирующий агент) 2%-ный ксантановый гидрат 10,00 Вода 74,60 G. Смачиваемый порошок. Соединение формулы I 25,80 "POLYFON H" 3,50 "SELLOGEN HR" 5,00 "STEPANOL ME DRY" 1,00 Аравийская камедь 0,50 "HISIL 233" 2,50 Н.Гранулы Соединение формулы I 5,0 Пропиленгликоль 5,0 Еххоn 200 5,0 Гранулированная глина FIorex 30/60 85,0
ФОРМУЛА ИЗОБРЕТЕНИЯN-(4-ПИРИДИЛ- ИЛИ 4-ХИНОЛИНИЛ)АРИЛАЦЕТАМИДНЫЕ ПРОИЗВОДНЫЕ общей формулы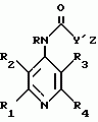 где R - водород; R1, R2, R3 и R4 имеют одно из следующих значений: а) R3 и R4 - водород, а R1 и R2 - независимо галоген, С1 - С4-алкил; б) один из R1, R2, R3 и R4 - С1 - С4-алкил, а остальные - водород; в) R1, R2, R3 и R4 - независимо водород или галоген; или г) R1 и R2, взятые вместе, образуют цепь -СН=СН-СН=СН-, которая может быть замещена атомом фтора, а R3 и R4 - водород; Y где R - водород; R1, R2, R3 и R4 имеют одно из следующих значений: а) R3 и R4 - водород, а R1 и R2 - независимо галоген, С1 - С4-алкил; б) один из R1, R2, R3 и R4 - С1 - С4-алкил, а остальные - водород; в) R1, R2, R3 и R4 - независимо водород или галоген; или г) R1 и R2, взятые вместе, образуют цепь -СН=СН-СН=СН-, которая может быть замещена атомом фтора, а R3 и R4 - водород; Y Z, взятые вместе, образуют неразветвленную или разветвленную С4 - С11 насыщенную углеводородную цепь или Y Z, взятые вместе, образуют неразветвленную или разветвленную С4 - С11 насыщенную углеводородную цепь или Y - группа -СН2-, а Z - фенил, одно- или дизамещенный С1 - С6-алкилом, галогеном, трифторметилом, С1 - С4-алкокси, который может быть замещен атомами фтора, фенилом, феноксигруппой, которая может иметь один или два заместителя, выбранных из С1 - С4-алкокси, галогена, трифторметила, циано, нитро, или группа трифторметилфенилмеркапто, - группа -СН2-, а Z - фенил, одно- или дизамещенный С1 - С6-алкилом, галогеном, трифторметилом, С1 - С4-алкокси, который может быть замещен атомами фтора, фенилом, феноксигруппой, которая может иметь один или два заместителя, выбранных из С1 - С4-алкокси, галогена, трифторметила, циано, нитро, или группа трифторметилфенилмеркапто, 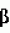 -нафтил или группа -нафтил или группа 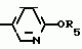 где R5 - фторзамещенный С1 - С4-алкил. где R5 - фторзамещенный С1 - С4-алкил.Популярные патенты: 2437262 Культиватор-плоскорез ... плоскости центральной секции рамы.2. Культиватор-плоскорез по п.1, отличающийся тем, что ограничитель поворота выполнен в виде щек, закрепленных на боковых балках рамы центральной секции, и съемного пальца, проходящего сквозь щеки и контактирующего с поперечной балкой рамы боковой секции при ее подъеме до уровня, параллельного плоскости центральной секции рамы, при этом концы поперечных балок боковых секций рамы, сопрягаемые с центральной секцией, размещены с зазором над рамой центральной секции, кроме того, с рамами боковых секций посредством шарниров с вертикальной осью сопряжены рамки с плоскорезными лапами, поворотные в горизонтальной плоскости.3. Культиватор-плоскорез ... 2153256 Инсектицидное средство и способ борьбы с вредителями сельскохозяйственных культур ... нами предложено средство, состоящее из карбофоса и сульфата железа, ионы которого катализируют процесс окисления в малаоксон. В результате наших исследований выявлен синергизм действия карбофоса 50% к. э. совместно с сульфатом железа в заявляемом соотношении компонентов: повреждение растений при обработке семян предлагаемым средством уменьшается на 2,8-5% по сравнению с повреждением растений при применении только "чистого" карбофоса. Изобретения иллюстрируются следующими примерами. Пример 1. Приготовление составов инсектицидного средства с различными соотношениями компонентов для обработки семян Готовили "базовый" раствор - смесь, состоящую из 9 л 50% к.э. карбофоса и 100 г ... 2218755 Способ длительного клонирования пайзы (echinochloa frumentacea link) ... с зачатками регенерационных побегов, волоски и очаги белых компактных тканей. Участки каллусов с компактными тканями и с зачатками регенерирующих побегов (тип А) переносили на свежие среды 2КС. В результате их переноса и развития на свежих средах формировались каллусы 4 типов (см. таблицу). Следует обратить внимание на то, что при переносе на свежие среды организованных участков каллусов типа Б также формируются каллусы типов А, Б, В, Г. Перенос участков каллусов типов А и Б со среды 2КС на среду MS (без регуляторов роста) приводил к затуханию пролиферации каллусной массы и умножению числа побегов без корней по типу кущения. Стоит отметить, что растения без корневой системы, ... 2167510 Способ и устройство для изготовления круглых тюков соломы или подобного материала с пленочным защитным покрытием ... числа оборотов тюка, например, только 5-8 оборотов, и вращение прекращается, когда каркас 22 достиг своей левой поднятой позиции. Теперь вся внешняя поверхность тюка покрыта пленкой, и пленка 19 подвешена между областью нижнего края задней пластины 24 и входа непосредственно под роликом 10. Таким образом, имеется возможность отрезать пленку где-то в этом положении, так что таким образом необходимый висящий край пленки может быть образован перед началом следующей операции заворачивания. Это может быть сделано с помощью срезающего рычага 28, который имеет движущийся резак 30 для отрезания пленки или, возможно, горячую проволоку для отрезания пленки путем расплавления. В качестве ... 2108695 Орудие для образования гребней в почве ... почве, содержащее стойку с закрепленным на ней делителем-рыхлителем, расположенным над съемным лемехом с режущими кромками и долото, отличающееся тем, что лемех выполнен в виде плоской трапеции с П-образно расположенными режущими кромками и со сквозным со стороны ее малого основания симметрично расположенным между ее боковыми гранями щелевым отверстием с размещенным вдоль него отогнутым от делителя-рыхлителя нижним концевым участком стойки с прикрепленным к ее концу выступающем за пределы контура малого основания трапеции долотом с возможностью плавного перехода отогнутого участка верхней поверхности стойки к верхней поверхности лемеха с обеспечением выполнения общей криволинейности ... |
Еще из этого раздела: 2245017 Способ подготовки картофеля перед закладкой на хранение 2038763 Регулятор вакуума 2462864 Устройство составления экономичного кормового рациона и экономичного кормления животных и птиц 2476277 Способ защиты почв от остатков пестицидов 2250602 Широкозахватный колесный дождеватель 2054235 Лесопосадочная машина 2475020 Способ подбора лучших сортов опылителей для насаждений яблони 2468582 Инсектицидно-фунгицидный состав и способ борьбы с вредителями и болезнями крестоцветных культур 2267924 Способ стимулирования роста растений 2184433 Рабочий орган щелевателя |
Изобретения в сельском хозяйстве
Обработка почвы в сельском и лесном хозяйствах
Посадка, посев, удобрение
Уборка урожая, жатва
Обработка и хранение продуктов полеводства и садоводства
Садоводство, разведение овощей, цветов, риса, фруктов, винограда, лесное хозяйство
Новые виды растений или способы их выращивания
Производство молочных продуктов
Животноводство, разведение и содержание птицы, рыбы, насекомых, рыбоводство, рыболовство
Поимка, отлов или отпугивание животных
Консервирование туш животных, или растений или их частей
Биоцидная, репеллентная, аттрактантная или регулирующая рост растений активность химических соединений или препаратов
Хлебопекарные печи, машины и прочее оборудование для хлебопечения
Машины или оборудование для приготовления или обработки теста
Обработка муки или теста для выпечки, способы выпечки, мучные изделия
|
|
||