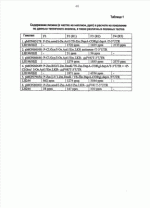
Семена трансгенных растений с повышенным содержанием лизинаПатент на изобретение №: 2460281 Автор: МАЛВАР Томас М. (US), ХУАНГ Шихших (US), ЛЮТИ Михель Х. (US) Патентообладатель: МОНСАНТО ТЕКНОЛОДЖИ ЛЛС (US) Дата публикации: 10 Ноября, 2009 Начало действия патента: 2 Октября, 2006 Адрес для переписки: 129090, Москва, ул. Б.Спасская, 25, стр.3, ООО "Юридическая фирма Городисский и Партнеры", пат.пов. Е.Е.Назиной, рег. 517 Изображения    Изобретение относится к области биохимии. Описано семя трансгенной кукурузы, содержащее более чем 4000 частей на миллион (ppm) свободного лизина, где семя кукурузы содержит нативную ДНК и одну или несколько экзогенных кассет для экспрессии в растениях, содержащих молекулу ДНК, кодирующую дигидродипиколинатсинтазу, устойчивую к ингибированию свободным L-лизином по принципу обратной связи, молекулу ДНК, транскрибируемую с получением молекулы РНК, подавляющей лизинкетоглутаратредуктазу/сахаропиндегидрогеназу, и молекулу ДНК, кодирующую аспартаткиназу, устойчивую к действию лизинопосредованной обратной связи; где молекулы ДНК функционально связаны с одной или несколькими промоторными молекулами таким образом, что происходит транскрипция одной или нескольких молекул РНК в основном в эндосперме кукурузного семени, где, необязательно, семя кукурузы содержит экзогенный ген, придающий устойчивость к гербицидам. Представлен способ получения кукурузной муки, включающий получение указанного семени кукурузы и переработку семени с получением муки. Описана мука, полученная указанным способом. Предложено применение указанного семени для получения муки тонкого или грубого помола, корма для животных, получения белкового концентрата или изолята и употребления указанного семени человеком или животным. Изобретение позволяет получить богатые лизином пищевые продукты, не требующие дополнительного добавления лизина. 7 н. и 4 з.п. ф-лы, 2 табл., 8 ил., 2 пр. Испрашиваемый приоритет По настоящей заявке испрашивается приоритет предварительной заявки США с серийным номером 60/723178, поданной 3 октября 2005 г. и полностью включенной в настоящее описание посредством ссылки. Предшествующий уровень техники 1. Область техники, к которой относится изобретение В настоящем описании раскрыты ДНК-конструкции, пригодные для получения трансгенных растений с частями, имеющими повышенное содержание лизина, а также способы использования таких ДНК-конструкций для получения трансгенных растений и семян, собранных с растений материалов, а также муки и пищевых продуктов, получаемых из вышеперечисленного сырья. Такие ДНК-конструкции пригодны для получения трансгенных растений повышенной пищевой ценности, обусловленной повышением накопления лизина в семенах. Также раскрыты полинуклеотидные молекулы и способы, пригодные для получения трансгенных растений с повышенным содержанием лизина в семенах. 2. Описание уровня техники Zea mays, обычно называемая маисом или кукурузой, представляет собой зерновую культуру, широко используемую в качестве пищи для человека и животного корма. Зерно, в настоящем описании называемое также семенами, является источником белка, крахмала и масла для многих низших животных, в том числе для свиней, мясного и молочного скота, рыбы и домашней птицы. В некоторых странах, таких как Мексика, более 70% собранной кукурузы потребляется людьми и кукуруза и получаемые из нее продукты, такие как мамалыга и плоские маисовые лепешки, являются пищевыми продуктами массового потребления. Основная часть аминокислотного состава зерна определяется количеством и типом аминокислот, содержащихся в полипептидах. Только относительно небольшая часть, до 10%, доступных аминокислот в зерне находится в виде свободных аминокислот; остальные содержатся в различных белках. Большинство полипептидов кукурузы, находящихся в зерне, являются запасными белками семян, или зеинами. Эти запасные белки семян синтезируются в ходе развития зерна и используются в качестве источника энергии в ходе прорастания и роста последнего. Однако эти запасные белки семян содержат мало лизина либо вообще не содержат этой аминокислоты. Из десяти аминокислот, которые считаются незаменимыми в смешанных зерновых кормах (аргинин, гистидин, изолейцин, лейцин, лизин, метионин или цистеин, фенилаланин или тирозин, треонин, триптофан и валин), не только лизин, но также треонин и метионин практически отсутствуют в кукурузном зерне. Нехватка этих незаменимых аминокислот, в особенности лизина, требует добавления этих питательных веществ к пищевому кукурузному зерну, что часто достигается путем дополнительного введения соевой муки или синтетического лизина. Увеличение содержания лизина в семенах кукурузы с целью повышения питательной ценности последних в качестве пищи или кормового зерна может быть полезным в данной области техники. Дополнительное преимущество может быть реализовано в том случае, если к зерну нужно будет добавлять лишь малые количества лизина либо не добавлять его вообще. В отношении питания человека имеет место плохая тенденция к употреблению пищи, относительно богатой недорогими крахмалосодержащими продуктами и относительно бедной высококачественным белком. Квашиоркор (детская пеллагра) - форма нарушения питания, вызванная потреблением белков неадекватного качества при общей высокой энергетической ценности (общей калорийности) потребляемой пищи. Ранние симптомы являются очень общими и включают усталость, раздражительность и сонливость. При продолжительном дефиците белка наблюдается отставание в росте, потеря мышечной массы, генерализированный отек (эдема) и снижение иммунитета. Обычным является вздутие живота. Часто наблюдаются кожные проявления (такие, как дерматит, изменение пигментации, истончение волос и витилиго). Смерти предшествуют шок и кома. Согласно одной из правительственных оценок не менее 50% пожилых людей в домах престарелых США страдают от нарушения питания, связанного с низким уровнем белковой калорийности пищи. Таким образом, продукты, полученные из кукурузы с улучшенным в силу повышенного содержания лизина качеством белкового состава, могли бы значительно улучшить не только питательную ценность пищевых продуктов, но и общий уровень здоровья. Молекулярно-биологический подход к повышению содержания лизина включает идентификацию и введение в кукурузу генов с целью оказания воздействия на содержание лизина в зерне, не сопровождающегося отрицательным воздействием на агрономические свойства. Лизин продуцируется из аспартата, метаболизм которого, в свою очередь, взаимно связан с биохимическими путями, в которых участвуют треонин, метионин и изолейцин. Сам лизин служит конечным продуктом, модифицирующим и регулирующим ферменты, принимающие участие в его собственном биосинтезе. Ключевыми ферментами, принимающими участие в метаболизме лизина, являются аспартаткиназа (AK) и дигидродипиколинатсинтаза (DHDPS), в то время как лизинкетоглутаратредуктаза (LKR, бифункциональный фермент, также известный как сахаропиндегидрогеназа, SDH), по-видимому, играет ключевую роль в катаболизме лизина. AK и DHDPS формируют петлю обратной связи, регулируемую лизином; по мере повышения содержания лизина он подавляет активность этих ферментов. Таким образом, для повышения содержания лизина предпочтительно оперировать с вариантами AK или DHDPS, нечувствительными к обратной связи. Были описаны нечувствительные к лизину варианты бактериального, а также растительного генов AK (см. Falco с соавторами, патент США В публикациях Falcо с соавторами (патенты США Настоящее изобретение относится к ДНК-конструкциям, которые, будучи экспрессированными в растительных клетках, обеспечивают повышение питательной ценности растений, в частности повышенное содержание лизина в семенах растения. Краткое описание сущности изобретения Настоящее изобретение относится к ДНК-конструкциям, которые при функционировании в геноме трансгенного растения обеспечивают повышение содержания лизина в семени растения. Собранные семена с высоким содержанием лизина могут быть полезны для производства пищевой и кормовой продукции, такой как кукурузная мука (в том числе мука, известная как «маса харина»), кукурузная мука и мучные изделия, в которые нужно добавлять лишь небольшие количества лизина либо не нужно добавлять его вообще. Предпочтительно трансгенное растение и семя представляет собой растение и зерно сельскохозяйственных культур, предпочтительно - однодольное растение и семя и наиболее предпочтительно - семя и растение кукурузы. Настоящее изобретение относится к содержащим ДНК-конструкции трансгенным растениям и семенам с повышенным содержанием лизина в семени. ДНК-конструкции по настоящему изобретению включают молекулу, которая, будучи экспрессированной в клетках кукурузы, ингибирует продукцию лизиндеградирующего полипептида, а также молекулу, которая, будучи экспрессированной в клетках кукурузы, обеспечивает продукцию нечувствительных к лизину полипептида дигидродипиколинатсинтазы и аспартаткиназы. Даже в том случае, если собранное зерно является нежизнеспособным и, таким образом, не может быть использовано в качестве семян, оно тем не менее содержит повышенное содержание лизина и характеризуется повышенным качеством белка согласно настоящему изобретению. Подобное собранное зерно может быть переработано тем же образом, что и обычное зерно. Соответственно, в другом воплощении настоящее изобретение относится к корму для животных с повышенным содержанием лизина, получаемому путем выращивания трансгенного растения по настоящему изобретению и сбора семян с повышенным содержанием лизина или путем переработки по настоящему изобретению либо их части. В другом воплощении настоящее изобретение относится к муке или мучным изделиям, получаемым путем выращивания трансгенного растения по настоящему изобретению и сбора семян с повышенным содержанием лизина или путем переработки семян по настоящему изобретению либо их части. В одном из воплощений настоящего изобретения ДНК-конструкция включает новые полинуклеотидные композиции, усовершенствованные для экспрессии в растительных клетках, особенно в клетках кукурузы. Один из новых полинуклеотидов (SEQ ID NO:5) кодирует полипептид дигидродипиколинатсинтазы, другой новый полинуклеотид (SEQ ID NO:9) является гомологичным и комплементарным части полинуклеотидной последовательности, кодирующей лизинкетоглутаратредуктазу. Экспрессия этой ДНК-конструкции в растительной клетке, особенно в клетке кукурузы, предпочтительно в клетке кукурузного семени, приводит к повышению содержания лизина в кукурузном семени. ДНК-конструкция включает полинуклеотиды, например такую последовательность, как SEQ ID NO:1, кодирующую нечувствительную к лизину дигидродипиколинатсинтазу, а также такую последовательность, как SEQ ID NO:2, кодирующую лизинкетоглутаратредуктазу и используемую в качестве матрицы для конструирования ингибиторных молекул РНК, либо такую последовательность, как SEQ ID NO:3, кодирующую аспартаткиназу. ДНК-конструкция предпочтительно содержит молекулу промотора, усовершенствованную для управления транскрипцией функционально связанного полинуклеотида в семени кукурузы. Помимо этого ДНК-конструкция может содержать новую молекулу ДНК (SEQ ID NO:10), содержащую молекулу для подавления гена, мишенью которой является ген лизинкетоглутаратредуктазы, где молекула, подавляющая ген, помещена в интрон ДНК-конструкции. В другом воплощении настоящее изобретение относится к способу получения кукурузного семени с повышенным содержанием лизина посредством скрещивания инбредных родительских растений с последующим получением гибридных семян, при котором каждое из родительских растений содержит в своем геноме одну или несколько ДНК-конструкций, составляющих предмет настоящего изобретения, в составе кассет для экспрессии в растениях, причем в каждом из родительских растений экспрессионные кассеты различны и ни одно из родительских растений не содержит всех трех; а также последующим сбором семян, имеющих содержание лизина выше, чем в каждом из родительских растений. В другом воплощении настоящее изобретение относится к способу получения продуктов питания человека или кормовых продуктов для животных, содержащих повышенное содержание лизина, включающему стадию переработки семян или их части, полученных из трансгенных растений, геном которых содержит экзогенную ДНК-конструкцию или набор конструкций согласно настоящему изобретению. Помимо этого настоящее изобретение относится к способу получения продуктов питания человека или кормовых продуктов для животных, имеющих повышенное содержание лизина, включающему стадию выращивания трансгенного растения с последующим получением семян, геном которых содержит экзогенную ДНК-конструкцию по настоящему изобретению, с последующим сбором семян. Краткое описание графического материала Фиг.1. Карта плазмиды pMON66649. Фиг.2. Карта плазмиды pMON80003. Фиг.3. Карта плазмиды pMON79465. Фиг.4. Карта плазмиды pMON93092. Фиг.5. Карта плазмиды pMON93093. Фиг.6. Карта плазмиды pMON80378. Фиг.7. Содержание свободного лизина в зернах, полученных из объектов, содержащих pMON93092. Фиг.8. Содержание свободного лизина в зернах, полученных из объектов, содержащих pMON93093. Подробное описание изобретения Трансгенное растение или семя, проявляющее желаемое свойство, например повышенное содержание лизина по изобретению, содержит специфическую экзогенную ДНК, встроенную в геном трансгенного растения и обуславливающую наличие желаемого свойства. Данное свойство может быть выражено как измеряемое изменение природного свойства контрольного растения, например растения или семени практически того же генотипа, лишенного специфической экзогенной ДНК. Предпочтительно изменение оценивается путем сопоставления количественного выражения данного свойства в трансгенном растении или семени, имеющем специфическую экзогенную ДНК, и количественного выражения того же свойства в контрольном растении или семени. Таким образом «маис с повышенным содержанием лизина» представляет собой растение кукурузы (маиса) с повышенным содержанием лизина в любой части растения, предпочтительно в семенах, которые в настоящем описании также могут быть названы зерном (в том числе и в агрегированной форме). Настоящее изобретение относится к ДНК-конструкциям и семенам, содержащим в своем геноме по крайней мере одну из ДНК-конструкций в составе кассет, экспрессии в растениях по настоящему изобретению, а также характеризующимся повышенным содержанием лизина по сравнению с семенами, не содержащими конструкции. Повышенное содержание лизина может проявляться растением путем накопления повышенных количеств данной аминокислоты в зерне и может быть измерено при помощи любого подходящего способа, такого как масс-спектрофотометрия или высокоэффективная жидкостная хроматография подходящим образом полученного тканевого экстракта. Трансгенное кукурузное зерно с повышенным содержанием лизина по настоящему изобретению особенно полезно в качестве пищевого продукта или корма, а также муки или мучных изделий, в качестве сырья для получения очищенных кукурузных белковых продуктов либо в качестве сырья для получения других продуктов, получаемых из зерна, содержащего повышенное содержание лизина по сравнению с нетрансгенным зерном подобного сорта. Общее содержание лизина в кукурузном зерне, составляющее примерно 4000 частей на миллион (ppm), является достаточным для того, чтобы в получаемые из этого зерна пищевые продукты или корма не нужно было добавлять лизин из дополнительных источников. Продукция и накопление лизина в кукурузе с повышенным содержанием этой аминокислоты по настоящему изобретению достигает вышеуказанного уровня. Настоящее изобретение относится к способам и композициям, значительно улучшенным по сравнению с ранее описанными способами и композициями для повышения содержания лизина в кукурузном зерне (см., например, патент США Способы повышения содержания аминокислот в трансгенных растениях включают экспрессию рекомбинантных молекул ДНК, кодирующих белки, вовлеченные в пути синтеза аминокислот, на более высоком уровне по сравнению с экспрессией нативных генов. Одним из способов повышения содержания лизина в кукурузе является экспрессия бактериальной дигидродипиколинатсинтазы (DHDPS) согласно раскрытому в патентах США Любое из растений или их частей по настоящему изобретению может быть переработано для получения корма, муки тонкого и грубого помола, белковых продуктов или масла. Особенно предпочтительной для этих целей частью растений является семя. В одном из предпочтительных воплощений настоящего изобретения корм, мука тонкого и грубого помола, белковые продукты или масло используются для кормления сельскохозяйственных животных (скота). Способы получения корма, муки тонкого и грубого помола, белковых продуктов или масла известны в данной области техники, см., например, патенты США В другом воплощении мука по настоящему изобретению может быть смешана с другими мучными продуктами. В предпочтительном воплощении настоящего изобретения мука, полученная из растений или семян по настоящему изобретению либо при помощи способа по настоящему изобретению составляет более чем примерно 0,5%, примерно 1%, примерно 5%, примерно 10%, примерно 25%, примерно 50%, примерно 75% или примерно 95% по объему или массе мучного компонента любого продукта. В другом воплощении настоящего изобретения мучной продукт может быть смешан и составлять более примерно 10%, более примерно 25%, более примерно 35%, более примерно 50% или более примерно 75% от смеси по объему. Настоящее изобретение также относится к способу усиления интенсивности роста человека или низшего животного, включающему употребление человеком или низшим животным пищи, по крайней мере часть которой представляет собой кукурузу с высоким содержанием лизина, содержащую одну или несколько кассет, для экспрессии в растениях по настоящему изобретению. В настоящем описании термин «низшие животные» относится к птицам, рыбам, а также млекопитающим. Рекомбинантные ДНК-конструкции Настоящее изобретение относится к ДНК-конструкциям, содержащим функционально связанные полинуклеотиды, способные обеспечить повышенное содержание лизина в зернах кукурузы. Термин «ДНК-конструкция» включает без ограничения полинуклеотидные молекулы, которые управляют транскрипцией связанных полинуклеотидных молекул в клетке растения. По меньшей мере часть ДНК-конструкции по настоящему изобретению может использоваться в способе трансформации растительной клетки, что подразумевает стабильное встраивание этой части ДНК-конструкции в геном данной клетки. Эта часть обуславливает наличие фенотипа, характеризующегося высоким содержанием лизина в зернах кукурузы или мучных продуктах, изготовленных из таких зерен, и является аспектом настоящего изобретения. ДНК-конструкции pMON93092 и pMON09093 были депонированы Monsanto Technology LLC согласно Будапештскому соглашению в Американской коллекции типовых культур (АТСС) под номерами доступа PTA-6733 и PTA-6734 соответственно. Данные депозиты составляют часть раскрытия настоящего изобретения, и, хотя последовательности, приведенные в настоящем письменном раскрытии, по мнению авторов, являются точными, при необходимости полинуклеотидные последовательности молекул ДНК, содержащие регуляторные элементы, кодирующие и некодирующие молекулы, могут быть определены при помощи этих депозитов и использованы для коррекции последовательностей, раскрытых в настоящем изобретении. Полинуклеотидные молекулы связаны в рекомбинантных ДНК-конструкциях при помощи способов, известных специалистам в данной области. Примером пригодной технологии создания ДНК-конструкций может служить технология клонирования GATEWAY Используемый в настоящем описании термин «экзогенная ДНК или выделенная ДНК» относится к молекуле ДНК, которая в норме не присутствует в геноме клетки-хозяина, или же к ДНК, которая в норме не присутствует в геноме клетки-хозяина в идентичном контексте, или же к двум связанным прилегающим друг к другу последовательностям, которые в норме или в природе не связаны друг с другом. Экзогенная ДНК может включать полинуклеотидную молекулу ДНК или РНК, которая является нативной для генома клетки-хозяина, или же может содержать нативный полинуклеотид, измененный путем присоединения или делеции одного или нескольких полинуклеотидов или же путем модификаций регуляторных элементов ассоциированного полинуклеотида или другой полинуклеотидной последовательности согласно описанному в настоящем описании. В дополнение к регуляторным элементам экзогенная ДНК может содержать кодирующую последовательность, продуктом которой является белок или полипептид, или же некодирующую последовательность, продуктом которой является небелковый продукт, такой как, например, молекула РНК, оказывающая влияние на транскрипцию или трансляцию другой последовательности ДНК. ДНК-конструкция по настоящему изобретению содержит кодирующую и некодирующую последовательности. Используемые для трансформации растительных клеток экзогенные ДНК-конструкции содержат представляющую интерес кодирующую последовательность, а также обычно другие регуляторные элементы согласно описанному в настоящем описании, такие как (без ограничения) промоторы, интроны, 5'- и 3'-нетранслируемые области, лидерные последовательности, последовательности сигналов локализации и транзитных сигналов, а также энхансеры, функциональное соединение которых обуславливает экспрессию РНК в клетках растений. Подобные ДНК-конструкции в контексте настоящего изобретения называются кассетами для гетерологичной экспрессии в растениях. ДНК-конструкции, перечисленные в таблице 1, иллюстрируют связи регуляторных элементов в экспрессионных кассетах, которые экспрессируют кодирующие и некодирующие последовательности; помимо этого также указан средний уровень лизина в трансгенных семенах маиса, содержащих каждую конструкцию. Примерами молекул промоторов ДНК экзогенной ДНК-конструкции по настоящему изобретению могут служить промоторы, усиливаемые в семени или семяспецифические промоторы, включающие, например, промоторы, используемые в однодольных сельскохозяйственных культурах, такие как кукурузный L3-промотор (промотор, описанный в патенте США Используемый в настоящем описании термин «ген» или «кодирующая последовательность» относится к молекуле ДНК, с которой транскрибируется молекула РНК. Молекула ДНК содержит область (CR-), кодирующую мРНК, которая, в свою очередь, кодирует белковый продукт, либо РНК, которая функционирует как молекула, подавляющая ген, либо структурные молекулы РНК, такие как тРНК, рРНК, snРНК либо другие молекулы РНК. Используемый в настоящем описании термин «экспрессия» относится к комбинации внутриклеточных процессов, включающих транскрипцию и трансляцию, при помощи которых молекула ДНК, такая как ген, продуцирует полипептид или молекулу РНК. Примером кодирующей последовательности является ген дигидродипиколинатсинтазы Corynebacterium (DHDPS; Bonnassie с соавторами, 1990; Richaud с соавторами, 1986), пригодный для получения кукурузных зерен с повышенным содержанием лизина. Кукурузное растение, трансформированное таким образом, что оно содержит и экспрессирует ген DHDPS Corynebacterium или любой другой ген, экспрессия которого приводит к повышению содержания лизина в ткани зерна, в контексте настоящего изобретения также называется кукурузным растением с повышенным содержанием лизина. Кодирующая область гена DHDPS Corynebacterium согласно настоящему изобретению дополнительно модифицируется для повышения экспрессии в растительных клетках, предпочтительно в клетках однодольных растений и наиболее предпочтительно в клетках кукурузы. Модифицированная кодирующая область гена DHDPS Corynebacterium, используемая в контексте настоящего изобретения, соответствует последовательности SEQ ID NO:5, обозначаемой в настоящем описании как CORgl.dapA.nno. Используемый в настоящем описании термин «промотор» относится к области последовательности ДНК, инициирующей транскрипцию РНК с ДНК. Промоторы расположены с 5'-конца смысловой цепи транскрибируемой молекулы ДНК и содержат области, служащие в качестве сайтов связывания для РНК-полимеразы, а также области, вовлеченные во взаимодействия с другими факторами, индуцирующими транскрипцию РНК. Более конкретно, базальные промоторы растений содержат канонические области, ассоциированные с инициацией транскрипции, такие как CAAT- и TATA-боксы. В контексте настоящего изобретения предпочтительные молекулы промоторов и 5'-нетранслируемые молекулы индуцируют транскрипцию в клетках семян или тканей на более высоком уровне, чем в других клетках или тканях растения. Молекулы промоторов могут быть выбраны из числа молекул, известных в данной области, например из промоторов, описанных в патенте США Помимо промотора ДНК-конструкции, используемые для трансформации растений, обычно также содержат другие регуляторные элементы, такие как, без ограничения, 3'-нетранслируемые области (содержащие сайты полиаденилирования), транзитные или сигнальные пептиды для направления белка в определенные клеточные органеллы растений, в частности в хлоропласты, лейкопласты и другие пластидные органеллы. Специалистам в данной области известны различные интроны, энхансеры, транзитные пептиды, нацеливающие сигнальные последовательности. 5'- и 3'-нетранслируемые области (UTR), полезные для конструирования эффективных векторов для экспрессии в растениях, подобных раскрытым, например, в публикации патентной заявки США 5'-UTR, функционирующий как трансляционная лидерная последовательность, представляет собой генетический ДНК-элемент, локализованный между промоторной и кодирующей последовательностями гена. Трансляционная лидерная последовательность присутствует в полностью процессированной мРНК с 5'-конца от последовательности начала трансляции. Трансляционная лидерная последовательность может оказывать влияние на процессинг первичного транскрипта в мРНК либо на стабильность мРНК или эффективность трансляции. Примеры трансляционных лидерных последовательностей включают лидерные последовательности генов белков теплового шока кукурузы и петуньи (патент США 3'-нетранслируемая область (3' UTR) или 3'-область полиаденилирования представляет собой молекулу ДНК, связанную со структурной полинуклеотидной молекулой и локализованную с 3'-конца от последней, и содержит полинуклеотиды, содержащие сигнал полиаденилирования и другие регуляторные сигналы, влияющие на транскрипцию, процессинг мРНК или экспрессию генов. Функция сигнала полиаденилирования в растениях состоит в запуске полиаденилирования, т.е. добавления полиаденилатнуклеотида к 3'-концу предшественника мРНК. Последовательность полиаденилирования может быть получена из природного гена, из множества растительных генов либо из Т-ДНК генов агробактерий. Примерами 3'-UTR могут служить 3'-область нопалинсинтазы (nos 3'; Fraley с соавторами, 1983), 3'-UTR-последовательности гена hsp17 пшеницы (T-Ta.Hsp17) и T-Ps.RbcS2:E9 (малая субъединица рибулозабисфосфаткарбоксилазы/оксигеназы (rubisco) гороха), 3'-UTR-последовательности, раскрытые в патенте Под термином «транзитные сигналы» в целом понимают пептидные молекулы, которые, будучи связанными с представляющим интерес белком, направляют последний в ту или иную ткань, клетку, внутриклеточный компартмент или клеточную органеллу. Примеры подобных пептидов включают без ограничения хлоропласт-транзитные пептиды, сигналы ядерной локализации и вакуолярные сигналы. В контексте настоящего изобретения особо применимыми являются пластид-транзитные пептиды, направляющие экспрессию фермента DHDPS в пластиды клеток семян. Хлоропласт-транзитный пептид (CTP) может быть получен в виде химерной конструкции, в которой CTP слит с N-концом белка, предназначенного для транспорта в хлоропласты. Множество белков, локализованных в хлоропластах, экспрессируются ядерными генами в виде предшественников и далее направляются в хлоропласты за счет CTP, удаляемого в ходе процессов, связанных с импортом белка в хлоропласты. Примеры хлоропластных белков включают малую субъединицу (RbcS2) рибулоза-1,5-бисфосфат-карбоксилаза, ферредоксин, ферредоксин-оксидоредуктаза, белки 1 и 2 светособирающего комплекса и тиоредоксин F. Было продемонстрировано, как in vivo, так и in vitro, что нехлоропластные белки могут быть перенаправлены в хлоропласты путем использования химерных CTP-слитых белков, а также что наличие CTP является достаточным условием для направления белка в хлоропласты. Было показано, что встраивание подходящего хлоропласт-транзитного пептида, такого как CTP генов EPSPS Arabidopsis thaliana (Klee с соавторами, 1987) и Petunia hybridа (della-Cioppa с соавторами, 1986), приводит к направлению гетерологичных белков в хлоропласты трансгенных растений. CTP гена DapA Zea mays (SEQ ID NO:6, в настоящем описании обозначаемая как TS-Zm.DapA) согласно настоящему изобретению может быть применен для направления связанного с ним полипептида DHDPS в пластиды семян. Специалистам в данной области будет понятно, что могут быть получены различные химерные конструкции, в которых используется функциональность специфического CTP для импорта гетерологичного полипептида DHDPS в пластиды растительной клетки. Описание использования хлоропласт-транзитных пептидов приведено в патенте США В таблице 1 приведены комбинации промоторов и других регуляторных элементов, функционально связанных с молекулами, подавляющими ген LKR, и с кодирующими молекулами DHDPS, а также соответствующие эффекты в отношении содержания лизина в растениях и зернах кукурузы. Специалисту в данной области будет ясно, что экзогенные молекулы ДНК со сходными свойствами могут быть заменены молекулами, перечисленными в таблице 1, и протестированы при помощи способов, описанных в настоящем описании, а также других сходных способов, пригодных для определения уровня лизина в растительных тканях, зернах, а также полученной из них продукции. ДНК-конструкции по настоящему изобретению могут необязательно содержать селектируемую или количественно оцениваемую маркерную молекулу. Особо важными являются селектируемые маркерные молекулы, которые также придают растениям ценное агрономическое свойство, например устойчивость к гербицидам. Гербициды, устойчивость к которым была продемонстрирована для трансгенных растений и к которым могут быть применены способы по настоящему изобретению, включают, без ограничения, глифосат, глюфосинат, сульфонилмочевины, имидазолиноны, бромоксинил, далапон, циклогександион, ингибиторы протопорфириногеноксидазы, а также изоксафлютоловые гербициды. Полинуклеотидные молекулы, кодирующие белки, вовлеченные в контроль устойчивости к гербицидам, хорошо известны в данной области и включают, без ограничения, полинуклеотидные молекулы, кодирующие 5-енолпирувилшикимат-3-фосфатсинтазу (EPSPS, патенты США Устойчивость к гербицидам является желательным фенотипом для сельскохозяйственных культур. ДНК-конструкции по настоящему изобретению предпочтительно содержат экспрессионную кассету, наличие которой предоставляет трансформированному кукурузному растению устойчивость к глифосату. Также экспрессионная кассета позволяет проводить селекцию трансформированных клеток кукурузы в глифосатсодержащей среде. Экспрессионная кассета предпочтительно содержит промотор, активирующий транскрипцию гена, кодирующего устойчивую к глифосату EPSPS, во всех клетках трансформированного растения. В частности, экспрессионная кассета, обуславливающая наличие устойчивости к глифосату, содержит промотор и интрон рисового актина 1 (P-Os.Act1, I-Os.Act1, патент США В ходе трансформации экзогенная ДНК может быть встроена в геном растения произвольно, т.е. не сайт-специфично. В некоторых случаях может быть полезным направить встраивание экзогенной ДНК в определенный сайт, т.е. провести сайт-специфичную интеграцию, например заменить существующую последовательность гена или геномной области. В некоторых других случаях может быть полезным направить встраивание экзогенной ДНК в определенный сайт, про который известно, что в нем имеет место экспрессия гена(ов). Существует несколько сайт-специфичных рекомбинационных систем, функционирующих в растениях, в том числе Cre/lox-система, раскрытая в патенте США Полезные маркерные селектируемые гены представляют собой гены, обеспечивающие устойчивость к антибиотикам, таким как ампициллин, канамицин (nptII), гигромицин B (aph IV) и гентамицин (aac 3 и aacС4), либо селектируемые маркерные гены, описанные в патентах США Подавление генов ДНК-конструкция по настоящему изобретению обеспечивает экспрессию антисмысловой молекулы РНК, подавляющей эндогенный ген LKR (лизинкетоглутаратредуктаза (LKR, бифункциональный растительный фермент, также известный как сахаропиндегидрогеназа SDH) в трансгенной растительной клетке. Подобная ДНК-конструкция содержит промотор, активный в ткани, в которой планируется подавить действие целевого фермента, а также транскрибируемую последовательность ДНК-элемента, комплементарную полинуклеотидной последовательности гена LKR, экспрессию которого планируется подавить. Целевой генный элемент, последовательность которого «копируется» для использования в качестве транскрибируемой ДНК в конструкции для подавления экспрессии гена, может представлять собой промоторный элемент, интронный элемент, экзонный элемент либо 5'- или 3'-UTR-элемент. Хотя минимальная длина фрагмента ДНК, «копированного» с последовательности гена, экспрессию которого планируется подавить, составляет примерно 21 или 23 нуклеотида, предпочтительными являются более длинные сегменты, например, вплоть до полноразмерной последовательности целевого гена. ДНК-элемент может содержать несколько фрагментов гена, например нуклеотиды, комплементарные непрерывным или отдельным генным элементам, соответствующим UTR, экзону и интрону. Подобные конструкции могут также содержать в соответствии с необходимостью другие регуляторные элементы, ДНК-фрагменты, кодирующие транзитные пептиды, сигнальные пептиды, селекционные и скрининговые маркеры. Для получения антисмысловым образом ориентированной РНК-петли длина комплементарного ДНК-элемента условно составляет не более половины длины антисмысловым образом ориентированного ДНК-элемента, часто не более одной трети от длины антисмысловым образом ориентированного ДНК-элемента, например не более одной четверти от длины вышеупомянутого антисмысловым образом ориентированного ДНК-элемента. Общая длина комбинации ДНК-элементов может варьироваться. Например, длина антисмысловым образом ориентированного ДНК-элемента может составлять от 500 до 5000 нуклеотидов, а длина комплементарного ДНК-элемента может составлять от 50 до 500 нуклеотидов. Дизайн антисмысловой транскрипционной единицы может быть проведен таким образом, чтобы подавлять экспрессию множества генов или членов генного семейства, при этом ДНК содержит два или более антисмысловым образом ориентированных элементов, полученных из различных генов, например комплементарных по меньшей мере части 5'-антисмыслового элемента. Подавление экспрессии включает в себя хорошо известные способы подавления транскрипции гена или накопления соответствующей этому гену мРНК, препятствующих трансляции транскрипта в белок. Посттрансляционное подавление экспрессии опосредуется транскрипцией интегрированной рекомбинантной ДНК с последующим формированием двуцепочечной РНК (дцРНК), гомологичной гену, экспрессию которого планируется подавить. Образование дцРНК обычно происходит в результате транскрипции интегрированного инвертированного повтора целевого гена и является обычным событием при использовании способов подавления экспрессии, известных как антисмысловое подавление, косупрессия или РНК-интерференция (RNAi). Транскрипционное подавление может быть опосредовано транскрибируемой дцРНК, гомологичной промоторной последовательности ДНК - эффект, называемый транс -супрессией промотора. Более конкретно, посттрансляционное подавление экспрессии гена, достигаемое путем встраивания рекомбинантной ДНК-конструкции, содержащей антисмысловым образом ориентированный ДНК-фрагмент, для регуляции экспрессии гена в клетках растений, раскрыто в патентах США Функционирование гена также может быть нарушено при помощи подавления экспрессии, достигаемого за счет инсерционных мутаций, создаваемых мобильными генетическими элементами. Например, многие двудольные растения могут быть легко трансформированы агробактериальной Т-ДНК, в результате чего может быть быстро получено большое число трансформированных растений. Помимо этого существуют линии некоторых видов, таких как Zea mays, содержащих активные мобильные генетические элементы, которые могут быть эффективно использованы для генерирования большого числа инсерционных мутаций, хотя другие виды лишены подобных возможностей. Мутантные растения с нарушенной экспрессией интересующего полипептида, полученные при помощи агробактериальной трансформации или мутагенеза, опосредованного мобильными генетическими элементами, могут быть идентифицированы при помощи полинуклеотидов, составляющих предмет настоящего изобретения. Например, многочисленная популяция мутантных растений может быть проскринирована при помощи полинуклеотидов, кодирующих интересующий полипептид, для идентификации мутантных растений со встроенным геном, кодирующим интересующий полипептид. Белковые молекулы Белки, составляющие предмет настоящего изобретения, представляют собой полноразмерные белки либо по меньшей мере фрагменты полноразмерных белков, достаточные для реализации релевантной биологической активности полноразмерного белка, например повышения содержания лизина в трансгенном кукурузном зерне. Термин «белок» также включает в себя молекулы, состоящие из одной или более полипептидных цепей. Таким образом, полезный белок в контексте настоящего изобретения может представлять собой продукт полноразмерного гена либо один или более функциональных фрагментов естественного белка, предоставляющих желаемое агрономическое свойство согласно настоящему изобретению, т.е. повышенное содержание лизина. Гомологи белков, составляющих предмет настоящего изобретения, могут быть идентифицированы при помощи сопоставления аминокислотных последовательностей белков DHDPS (SEQ ID NO:7) или аспартаткиназы (SEQ ID NO:8) с аминокислотными последовательностями белков тех же или других растительных или бактериальных организмов, например, вручную либо при помощи известных поисковых алгоритмов, основанных на поиске гомологии, таких как BLAST, FASTA и алгоритм Smith-Waterman. В другом аспекте настоящее изобретение относится к последовательностям, кодирующим функциональные гомологичные белки, отличающиеся от белков DHDPS и аспартаткиназы согласно настоящему изобретению на одну или более аминокислот; возникновение подобных белков является результатом хорошо известных консервативных аминокислотных замен, например замена на валин является консервативной для аланина, а треонин - консервативной заменой для серина. При экспрессии подобных гомологичных белков в трансгенном растении они будут оказывать эффекты, практически эквивалентные таковым, оказываемым белками DHDPS или аспартаткиназы. Консервативные замены для той или иной аминокислоты в нативной последовательности белка могут быть выбраны из других членов класса, к которому принадлежит данная природная аминокислота. Типичные аминокислоты, принадлежащие к различным классам, включают в себя без ограничения (1) кислые (отрицательно заряженные) аминокислоты, такие как аспарагиновая кислота и глутаминовая кислота; (2) основные (положительно заряженные) аминокислоты, такие как аргинин, гистидин и лизин; (3) нейтральные полярные аминокислоты, такие как глицин, серин, треонин, цистеин, тирозин, аспарагин и глутамин; и (4) нейтральные неполярные (гидрофобные) аминокислоты, такие как аланин, лейцин, изолейцин, валин, пролин, фенилаланин, триптофан и метионин. Консервативные замены для той или иной аминокислоты в нативной последовательности белка могут быть выбраны из других членов группы, к которой принадлежит данная природная аминокислота. Например, группа аминокислот с алифатическими боковыми цепями включает в себя глицин, аланин, валин, лейцин и изолейцин; группа аминокислот с боковыми гидроксилсодержащими алифатическими цепями включает в себя серин и треонин; группа аминокислот с амидосодержащими боковыми цепями включает в себя аспарагин и глутамин; группа аминокислот с ароматическими боковыми цепями включает в себя фенилаланин, тирозин и триптофан; группа аминокислот с основными боковыми цепями включает в себя лизин, аргинин и гистидин; и группа аминокислот с серосодержащими боковыми цепями включает в себя цистеин и метионин. Группами, в которых происходят природные консервативные аминокислотные замены, являются аминокислотные пары валин-лейцин, валин-изолейцин, фенилаланин-тирозин, лизин-аргинин, аланин-валин, аспарагиновая кислота-глутаминовая кислота и аспарагин-глутамин. В другом аспекте настоящее изобретение относится к белкам, отличающимся от описанных белковых последовательностей DHDPS и аспартаткиназы на одну или более аминокислот; возникновение подобных белков является результатом инсерции или делеции одной или более аминокислот в нативной последовательности. При экспрессии подобных гомологичных белков в трансгенном растении они будут оказывать эффекты практически эквивалентным образом, например обеспечивать повышение содержание лизина в кукурузном зерне. Белки, составляющие предмет настоящего изобретения и являющиеся вариантами белков, к которым относится настоящее изобретение, в общем случае демонстрируют значительную степень идентичности с последними, такую как по меньшей мере 50% и более, например по меньшей мере 60% или 70% идентичности с белками DHDPS и аспартаткиназы. Полезные белки также включают в себя белки, демонстрирующие еще большую идентичность с аминокислотами белковых сегментов белков DHDPS и аспартаткиназы, например, 80%, 90%, 95%, 98% или до 99% идентичности. Способы трансформации и трансформированные растения В контексте настоящего изобретения термин «кукуруза» относится к Zea mays, также известному как кукуруза, и включает в себя все виды растений, которые могут быть скрещены с кукурузой, включая дикие сорта кукурузы. В практических воплощениях настоящего изобретения способы и композиции для трансформации растений посредством встраивания экзогенной ДНК в геном растения могут включать в себя любой из хорошо известных и продемонстрированных способов. Предпочтительными способами трансформации растений являются бомбардировка микрочастицами, описанная в патентах США Используемый в настоящем описании термин «трансгенный» организм относится к организму, геном которого содержит экзогенную ДНК или изолированную ДНК. Трансгенным организмом может быть растение, животное, насекомое, гриб, бактерия или вирус. Используемый в настоящем описании термин «трансгенное растение» относится к стабильно трансформированному растению или полученному от него потомству любого поколения, в котором ДНК растения и его потомства содержит экзогенную ДНК. Помимо этого трансгенное растение может содержать также последовательности, нативные для трансформированного растения, в которые была встроена экзогенная ДНК для изменения уровня и паттерна экспрессии гена. Используемый в настоящем описании термин «стабильно» трансформированное растение относится к растению, в котором экзогенная ДНК наследуется. Экзогенная ДНК может наследоваться в качестве фрагмента ДНК, присутствующего в клетке растения, при этом не встроенного в геном хозяина. Стабильно трансформированное растение предпочтительно содержит экзогенную ДНК, встроенную в хромосомную ДНК в ядре, митохондриях или хлоропластах, более предпочтительно - встроенную в ядерную хромосомную ДНК. Используемый в настоящем описании термин «трансгенное растение R 0» относится к растению, которое было трансформировано экзогенной ДНК или получено из клетки, каллюса или кластера клеток, которые были трансформированы экзогенной ДНК. Используемый в настоящем описании термин «потомство» относится к последующему поколению, включая семена и полученные из них растения, которые произошли от конкретного родительского растения или нескольких родительских растений; это потомство может быть высоковырожденным или в значительной степени гомозиготным в зависимости от сорта. Потомство трансгенного растения настоящего изобретения может быть, например, оплодотворено путем самоопыления, скрещено с другим трансгенным растением, скрещено с нетрансгенным растением и/или подвергнуто обратному скрещиванию с родительским растением. Семена растений, составляющие предмет настоящего изобретения, могут быть собраны с плодородных трансгенных растений и могут быть использованы для выведения поколений потомства растений, составляющих предмет настоящего изобретения, включая гибридные линии растений, содержащие в геноме экзогенную ДНК-конструкцию согласно приведенному в таблице 1 настоящего описания, которая обеспечивает трансгенные продукты преимуществом, заключающимся в повышении содержания лизина в кукурузном зерне и опциональном повышении устойчивости к глифосатным гербицидам. Трансгенный «продукт» получают путем трансформации растительной клетки экзогенной ДНК-конструкции, последующей регенерации растения, полученной в ходе специфического встраивания экзогенной ДНК в растительный геном и селекции растения, характеризуемого наличием трансгенной ДНК. Каждый продукт является уникальным индивидом, каждый из которых отличается от других продуктов специфической локализацией геномной вставки экзогенной ДНК-конструкции, составляющей предмет настоящего изобретения. Детектирование трансгенной ДНК осуществляется при помощи любого числа способов обнаружения ДНК, известных специалистам в данной области техники, которые могут быть выполнены с использованием растительных тканей, семян и обработанных трансгенных продуктов, содержащих трансгенную ДНК. Обычно трансформируют несколько растительных клеток, каждая из которых потенциально представляет собой продукт интеграции, отличный от других продуктов, что приводит к получению популяции растений, из которой далее выбирается то или иное конкретное растение. Вследствие того, что локус интеграции в большинстве случаев является стабильным на протяжении повторяющихся репродуктивных циклов растений, термин «продукт» относится к первоначальному трансформанту R0 и его потомству, которые содержат экзогенную ДНК, встроенную в специфический и уникальный сайт в геноме, т.е. трансгенную ДНК. Потомство, полученное в результате полового ауткроссинга, самооплодотворения или повторного обратного скрещивания, при проведении которых хотя бы одно из используемых в скрещивании растений является потомком трансформанта R 0 любого поколения и содержит ту же трансгенную ДНК. В ходе процессинга семян и зерен, составляющих предмет настоящего изобретения, для получения корма и продуктов питания нормальные структуры тканей растения уничтожаются, клетки растения разрушаются и нативная ДНК и экзогенные экспрессионные кассеты растений могут не остаться полностью интактными, в особенности при обработке с использованием высоких температур, экстрагирующих растворителей и им подобных. Несмотря на это уникальные процессированные продукты, полученные в ходе практических воплощений настоящего изобретения, могут быть легко идентифицированы как содержащие нативную ДНК и фрагменты экзогенных кассет, предназначенных для экспрессии в растениях. Под «фрагментами» подразумеваются изолируемые или амплифицируемые сегменты ДНК длиной по меньшей мере 20 пар оснований. Такие фрагменты могут быть секвенированы или картированы при помощи рестрикционного анализа для подтверждения идентичности их последовательностей нативной ДНК или экзогенными экспрессионными кассетами исходного материала. ПРИМЕРЫ Нижеследующие примеры приведены для демонстрации примеров конкретных предпочтительных воплощений настоящего изобретения. Специалистам в данной области техники будет понятно, что технологии, раскрытые в нижеследующих примерах, представляют собой подходы, которые, по данным авторов настоящего изобретения, хорошо работают в контексте практических реализаций настоящего изобретения и таким образом могут служить примерами предпочтительных практических воплощений настоящего изобретения. Тем не менее, в свете настоящего раскрытия специалисты в данной области техники должны понимать, что раскрытые специфические воплощения могут быть подвергнуты множеству изменений и тем не менее приводить к сходным результатам без выхода за рамки сущности и объема настоящего изобретения. Пример 1 ДНК-конструкции и трансформирование растений ДНК-конструкции, составляющие предмет настоящего изобретения, содержат регуляторные молекулы, функционально связанные с интересующей ДНК. В частности, ДНК-конструкция содержит промотор, интрон, 5'-лидерную последовательность, кодирующую или некодирующую молекулу и 3'-нетранслируемую область. ДНК-конструкция, составляющая предмет настоящего изобретения, была получена с использованием различных молекулярных способов и инструментов, например, описанных Sambrook с соавторами; в значительной степени схожие конструкции могут быть получены при помощи вариантов данных способов, известных специалистам в области манипуляций с ДНК. Такие методы, как ПЦР-амплификация, клонирование и субклонирование использовались для функционального связывания промоторов, лидерных последовательностей, интронов, транзитных пептидов, кодирующих молекул, некодирующих молекул и 3'-нетранслируемых областей, приведенных в таблице 1 в функциональных конфигурациях и далее проиллюстрированных на фиг.1-6. ДНК-конструкции были клонированы в один или более плазмидных «скелетов», пригодных для использования в агробактериальной трансформации клеток кукурузы, хотя могут быть выбраны и другие плазмидные «скелеты», например высококопийные плазмиды, для изоляции ДНК-фрагментов и трансформации с использованием микрочастиц либо плазмиды, совместимые с другими бактериальными хозяевами. Для тестирования комбинаций стратегий экспрессии нечувствительного к действию лизинопосредованной петли обратной связи полипептида DHDPS (SEQ ID NO:7) и репрессии катаболизма лизина посредством подавления экспрессии эндогенного гена LKR/SDH кукурузы (SEQ ID NO:2) или экспрессии гена аспартаткиназы (SEQ ID NO:8) были получены 35 конструкций, приведенных в таблице 1. Эти стратегии включают в себя, например: 1) экспрессию дцРНК гена LKR в зародыше; 2) экспрессию полипептида DHDPS и дцРНК гена LKR в зародыше; 3) экспрессию полипептида DHDPS и дцРНК гена LKR в эндосперме; 4) экспрессию полипептида DHDPS в эндосперме и дцРНК гена LKR в зародыше; 5) экспрессию полипептида DHDPS и аспартаткиназы, а также экспрессию дцРНК гена LKR. Получение трансгенных растений Ткани кукурузы (инбредные линии LH198 или LH244), содержащие незрелые зародыши или каллюс, для трансформации изолировали, после чего ДНК-конструкцию, составляющую предмет настоящего изобретения, встраивали в геном кукурузы при помощи агробактерий (см., например, патенты США Пример 2 Определение содержания лизина в тканях и семенах кукурузы Различные способы являются полезными для определения содержания лизина в тканях растений, их зернах и процессированных продуктах, например, в настоящем изобретении для анализа содержания свободного лизина (в частях на миллион, ppm) в зернах кукурузы, соответствующих различным трансгенным продуктам, идентифицированным как трансформированные при помощи ДНК-конструкции, описанной в таблице 1, использовалась жидкостная хромотография-масс-спектрофотометрия/масс-спектрофотометрия (LC-MS-MS); результаты данного анализа приведены в таблицах 1 и 2. Пробы индивидуальных зрелых кукурузных зерен, соответствующих каждому из трансгенных продуктов, сначала взвешивали, затем перемалывали в тонкий гомогенный порошок, который далее экстрагировали при помощи растворителя, состоящего из метанола, воды и муравьиной кислоты. В случае «bulked»-зерна использовали примерно 30 мг измельченного порошка. Для выделения лизина из экстракта применяли жидкостную хроматографию и масс-спектрометрию с мониторингом множественных реакций (MRM). После отделения количество лизина вычисляли по площади масс-спектрометрического пика относительно калибровочной кривой, которая была получена с использованием дейтерированного d4-лизина в качестве внутреннего стандарта (IS). В другом случае определение содержания лизина в зернах кукурузы было основано на определении свободных аминокислот при помощи высокоэффективной жидкостной хроматографии (HPLC). Отдельные зерна или зерновые пулы каждого из трансгенных продуктов перемалывали в тонкий гомогенный порошок согласно ранее описанному и в данном случае для анализа использовали примерно 30 мг данного порошка. Экстракцию аминокислот проводили при помощи 5% трихлоруксусной кислоты, определение аминокислот проводили при помощи предколоночной первичной аминной дериватизации с использованием о-фталальдегида (OPA). При проведении хроматографии с обращенной фазой разделение происходит благодаря гидрофобности R-групп каждой из аминокислот. Для стабилизации флуорофора добавляется тиол, такой как 2-меркаптоэтанол (SHCH2CH2OH) или 3-меркаптопропионовая кислота (SHCH2CH2 COOH). Уровень свободного лизина (в частях на миллион, ppm) в трансгенных продуктах, полученных в ходе трансформации каждой из конструкций, были усреднены и обобщены в таблице 1. Также приведены поколения (F1, F2, F3 и F4) проанализированных зерен. Результаты измерения содержания свободного лизина в зернах поколения R1 трансгенных кукурузных продуктов, содержащих pMON80378, приведены в таблице 2. Содержание лизина было неожиданно высоким в проанализированных продуктах 5 и 6. Содержание лизина может быть далее отрегулировано путем скрещивания кукурузных продуктов, содержащих различные комбинации кассет, предназначенных для экспрессии в растениях и описанных в таблице 1, таких, что гибридное зерно, полученное от скрещивания родительских растений, содержащих одну или более экспрессионных кассет, будет содержать желаемое количество лизина. Инбредное родительское растение, содержащее, например, экспрессионные кассеты CordapA и lysC E.coli (дикий тип или Ec.lysC.mut, SEQ ID NO:11, молекула ДНК, кодирующая белок, модифицированный в четырех позициях - S2A, C58G, T352I и A401G), может быть скрещено с другим родительским растением, содержащим экспрессионную кассету дцРНК LKR, в результате чего получаемое зерновое потомство содержит большее количество лизина, нежели суммарное содержание лизина в обоих родительских растениях. Родительское растение, содержащее другие комбинации, такие как, например, комбинация CordapA и дцРНК LKR, может быть скрещено с другим родительским растением, содержащим LysC, или же родительское растение, содержащее LysC и дцРНК LKR, может быть скрещено с другим родительским растением, содержащим CordapA, для получения неожиданно высокого содержания лизина в гибридных зернах. Содержание свободного лизина в зернах трансгенных продуктов, содержащих pMON93092, также было измерено при помощи тандемной масс-спектрофотометрии (LC-MS-MS) в измельченных и экстрагированных пробах, примерно по 20 зерен в каждой лунке. Содержание свободного лизина в частях на миллион (ppm) в зернах поколения R2 из ряда трансформированных продуктов продемонстрировано на фиг.7 и 8. Как показано для продуктов, содержащих pMON93092, содержание свободного лизина составляло примерно 3500-5500 ppm, тогда как для продуктов, содержащих pMON93093, содержание свободного лизина составляло примерно 1700-6500 ppm. В большинстве случаев были проведены независимые измерения в двух или более лунках, соответствующих одному и тому же продукту; на фигурах также продемонстрированы значения стандартного отклонения. Для сравнения, содержание лизина в кукурузе дикого типа составляет от 50 до 100 ppm. Раскрытые выше и процитированные в формуле изобретения плазмиды pMON93092 и pMON93093 были депонированы Monsanto Technology LLC по Будапештскому соглашению с Американской коллекцией типовых культур (ATCC), 10801 University Boulevard, Manassas, Va. 20110. Номера ATCC - PTA-6733 и PTA-6734 соответственно. Депозит будет храниться в депозитарии в течение 30 лет, либо в течение 5 лет после последнего запроса, либо в течение срока эффективного использования патента - в зависимости от того, какой срок окажется дольше, и будет при необходимости заменен в течение этого периода. Все публикации, патенты и патентные заявки включены в настоящее описание посредством ссылки в той же степени, как если бы каждая отдельная публикация или патентная заявка была специально и индивидуально включена посредством ссылки. ССЫЛКИ Ссылки, приведенные ниже, включены в настоящее описание посредством ссылки в такой степени, чтобы дополнить, объяснить, раскрыть основу или описать методологию, технологию и/или композиции, использованные в контексте настоящего изобретения. Патент США Патентная заявка США Патентная заявка США с серийным Bonnassie с соавторами, Nucleic Acids Res., 18: 6421, 1990. DeBlock с соавторами, EMBO J., 6: 2513-2519, 1987. della-Cioppa с соавторами, Proc. Natl. Acad. Sci. USA, 83: 6873-6877, 1986. Fraley с соавторами, Proc. Natl. Acad. Sci. USA, 80: 4803-4807, 1983. Klee с соавторами, Mol. Gen. Genet, 210: 437-442, 1987. Misawa с соавторами, Plant J., 4: 833-840, 1993. Misawa с соавторами, Plant J., 6: 481-489, 1994. Padgette с соавторами, In: Herbicide Resistant Crops, Lewis Publishers, 53-85, 1996. PCT заявка WO 0011200A2. Penaloza-Vazquez с соавторами, Plant Cell Reports, 14: 482-487, 1995. Redenbaugh с соавторами, In: Safety Assessment of Genetically Engineered Flavr SavrTM Tomato, CRC Press, Inc., 1992. Richaud с соавторами, J. Bacteriol., 166: 297-300, 1986. Sambrook с соавторами, In: Molecular cloning, Cold Spring Harbor Laboratory Press, Cold Spring Harbor, NY, 2000. Sathasiivan с соавторами, Nucl. Acids Res., 18: 2188-2193, 1990. Turner and Foster, Molec. Biotech., 3: 225, 1995. Формула изобретения1. Семя трансгенной кукурузы, содержащее более чем 4000 частей на миллион (ррm) свободного лизина, где семя кукурузы содержит нативную ДНК и одну или несколько экзогенных кассет для экспрессии в растениях, содержащих молекулу ДНК, кодирующую дигидродипиколинатсинтазу, в значительной степени устойчивую к ингибированию свободным L-лизином по принципу обратной связи, молекулу ДНК, транскрибируемую с получением молекулы РНК, подавляющей лизинкетоглутаратредуктазу/сахаропиндегидрогеназу, и молекулу ДНК, кодирующую аспартаткиназу, в значительной степени устойчивую к действию лизин-опосредованной обратной связи; где молекулы ДНК функционально связаны с одной или несколькими промоторными молекулами таким образом, что происходит транскрипция одной или нескольких молекул РНК в основном в эндосперме кукурузного семени, где, необязательно, семя кукурузы содержит экзогенный ген, придающий устойчивость к гербицидам. 2. Кукурузная мука, полученная из семени кукурузы по п.1, в которую не добавлен лизин. 3. Семя трансгенной кукурузы по п.1, которое содержит экзогенный ген, придающий устойчивость к гербицидам. 4. Семя трансгенной кукурузы по п.3, которое является устойчивым к гербициду глифосат. 5. Применение семени трансгенной кукурузы по п.1 для получения корма. 6. Применение семени трансгенной кукурузы по п.1 для получения муки грубого или тонкого помола. 7. Применение семени трансгенной кукурузы по п.1 для получения белкового концентрата или изолята. 8. Способ получения кукурузной муки, включающий получение семени трансгенной кукурузы, имеющего содержание лизина по меньшей мере 4000 частей на миллион (ppm), где семя кукурузы содержит нативную ДНК и одну или несколько экзогенных кассет для экспрессии в растениях, содержащих молекулу ДНК, кодирующую дигидродипиколинатсинтазу, в значительной степени устойчивую к ингибированию свободным L-лизином по принципу обратной связи, молекулу ДНК, транскрибируемую с получением молекулы РНК, подавляющей лизинкетоглутаратредуктазу/сахаропиндегидрогеназу, и молекулу ДНК, кодирующую аспартаткиназу, в значительной степени устойчивую к действию лизин-опосредованной обратной связи; где молекулы ДНК функционально связаны с одной или несколькими промоторными молекулами таким образом, что происходит транскрипция одной или нескольких молекул РНК в основном в эндосперме кукурузного семени, где, необязательно, семя кукурузы содержит экзогенный ген, придающий устойчивость к гербицидам, без добавления лизина, и переработку семени кукурузы с получением кукурузной муки. 9. Способ по п.8, где указанное семя трансгенной кукурузы содержит экзогенный ген, придающий устойчивость к гербицидам. 10. Способ по п.9, где семя трансгенной кукурузы является устойчивым к гербициду глифосат. 11. Применение семени трансгенной кукурузы по п.1 для употребления человеком или животным. Популярные патенты: 2282959 Устройство для крепления навесного оборудования к транспортному средству ... транспортное положение. Для этого вынимается ось 31, и передняя часть поворачивается вверх до совпадения другого отверстия 30 в передней части 22 с отверстием в задней части 21, и фиксируются обе части осью 31. Центральная тяга 19 фиксируется фиксатором 20.Для работы трактора с бульдозерным оборудованием нижние тяги фиксируются осью 31 в рабочем положении, опускаются в крайнее нижнее положение и передние части 22 нижних тяг переставляются с правой задней части 21 на левую и наоборот так, чтобы крюки 32 были установлены направленными друг к другу. После чего трактор подъезжает к бульдозерному оборудованию так, чтобы передняя часть нижних тяг оказалась под шаровыми шарнирами на оси ... 2272399 Зерноуборочный комбайн ... частях внутренних полостей которых установлены турбокомпрессоры 23 с воздухозаборниками 24, а в боковых стенках - сопловые устройства 25, их передние части открыты сверху, размещены под измельчителем 2 и на них установлены шнековые захватывающие устройства 26. Устройства для принудительного осевого перемещения обмолачиваемой массы выполнены в виде закрепленных на подбичниках 14 граблеобразных хвостовиков 27, зубья которых изогнуты вдоль винтовых линий, проходящих вокруг молотильных барабанов 13.Комбайн работает следующим образом.Скошенная жаткой 1 стеблевая масса поступает к измельчителю 2, где захватывается направляющими валками 6 и через противорежущее устройство 8 подается к ... 2115304 Доильный аппарат ... A 01 J 5/04, 1966. 2. Авторское свидетельство СССР N 971176, кл. A 01 J 5/02, A 01 J 7/00, 1982.5 ФОРМУЛА ИЗОБРЕТЕНИЯ Доильный аппарат, содержащий молокосборник, коллектор, двухкамерные доильные стаканы, основной и дополнительный пульсаторы, каждый из которых имеет камеры переменного и постоянного вакуума, при этом камера переменного вакуума основного пульсатора соединена с камерой постоянного вакуума дополнительного пульсатора, переменная камера которого соединена с воздухораспределительной камерой коллектора, отличающийся тем, что доильный аппарат снабжен установленной на молокосборнике молочной приставкой с полым поршнем, сообщающимся воздуховодом с камерой постоянного ... 2043709 Система управления работой форсунки разбрызгивателя ... моторедуктора подвижным контактом концевика. Время между импульсами от конечных зон концевика аппроксимируется в КНД, и вырабатываются управляющие сигналы для синтезатора временных интервалов (СВИ). СВИ на активном интервале концевика определяет точку начала подачи дозы с возможностью электронной перестройки или корректировки. Такое построение системы управления позволяет на порядок повысить точность определения момента подачи дозы и свести к минимуму влияние механических и иных факторов. Система управления при установке на механизмы подвергается сильным перепадам температур и воздействию агрессивных сред. Поэтому традиционное использование электролитических конденсаторов большой ... 2167648 Средство для защиты от укусов кровососущих насекомых (варианты) и способ его получения ... Simulium), мокрецов (p. Culicoides), слепней (p. Tabanus, p. Chrysopus), москитов (p. Phlebatomus). Пример N 1 Средство для защиты от укусов кровососущих насекомых содержит следующие ингредиенты, мас.%: 1) ДЭТА - 7,5 2) Сополимер малеиновый ангидрид/гексен ("А") и/или октадецен ("В") - 1,2 3) Вода - 84,0 4) Ацетостеарин - 3,0 5) Олеат полиэтиленгликоля - 3,0 6) Стеарат натрия - 0,5 7) Витамин E - 3,0 8) Цитраль - 0,5 Полимерный модификатор ДЭТА представляет собой тройной (или двойной) сополимер малеинового ангидрида с алкиловыми производными винила (в общей формуле для обоих мономеров заместитель R1: -H; a R2 для мономера "А": - С4H9; для мономера "В": - C16H33). Содержание "А" от ... |
Еще из этого раздела: 2039429 Линия производства молочных продуктов 2184433 Рабочий орган щелевателя 2261583 Выгрузное устройство бункера зерноуборочного комбайна 2236787 Способ испытаний опрыскивателей и устройство для его осуществления 2236122 Устройство для содержания животных 2264075 Рулонный пресс-подборщик лубяных культур 2298909 Устройство для сбора семян 2140137 Универсальный способ получения проросших семян сельскохозяйственных культур 2038763 Регулятор вакуума 2145478 Гранулированное либо пеллетированное средство для защиты растений, способ его получения и способ борьбы с грибами |
Изобретения в сельском хозяйстве
Обработка почвы в сельском и лесном хозяйствах
Посадка, посев, удобрение
Уборка урожая, жатва
Обработка и хранение продуктов полеводства и садоводства
Садоводство, разведение овощей, цветов, риса, фруктов, винограда, лесное хозяйство
Новые виды растений или способы их выращивания
Производство молочных продуктов
Животноводство, разведение и содержание птицы, рыбы, насекомых, рыбоводство, рыболовство
Поимка, отлов или отпугивание животных
Консервирование туш животных, или растений или их частей
Биоцидная, репеллентная, аттрактантная или регулирующая рост растений активность химических соединений или препаратов
Хлебопекарные печи, машины и прочее оборудование для хлебопечения
Машины или оборудование для приготовления или обработки теста
Обработка муки или теста для выпечки, способы выпечки, мучные изделия
|
|
||
 5773691, включенный в настоящее описание посредством ссылки). Нечувствительные к лизину формы AK были идентифицированы в ячмене, кукурузе и табаке. Было показано, что бактериальный ген DHDPS, выделенный из E.coli, по меньшей мере в 20 раз менее чувствителен к повышению содержания лизина (Glassman с соавторами, патент США
5773691, включенный в настоящее описание посредством ссылки). Нечувствительные к лизину формы AK были идентифицированы в ячмене, кукурузе и табаке. Было показано, что бактериальный ген DHDPS, выделенный из E.coli, по меньшей мере в 20 раз менее чувствителен к повышению содержания лизина (Glassman с соавторами, патент США  (Invitrogen Life Technologies, Carlsbad, California), в которой применяется сайт-специфичная реакция клонирования LR-рекомбиназы в системе Integrase/att бактериофага лямбда для создания векторной конструкции без использования эндонуклеаз и лигаз. В руководстве по использованию технологии клонирования GATEWAY
(Invitrogen Life Technologies, Carlsbad, California), в которой применяется сайт-специфичная реакция клонирования LR-рекомбиназы в системе Integrase/att бактериофага лямбда для создания векторной конструкции без использования эндонуклеаз и лигаз. В руководстве по использованию технологии клонирования GATEWAY