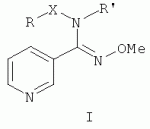
N,n-дизамещенные никотинамид-(z)-o-метилоксимы, обладающие фунгицидной активностьюПатент на изобретение №: 2442784 Автор: Марцынкевич Андрей Михайлович (RU), Захарычев Владимир Владимирович (RU), Шаранина Наталья Ивановна (RU) Патентообладатель: Государственное образовательное учреждение высшего профессионального образования "Российский химико-технологический университет им. Д.И. Менделеева" (РХТУ им. Д.И. Менделеева) (RU) Дата публикации: 20 Февраля, 2012 Начало действия патента: 23 Сентября, 2010 Адрес для переписки: 125047, Москва, Миусская пл., 9, "Российский химико-технологический университет им. Д.И. Менделеева" (РХТУ им. Д.И. Менделеева), патентно-лицензионный отдел Изобретение относится к химии N,N-дизамещенным никотинамид-(Z)-O-метилоксимам общей формулы I
где если Х означает метиленовую группу, то R означает фенил, бензил или 2-фурил, R' означает метил или n-хлорфенил, если X означает карбонильную группу, то R означает стирил, n-хлорстирил или бензил, R' означает метил, обладающий фунгицидной активностью. Технический результат: получены и описаны новые соединения, которые могут быть эффективны против вредоносных грибов. 10 пр., 1 табл. Изобретение относится к химии гетероциклических соединений, а именно к N,N-дизамещенным никотинамид-(Z)-O-метилоксимам общей формулы I, где если Х означает метиленовую группу, то R означает фенил, бензил или 2-фурил, R' означает метил или n-хлорфенил, если Х означает карбонильную группу, то R означает стирил, n-хлорстирил или бензил, R' означает метил, обладающим фунгицидной активностью
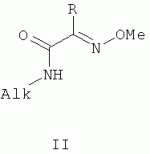
N,N - дизамещенные никотинамид-(Z)-O-метилоксимы общей формулы I могут найти применение для борьбы с вредоносными грибами в медицине, ветеринарии, сельском хозяйстве, строительстве. Известны соединения общей формулы II, где R означает орто-замещенный фенил [Патент ЕР 477631, 1990], обладающий фунгицидной активностью
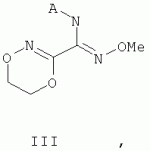
Известны азадиоксациклоалкены общей формулы III
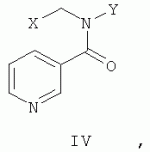
где Е означает метиленовую группу, А означает замещенный арил или гетарил, обладающие фунгицидной активностью [Пат. WO 95/04728, 1993]. Среди производных никотиновой кислоты наиболее близки по структуре к соединениям формулы I никотинамиды общей формулы IV
где Х означает 2-фурил, 2-пиридил, 3-пиридил, незамещенный или замещенный атомом галогена фенил, Y означает незамещенный, замещенный атомом галогена или бензилокси-группой фенил, проявляющие фунгитоксичность [Пат. РФ 2341525, 2008]. Несмотря на эффективность существующих сегодня фунгицидных препаратов, поиск новых средств борьбы с вредоносными грибами всегда остается актуальным из-за появления резистентных штаммов. Техническая задача, решаемая настоящим изобретением, состоит в расширении ассортимента фунгицидов для более эффективной борьбы с вредоносными грибами. Поставленная задача решается получением N,N-дизамещенных никотинамид-(Z)-O-метилоксимов общей формулы I, где если Х означает метиленовую группу, то R означает фенил, бензил или 2-фурил, R' означает метил или n-хлорфенил, если Х означает карбонильную группу, то R означает стирил, n-хлорстирил или бензил, R' означает метил, обладающих фунгицидной активностью. N,N - дизамещенные никотинамид-(Z)-O-метилоксимы общей формулы I, где Х означает метиленовую группу, R означает фенил, бензил или 2-фурил, R' означает метил или n-хлорфенил, могут быть получены метилированием N,N-дизамещенных (Z)-никотинамидоксимов общей формулы V, где Х означает метиленовую группу, R означает фенил, бензил или 2-фурил, R' означает метил или n-хлорфенил, в присутствии оснований различными метилирующими агентами, например диметилсульфатом, по известной методике [Rubina K. O-Alkylation of pyridine aldoximes under phase-transfer conditions. / Rubina K., Goldberg Yu., Gaukhman A., Shymanska M. // Synth. Comm. - 1989. - P.3129-3138.]: а также взаимодействием литиевых солей соединений общей формулы VI, где X, R и R' имеют те же значения, что и в формуле V, с O-метилникотингидроксамоилхлоридом: Реакции взаимодействия O-замещенных гидроксамоилхлоридов с основаниями описаны в литературе [Andersen N.H. Reaction of O-Methylbenzohydroximoyl Chlorides with Sodium Methoxide. Inversion of Configuration at Trigonal Carbon during Nucleophilic Substitution. / Andersen N.H., Costin C.R., Syrdal D.D., Svedberg D.P. // J. Am. Chem. Soc. - 1973. - P. 2051-2051]. Соединения общей формулы V могут быть получены известным способом из никотингидроксамоилхлорида и аминов общей формулы VI, где X, R и R' имеют те же значения, что и в формуле V: Аналогичные реакции описаны в литературе [Ехnеr О. Configuration and conformation of amidoximes. N,N-dialkyl derivatives. / Exner 0., Motekov N. // Coll. Czech Chem. Comm. -1982. - Vol.47. - P. 814 - 827]. N,N-дизамещенные никотинамид-(Z)-O-метилоксимы общей формулы I, где Х означает карбонильную группу, R означает стирил, n-хлорстирил или бензил, R' означает метил, могут быть получены ацилированием хлорангидридами кислот VII, где R означает стирил, n-хлорстирил или бензил, соединений общей формулы VIII, где R' означает метил: Соединения общей формулы VIII в свою очередь могут быть получены аналогично соединениям общей формулы V из соответствующих аминов. Никотингидроксамоилхлорид и O-метилникотингидроксамоилхлорид могут быть получены известными способами из соответствующих альдоксимов прямым хлорированием, а также из соответствующих N,N-незамещенных амидоксимов по реакции диазотирования. Такие способы представлены в литературе [Chiang Y.H. Chlorination of oximes. I. Reaction and mechanism of the chlorination of oximes in commercial chloroform and methylene chloride. / Chiang Y.H. // J. Org. Chem. - 1971. - Vol.36 - P. 2146-2155]. Изобретение может быть проиллюстрировано следующими примерами. Пример 1. Раствор 1,65 г (8,55 ммоля) гидрохлорида никотингидроксамоилхлорида в 10 мл МеОН прибавляли по каплям к 4 мл 7 М раствора MeNH 2 в МеОН при 0-5°С и перемешивали при указанной температуре 8 ч. Растворитель отгоняли в вакууме, к остатку добавляли 15 мл воды и экстрагировали СНСl3 (3×10 мл). Экстракт сушили над безводным сульфатом магния. Растворитель отгоняли в вакууме, остаток хроматографировали на колонке с силикагелем (элюент СНСl3-МеОН 10:1). Получили 1.05 г (79%) (Z)-N-метилникотинамидоксима в виде белого порошка с т.пл. 108-110°С. Спектр ЯМР 1Н ((CD3)2SO, Пример 2. Раствор 1,30 г (6,7 ммоль) гидрохлорида никотингидроксамоилхлорида в 25 мл МеОН прибавляли по каплям к 2,42 г (20 ммоль) N-метил-N-бензиламина в 30 мл МеОН при 0-5°С и перемешивали при указанной температуре 8 ч. Растворитель отгоняли в вакууме, к остатку добавляли 15 мл воды и экстрагировали СНСl3 (3×10 мл). Экстракт сушили над безводным сульфатом магния. Растворитель отгоняли в вакууме, остаток хроматографировали на колонке с силикагелем (элюент СНСl3-МеОН 10:1). Получили 1,29 г (80%) (Z)-N-метил-N-бензилникотинамидоксима в виде белого порошка с т.пл. 126-128°С. Спектр ЯМР 1H ((СD3)2SO, Пример 3. Смесь 0.37 г (6.8 ммоля) MeONa метилата натрия, 15 мл сухого ДМФА и 1.03 г (6.8 ммоль) N-метилникотинамидоксима охлаждали до 0°С и прибавляли к ней по каплям 0.65 мл (6.8 ммоль) диметилсульфата, поддерживая температуру 0-5°С. Реакционную массу перемешивали в течение 6 часов при той же температуре. Затем ДМФА удаляли в вакууме, а остаток растворяли в 30 мл холодной воды и эктрагировали эфиром (3×15 мл). Экстракт сушили над безводным сульфатом магния. Эфир удаляли в вакууме. Остаток перекристаллизовывали из изопропанола. Получили 0.54 г (48%) N-метилникотинамид-(Z)-O-метилоксима в виде белых кристаллов с т.пл. 83-85°С. Спектр ЯМР 1 H (CDCl3, Пример 4. К раствору 0,45 г (2,17 ммоль) N-(n-хлорфенил)-N-(2-фурилметил)амина в 10 мл ТГФ при температуре -10 - -5°С в атмосфере аргона прибавляли 1,36 мл 1,6 N (2,17 ммоль) раствора бутиллития. Затем, не снимая охлаждения, перемешивали смесь 20 минут и добавляли раствор 0,37 г (2,17 ммоль) O-метилникотингидроксамоилхлорида в 5 мл ТГФ. Реакционную массу кипятили в течение 10 часов, выливали в воду и экстрагировали эфиром (3×5 мл). Экстракт сушили над безводным сульфатом магния. Эфир удаляли в вакууме. Остаток хроматографировали на колонке с силикагелем (элюент гексан-ЕtOАс 5:1). Получили 0,15 г (20%) N-(n-хлорфенил)-N-(2-фурилметил)никотинамид-(Z)-O-метилоксим в виде светло-коричневых кристаллов с т.пл. 73-75°С. ЯМР 1H-спектр ((CD3)2SO, Пример 5. Смесь 224 мг (4,1 ммоль) метилата натрия, 15 мл сухого ДМФА и 1 г (4,1 ммоль) N-бензил-N-метилникотинамидоксима охлаждали до 0°С и прибавляли к ней по каплям 0,4 мл (4,1 ммоль) диметилсульфата, поддерживая температуру 0-5°С. Смесь перемешивали в течение 6 часов при той же температуре. Затем ДМФА удаляли в вакууме, а остаток растворяли в 60 мл холодной воды и эктрагировали эфиром (3×20 мл). Экстракт сушили над безводным сульфатом магния. Эфир удаляли в вакууме. Остаток хроматографировали на колонке с силикагелем (элюент СНСl3-МеОН 10:1). Получили 190 мг (18%) N-бензил-N-метилникотинамид-(Z)-O-метилоксима. Спектр ЯМР 1H ((СO3)2SO, Пример 6. Раствор 1,3 г (6,7 ммоль) гидрохлорида никотингидроксамоилхлорида в 25 мл МеОН прибавляли по каплям к 2,7 г (20 ммоль) N-метил-N-(2-фенилэтил)амина в 30 мл МеОН при 0-5°С и перемешивали при указанной температуре 8 ч. Растворитель отгоняли в вакууме, к остатку добавляли 15 мл воды и экстрагировали СНСl3 (3×10 мл). Экстракт сушили над безводным сульфатом магния. Растворитель отгоняли в вакууме, остаток хроматографировали на колонке с силикагелем (элюент СНСl3-МеОН 10:1). Получили 1,4 г (82%) (г)-N-метил-N-(2-фенилэтил)никотинамидоксима в виде желтого масла. Спектр ЯМР 1H ((СD2 )2SO, Пример 7. К раствору 0,138 г (0.84 ммоля) N-метилникотинамид-О-метилоксима и 0,122 г (1 ммоль) ДМАП в 25 мл СНСl3 прибавляли раствор 0,168 г (1 ммоль) циннамоилхлорида в 5 мл СНСl3 . Смесь кипятили 6 ч, охлаждали, промывали 20 мл воды и сушили над безводным сульфатом магния. Растворитель отгоняли в вакууме, остаток хроматографировали на колонке с силикагелем (элюент EtOАс-гексан 5:1). Получили 0,051 г (24%) N-метил-N-(Е)-циннамоилникотинамид-(Z)-O-метилоксима в виде масла. Спектр ЯМР 1H ((CD3) 2SO, Пример 8. К раствору 300 мг (1,81 ммоль) N-метилникотинамид-O-метилоксима и 244 мг (2,0 ммоль) ДМАП в 20 мл СНСl3 прибавляли раствор 365 мг (2,18 ммоль) n-хлорциннамиолхлорида в 20 мл СНСl3. Смесь кипятили 6 ч, охлаждали, промывали 20 мл воды и сушили над безводным сульфатом магния. Растворитель отгоняли в вакууме, остаток хроматографировали на колонке с силикагелем (элюент EtOAc-гексан 5:1). Получили 150 мг (25%) N-метил-N-((E-n-хлорциннамоил)никотинамид-(Z)- O-метилоксима в виде белых кристаллов с т.пл. 79-81°С. Спектр ЯМР 1Н ((СD3)2SO, Пример 9. К раствору 300 мг (1,81 ммоль) N-метилникотинамид-O-метилоксима и 244 мг (2,0 ммоль) ДМАП в 20 мл СНСl3 прибавляли раствор 309 мг (2,0 ммоль) фенилацетилхлорида в 20 мл СНСl 3. Смесь кипятили 6 ч, охлаждали, промывали 20 мл воды и сушили над безводным сульфатом магния. Растворитель отгоняли в вакууме, остаток хроматографировали на колонке с силикагелем (элюент EtOAc). Получили 70 мг (17%) N-метил-N-(фенилацетил)никотинамид-(Z)-О-метилоксима в виде масла. Спектр ЯМР 1H ((CD3) 2SO, ЯМР 1H-спектры зарегистрированы на приборе Bruker AM300 в (CD3) 2SO. Пример 10. Предварительную оценку фунгицидной активности некоторых соединений проводили in vitro против фитопатогенных грибов: Rhizoctonia solani Kühn (R.s.), Fusarium moniliforme Sheldon (F.m.) и Helminthosporium sativum Pammel, King et Bakke (Н.s.). Концентрация активного компонента составляла 30 мг/л. В качестве питательной среды использовали сахарозно-картофельный агар. Инокулированные среды выдерживали в термостате при 25°С в течение 3 суток. Активность соединений определяли как процент подавления роста мицелия гриба по отношению к контролю. Фунгицидная активность N,N-дизамещенных никотинамид-(Z)-O-метилоксимов общей формулы I приведена в таблице. По предварительной оценке активность N,N-дизамещенных никотинамид-(Z)-O-метилоксимов общей формулы I в ряде случаев сравнима или превышает активность эталона. Фунгицидная активность N,N-дизамещенных никотинамид-(Z)-О-метилоксимов общей формулы I Соединение Подавление радиального роста мицелия грибов в сравнении с контролем, % X RR' R.s.F.m. H.s.1 CH2 2-фурилn-СlС 6Н4- 6552 522 СН2 PhМе 3717 483 СН2 ВnMe 3966 864 C=O PhCH=CH-Me 48 4774 5 C=On-СlС6 Н4СН=СН- Me62 6281 6 C=OВn Me25 326 Эталон*70 6069 *Эталон - коммерческий фунгицид спироксамин (8-трет-бутил-1,4-диоксаспиро[4.5]декан-2-илметил(этил)(пропил)амин). X RR' R.s.F.m. H.s.1 CH2 2-фурилn-СlС 6Н4- 6552 522 СН2 PhМе 3717 483 СН2 ВnMe 3966 864 C=O PhCH=CH-Me 48 4774 5 C=On-СlС6 Н4СН=СН- Me62 6281 6 C=OВn Me25 326 Эталон*70 6069 *Эталон - коммерческий фунгицид спироксамин (8-трет-бутил-1,4-диоксаспиро[4.5]декан-2-илметил(этил)(пропил)амин).
Формула изобретенияN,N-дизамещенные никотинамид-(Z)-O-метилоксимы общей формулы I, где если Х означает метиленовую группу, то R означает фенил, бензил или 2-фурил, R' означает метил или n-хлорфенил, если Х означает карбонильную группу, то R означает стирил, n-хлорстирил или бензил, R' означает метил, обладающие фунгицидной активностью Популярные патенты: 2084132 Устройство для выращивания растений ... корневых систем растений. Наиболее близким техническим решением, принятым за прототип, является устройство для выращивания растений в малом объеме субстрата, размещаемом на пленочном пористом материале, соприкасающемся с двухслойными влагопроводящими элементами, образующими капилляры, опущенными в питающие каналы с регулируемым уровнем питательного раствора (А.с. СССР N 1537188 МКИ A 01 G 31/02, 1990 г.). Недостатком известного устройства является то, что оно не обеспечивает возможность перемещения корневой системы в процессе роста растений, отсутствует контроль солевого состава и влажности непосредственно в растильне, что в конечном счете не обеспечивает в достаточной степени ... 2127511 Композиция пленочного полимерного материала для покрытия теплиц и оптический активатор для полимерного материала (варианты) ... стронция, активированный европием, диспрозием и/или тербием, или сульфиды стронция, кальция, активированные европием, диспрозием и/или тербием при следующем соотношении компонентов, мас.%: Стабилизатор - 0,05 - 0,1 Оптический активатор - 0,01 - 0,5 Полимер - Остальное 2. Оптический активатор для полимерного материала на основе соединения европия, отличающийся тем, что в качестве соединений европия он содержит сульфид стронция, активированный европием, при следующем соотношении компонентов, мас.%: Сульфид стронция - 99,5 - 99,95 Европий 0,05 - 0,5 3. Активатор по п. 2, отличающийся тем, что он дополнительно содержит фосфат-ванадат иттрия, активированного европием в соотношении (1 - ... 2479988 Способ формирования линейно ориентированного виноградника с капельным орошением (версия 3) ... двух сторон избыточную ее длину изгибают и через отверстие в вертикальных опорах располагают ее внутри.4. Способ формирования линейно ориентированного виноградника с капельным орошением по п.1, отличающийся тем, что между двумя последовательными вертикальными опорами на последовательных уровнях располагают направляющие проволоки разной длины.5. Способ формирования линейно ориентированного виноградника с капельным орошением по п.1, отличающийся тем, что в продолжение двух крайних вертикальных опор линейно ориентированного виноградника устанавливают вспомогательные опоры с крепежным цилиндром с отверстием, количество которых соответствует числу направляющей проволоки, и после введения ... 2238970 Штамм mycelia sterilia лх-1-продуцент комплекса биологически активных веществ, обладающих рострегуляторными свойствами ... №5, 1975/.Известен препарат “Симбиот-2”, стимулирующий урожайность растений, полученный из продуктов метаболизма грибов-эндофитов (ав.св. СССР №921488). В качестве сырья для его изготовления используют эндофиты, выделенные из корней облепихи.Недостатком известных стимуляторов роста является невысокая активность препаратов, полученных из эндофитов растений, обладающих наибольшей лекарственной ценностью.Известен препарат Симбионт-1, изготавливающийся из эндофитов, выделенных из корней жень-шеня. Препарат эффективен только при хороших условиях роста растений (ав.св. СССР №370932).Общим недостатком известных препаратов является невозможность идентифицировать получаемую с ... 2154931 Корнеуборочная машина ... рамы 1, установленной на ходовые колеса 2, выкапывающих рабочих органов 3, битера 4, сепаратора 5, образованного валиками, вращающимися в одну сторону. Над серединой восходящего участка сепаратора 5 установлена приводная цилиндрическая щетка 6 с эластичными прутками, а в верхней его части установлен лопастной метатель 7 корнеплодов. За сепаратором 5 установлен поперечный транспортер 8, который охвачен по бокам стенками 9, между которыми вверху установлены две встречновращающиеся цилиндрические щетки 10, под которыми установлены две изогнутые плоскости 11, в центре изгибов которых имеются цилиндрические шарниры, установленные на осях 12 рамы 1, образующие лоток. Размеры плоскостей 11 ... |
Еще из этого раздела: 2054235 Лесопосадочная машина 2420949 Способ оценки потенциальной урожайности семянок сафлора красильного 2473366 Вещество, обладающее антимикробным действием 2040152 Способ выращивания корнеплодных культур в контролируемых условиях и установка для его осуществления 2159526 Устройство для навешивания сельскохозяйственных орудий на трактор 2075933 Композиция для иммунизации растений от различных фитопатогенов 2171570 Устройство для группового учета надоев молока при доении 2154296 Зерноуборочная машина, преимущественно зерноуборочный комбайн, с мультипроцессорным управляющим устройством 2209542 Контейнер 2250602 Широкозахватный колесный дождеватель |
Изобретения в сельском хозяйстве
Обработка почвы в сельском и лесном хозяйствах
Посадка, посев, удобрение
Уборка урожая, жатва
Обработка и хранение продуктов полеводства и садоводства
Садоводство, разведение овощей, цветов, риса, фруктов, винограда, лесное хозяйство
Новые виды растений или способы их выращивания
Производство молочных продуктов
Животноводство, разведение и содержание птицы, рыбы, насекомых, рыбоводство, рыболовство
Поимка, отлов или отпугивание животных
Консервирование туш животных, или растений или их частей
Биоцидная, репеллентная, аттрактантная или регулирующая рост растений активность химических соединений или препаратов
Хлебопекарные печи, машины и прочее оборудование для хлебопечения
Машины или оборудование для приготовления или обработки теста
Обработка муки или теста для выпечки, способы выпечки, мучные изделия
|
|
||
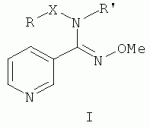
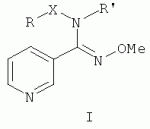




 , м.д., J, Гц): 2.59 (д, 3 Н, СН3, J=6.6); 5.91 (к, 1 Н, NH, J=6.6); 7.41-7.49 (м, 1Н, 5-СН ру); 7.83 (д, 1 Н, 4-СН ру, J=8.3); 8.61 (д, 1 Н, 6-СН ру, J=4.2); 8.62 (с, 1 Н, 2-СН ру); 9.81 (с, 1 Н, ОН).
, м.д., J, Гц): 2.59 (д, 3 Н, СН3, J=6.6); 5.91 (к, 1 Н, NH, J=6.6); 7.41-7.49 (м, 1Н, 5-СН ру); 7.83 (д, 1 Н, 4-СН ру, J=8.3); 8.61 (д, 1 Н, 6-СН ру, J=4.2); 8.62 (с, 1 Н, 2-СН ру); 9.81 (с, 1 Н, ОН).