Кофейное растение с пониженной активностью -d-галактозидазыПатент на изобретение №: 2303349 Автор: МАРРАЧЧИНИ Пьер (BR), ДЕЗЕЙ Ален (FR), РОДЖЕРС Джон (FR) Патентообладатель: СОСЬЕТЕ ДЕ ПРОДЮИ НЕСТЛЕ С.А. (CH) Дата публикации: 20 Апреля, 2005 Начало действия патента: 15 Августа, 2002 Адрес для переписки: 129090, Москва, ул. Б.Спасская, 25, стр.3, ООО "Юридическая фирма Городисский и Партнеры", пат.пов. Е.Е.Назиной, рег. № 517 Изобретение относится к биотехнологии, в частности к модификации галактоманнанов в зеленых кофейных зернах путем снижения эндогенного уровня активности Настоящее изобретение относится к модификации галактоманнанов, находящихся в зеленых кофейных зернах, путем снижения эндогенного уровня активности В кофейных зернах содержание полисахаридов клеточной оболочки составляет примерно 48% сухого вещества зрелых кофейных зерен, из которых на долю маннанов приходится примерно половина. В основном данные полисахариды являются нерастворимыми в очищенной форме и имеют очень низкую степень разветвления галактозы (Bradbury and Haliday, J. agric. Food Chem. 38 (1990), 389-392). Считается, что полимеры маннаны являются основной причиной больших потерь исходной массы зеленого кофе при получении растворимых кофейных напитков. Потери происходят либо когда нерастворимый материал остается в виде осадка во время первоначальной экстракции, либо когда во время хранения кофейного напитка образуются осадки и гели. Также было показано, что маннаны являются основным компонентом, ответственным за помутнение и осаждение кофейных напитков при отстаивании. Было установлено, что в некоторых растениях степень разветвления галактозы в маннановых цепях частично зависит от активности Также активность кДНК В свете известного влияния галактоманнанов на получение и/или стабильность при хранении растворимого кофе в данной области техники имеется потребность в совершенствовании данной ситуации. Следовательно, целью настоящего изобретения является обеспечение усовершенствованного способа получения растворимого кофе при одновременном устранении недостатков, известных как имеющиеся при хранении кофейного напитка. Вышеуказанная проблема была решена путем получения клетки кофейного растения и соответственно кофейного растения, где степень разветвления галактозы в галактоманнанах была повышена. По предпочтительному воплощению данная цель может быть достигнута снижением эндогенного уровня активности По другому предпочтительному воплощению подобный сниженный эндогенный уровень активности С этой целью антисмысловая копия мРНК, кодируемая геном Нуклеиновая кислота, кодирующая рибонуклеиновую кислоту, антисмысловую к мРНК, кодируемой геном По предпочтительному воплощению используемый промотор представляет собой cspl-промотор кофе, который обеспечивает достаточно высокий уровень транскрипции. Следовательно, настоящее изобретение обеспечивает соответственно модифицированную клетку кофейного растения и кофейное растение, где уровень активности Настоящее изобретение также обеспечивает способ получения растворимого кофе, который включает стадию использования кофейных зерен, полученных из растения, обладающего пониженной активностью Данное изобретение относится к повышению растворимости галактоманнанов кофе путем увеличения степени разветвления галактозы в них. Принятой стратегией является снижение эндогенного уровня активности Данный cspl-промотор уже охарактеризован (Marraccini et al., Plant Physiol. Biochem. 37 (1999), 273-282) и регулирует экспрессию гена, кодирующего запасающий белок 11S кофе. Была сконструирована кассета, включающая данный промотор, и введена в область Т-ДНК бинарного вектора трансформации, полученного из плазмиды pTiT37 (Bevan, Nucl. Acids Res. 12 (1984), 8711-8721). Данный рекомбинантный вектор был встроен в Agrobacterium tumefaciens, которую использовали для трансформации эксплантатов кофе. Регенерировали кофейные растения, несущие Т-ДНК, встроенную в их геном, и анализировали на активность I. Анализ активности Собирали плоды на различных стадиях созревания (возраст выражался в неделях после цветения: WAF) Coffea Arabica сорта Caturra Т2308, растущего в теплице (температура примерно 25°С, 70% влажность и естественное освещение). После сбора зерна замораживали в жидком азоте и хранили при -85°С до использования. Для проведения исследований по созреванию отделяли ткани эндосперма и перисперма. Растительный материал измельчали в жидком азоте и экстрагировали на льду холодным буфером для выделения фермента (глицерин 10% об./об., 10 мМ метабисульфита натрия, 5 мМ ЭДТА, 40 мМ MOPS (NaOH), рН 6,5) при примерном соотношении 20 мг на 100 мкл. Смесь перемешивали на льду в течение 20 мин, центрифугировали (12000 g · 30 мин), разливали на порции и хранили при -85°С до использования. Активность Реакционная смесь содержала 200 мкл 100 мМ pNGP в буфере МакИлваина (100 мМ лимонной кислоты - 200 мМ Na2HPO4, рН 6,5) до конечного объема 1 мл с экстрактом фермента. Реакцию проводили при 26°С и начинали добавлением фермента и останавливали добавлением 4 объемов раствора для остановки реакции (100 мМ Na2CO3-NaHCO 3, рН 10,2). Поглощение определяли при 405 нм. Рассчитывали образование нитрофенила с использованием молярного коэффициента экстинкции Активность II. Выделение полноразмерной кДНК Несмотря на то, что в литературе имеются данные по нескольким последовательностям кДНК Библиотеку кДНК Coffea arabica сорта Caturra T2308 конструировали с помощью полиА+мРНК, выделенной через 30 недель после цветения по методу Rogers et al. (Plant Physiol. Biochem., 37 (1999), 261-272). Данную плазмидную библиотеку кДНК (10 нг) тестировали ПЦР с использованием праймеров BETA1 (SEQ ID NO:2) и BETA3 (SEQ ID NO:3), непосредственно расшифрованных из последовательности кДНК По литературным данным 5'-конец кДНК Полученная кДНК содержит открытую рамку считывания из 1263 п.н. с началом в положении 51 и концом в положении 1313 последовательности SEQ ID NO:1. Продукт трансляции соответствует последовательности SEQ ID NO:2, на основании чего можно предположить, что III. Экспрессия гена Прослеживали экспрессию гена, кодирующего После разгонки РНК окрашивали бромистым этидием (ВЕТ) по Sambrook et al. (Molecular Cloning, A Laboratory Manual, Cold Spring Harbor Laboratory Press, США, 1989, chapter 9.31 to 9.51). Данная процедура позволяет стандартизировать количества, отложенные на геле, от интенсивности флуоресценции рибосомальных 18S- и 25S-РНК. Затем общую фракцию РНК переносили и фиксировали на положительно заряженных нейлоновых мембранах согласно рекомендациям изготовителя Boehrinfer Mannheim (Roche-Boehringer Mannheim GmbH, Biochemica, Postfach 310120, Mannheim 31, DE). Прегибридизацию и гибридизацию проводили в условиях, описанных выше. Результаты нозерн-блоттинга показывали пик экспрессии гена на ранней стадии развития эндосперма. Пик экспрессии специфической мРНК в условиях теплицы имеет место примерно через 26 WAF и соответствует началу повышения ферментативной активности. Период максимальной экспрессии мРНК соответствует основному периоду распускания и затвердевания эндосперма в созревающих зернах в данных условиях. Пик экспрессии специфической мРНК IV. Конструкция антисмысловой кассеты Последовательность 11S-промотора (Marraccini et al., Plant Physiol. Biochem. 37 (1999), 272-282) из кофе амплифицировали со специфическим праймером UP210-1, соответствующим последовательности SEQ ID NO:7, и BAGUS2, соответствующим последовательности SEQ ID NO:8. Олигонуклеотид UP210-1 соответствует последовательности между нуклеотидами 24 и 76, опубликованной Marraccini et al., выше, и содержит на 5'-конце синтетическую последовательность CGGGGTACCCCG, включающую сайт рестрикции KpnI и соответствующую последовательности SEQ ID NO:9. Праймер BAGUS2 содержит на 5'-конце синтетическую последовательность CGCGGATCCGCG, соответствующую последовательности SEQ ID NO:10, которая несет сайт рестрикции BamHI. Данный праймер также включает нуклеотиды 998-976 последовательности, опубликованной Marraccini et al. (1999). Данную реакцию проводили в присутствии ДНК-полимеразы Pfu (3 единицы) с 10 нг pCSPP4 (WO 99/02688) в конечном объеме 50 мкл, содержащем 10 мМ KCl, 6 мМ (NH4)2SO 4, 20 мМ Трис-HCl, рН 8,0, 0,1% Тритона Х-100, 2 мМ MgCl 2, 10 мкг/мл BSA, 0,2 мМ каждого dNTP, 0,25 мкМ каждого из олигонуклеотидов, описанных выше. Затем реакционную смесь инкубировали в течение 30 циклов (94°С - 60 сек, 55°С - 60 сек, 72°С - 3 мин) с последующим конечным циклом удлинения при 72°С в течение 7 мин. Фрагменты ПЦР размером примерно 950 п.н. выделяли на картридже Microcon 100 (Millipore, Франция) и лигировали в вектор pCR-Script Amp SK (+) в присутствии ДНК-лигазы Т4 (Promega Corporation, 2800 Woods Hollow Road, Madison, Wisconsin 53711, США), следуя рекомендациям изготовителя. Затем штамм E. coli XL1-Blue MRF' трансформировали полной смесью для лигирования. Отбирали один трасформант и его плазмиду выделяли для секвенирования вставки для определения ориентации фрагмента ПЦР. Проведенный таким образом анализ позволил отобрать плазмиду pLP7. Более короткий вариант 11S-промотора также амплифицировали с использованием того же подхода, за исключением того, что праймер UP213-1, имеющий последовательность нуклеиновой кислоты SEQ ID NO:11, замещал праймер UP210-1. Данный праймер соответствует последовательности нуклеотидов 754-777, опубликованной Marraccini et al., выше, и содержит на 5'-конце синтетическую последовательность SEQ ID NO:9. Это приводило к амплификации фрагмента 250 п.н. p11S-промотора кофе, который клонировали, как описано ранее с получением плазмиды pLP8. Терминатор TNOS амплифицировали, следуя методике, описанной для амплификации р11S-промотора, за исключением того, что использовали праймер TNOS1, имеющий последовательность нуклеиновой кислоты SEQ ID NO:12, и TNOS2, имеющий последовательность нуклеиновой кислоты SEQ ID NO:13. TNOS1 включает последовательность SEQ ID NO:10 на 5'-конце. TNOS2 включает последовательность SEQ ID NO:9 на 5'-конце последовательности. Данные праймеры приводили к амплификации последовательности TNOS из промышленно доступного вектора р35SGFP (Clontech Laboratories Inc., 1020 East Meadow Circle, Palo Alto, California 94303-4230, США). Продукт ПЦР клонировали в вектор pCR-Script Amp SK (+), как описано ранее, с получением рекомбинантного вектора, названного pLP32, и его секвенировали для определения его ориентации. Затем данный вектор расщепляли рестриктазой BamHI с удалением последовательности TNOS, которую затем обрабатывали ДНК-полимеразой Т4 с получением В«затупленныхВ» концов. Затем векторы pLP7 и pLP8 линеаризовали с помощью EcoRI и также обрабатывали ДНК-полимеразой Т4 с получением В«затупленныхВ» концов. Затем TNOS-терминатор клонировали в правильной ориентации в векторах pLP7 и pLP8 с получением соответственно векторов p11STNOS7 и p11STNOS7+. кДНК Данную плазмиду расщепляли рестриктазой BamHI с выделением кДНК Для включения данных кассет в бинарный вектор, использованный для трансформации кофейной клеточной суспензии, проводили конечную реакцию ПЦР с ДНК-полимеразой Pfu с использованием праймеров UPSAL1, имеющего последовательность нуклеиновой кислоты SEQ ID NO:16, и UPSAL2, имеющего последовательность нуклеиновой кислоты SEQ ID NO:17. Оба олигонуклеотида включают сайт рестрикции SalI и последовательности распознавания ДНК вектора pCR-Script Amp SK (+), фланкирующего с ДНК-областями 11S-промотора и NOS-терминатора (TNOS). Кроме того, данный сайт рестрикции отсутствует в последовательности, предназначенной для введения в Т-ДНК бинарной плазмиды. Данные продукты ПЦР вновь клонировали в вектор pCR-Script Amp SK (+), который расщепляли рестриктазой SalI для подтверждения того, что данный сайт рестрикции фланкирован с кассетами. Полученные плазмиды были названы соответственно pALP414 и pALP50 и происходили соответственно от pALPHA1 и pALPHA9. V. Клонирование антисмысловой кассеты Кассеты VI. Трансформация Agrobacterium tumefaciens Бинарные векторы трансформации pBIA121, pBIA126 и pBIA9, описанные выше, независимо вводили в штамм Agrobacterium tumefaciens LBА4404 без В«плечВ» c использованием метода прямой трансформации, описанного An et al. (Plant Mol. Biol. Manuel, Gelvin, Schilperoort and Verma Eds, Kluwer Academic Publishers Dordrecht, Нидерланды, A3 (1993), 1-19). Для каждой трансформации отбирали рекомбинантные клоны Agrobacterium tumefaciens на среде LB с добавлением канамицина (50 мкг/мл), стрептомицина (100 мкг/мл) и рифампицина (50 мкг/мл). Для проверки структуры введенных в Agrobacterium tumefaciens плазмид их выделяли экспрессивным минипрепаративным методом и затем анализировали рестрикционным картированием после обратной трансформации в штамме E. coli XL2 Blue MRF'. VII. Трансформация Coffea sp. Культивировали эксплантаты листьев и субкультивировали каждые пять недель в течение 3-5 месяцев, пока не появлялись соматические зародыши по краю эксплантатов. Соматические зародыши собирали на стадии покоя, надрезали стерильным скальпелем и замачивали в течение двух часов в 0,9% растворе NaCl, содержащем рекомбинантный штамм Agrobacterium tumefaciens LBA4404 до OD 600 нм 0,3-0,5. Проводили совместное культивирование в темноте на полутвердой среде MS без гормонов в течение трех суток и затем отмывали в жидкой среде MS, содержащей цефотаксим (1 г/л) в течение 3-5 ч при постоянном, но мягком встряхивании. Зародыши культивировали на полутвердой среде с 5 мкМ ВАР, 90 мкМ сахарозы в присутствии цефотаксима (400 мг/л) при низкой освещенности (период освещения 16 ч в день). Через 3-4 недели их переносили на селективную среду MS с добавлением цефотаксима (400 мг/л) и хлорсульфурона (80 мг/л). Затем их переносили каждый месяц на свежую селективную среду до регенерации каллусов. Трансформированные зародыши, растущие вокруг каллусов, затем культивировали на полутвердой среде MS с витаминами Morel (1 мкМ ВАР и 30 мкМ сахарозы) для индукции их роста. После данной стадии их переносили на среду для укоренения, соответствующую среде, описанной выше, но без ВАР. Для проверки эффективности трансформации каллусы, веточки, корни и листья регулярно тестировали на экспрессию uidA-репортера с помощью гистохимического метода GUS (Jefferson et al., J. EMBO 6 (1987), 3901-3907). После данной процедуры отбирали несколько отдельных растений и размножали в условиях in vitro с помощью микрочеренков. Некоторые из них переносили в теплицу для достижения развития. Морфологических аномалий не наблюдали. VIII. Анализ соматических зародышей из трансформированных кофейных растений Соматические зародыши также индуцировали из эксплантатов листьев для детектирования присутствия антисмысловой мРНК Из 100 мг трансформированных соматических зародышей выделяют общую фракцию РНК, как описано ранее, и тестировали ОТ-ПЦР с использованием набора Access RT-PCR system (Promega, США). Вначале подтверждали присутствие специфической мРНК 11S осуществлением ОТ-ПЦР с использованием праймеров, расположенных в кодирующей последовательности 11S-кДНК. Данную процедуру проводили с использованием праймера SO11, соответствующего последовательности SEQ ID NO:18, и SO2-1, соответствующего последовательности SEQ ID NO:19. Праймер SO11 соответствовал последовательности между нуклеотидами 1035 и 1059 последовательности, опубликованной Marraccini et al., выше. С другой стороны, праймер SO2-1 соответствовал последним 24 нуклеотидам в опубликованной последовательности. Синтез первой цепи кДНК (стадия обратной транскрипции) проводили, как описано изготовителем (45 мин, 48°С). Для реакции ПЦР использовали следующие параметры: 45 циклов (60 сек при 94°С на стадии денатурации, 90 сек при 52°С на стадии отжига, 4 мин при 68°С на стадии удлинения) с конечным удлинением при 68°С в течение 7 мин. В результате этого опыта получали продукт ПЦР из 1590 п.н., соответствующий последовательности 11S-кДНК, фланкированной праймерами SO11 и SO2-1. Данные подтверждали, что мРНК 11S отсутствовала во всех тестированных тканях, т.е. корнях, листях, цветах, но имелась в высокой концентрации в соматических зародышах Coffea canephora, а также в зернах через 27 WAF. Второе, тестировали присутствие смысловой мРНК Параллельно проводили детектирование антисмысловой мРНК Список последовательностей приведен в конце описания. Формула изобретения1. Клетка кофейного растения, продуцирующая галактоманнаны, включающая нуклеиновую кислоту, которая транскрибируется в рибонуклеиновую кислоту, которая является антисмысловой к мРНК, происходящей из гена 2. Клетка кофейного растения по п.1, отличающаяся тем, что промотор представляет собой кофейный промотор csp1. 3. Кофейное растение, содержащее растительную клетку по любому из предшествующих пунктов. 4. Способ получения растворимого кофе, включающий стадию использования кофейных зерен, полученных из кофейного растения по п.3. 5. Способ повышения растворимости кофе, включающий стадию использования кофейных зерен, полученных из растения по п.3. 6. Применение зерен, полученных из кофейного растения по п.3, для получения растворимого кофе. MM4A Досрочное прекращение действия патента из-за неуплаты в установленный срок пошлины за поддержание патента в силе Дата прекращения действия патента: 16.08.2010 Дата публикации: 10.12.2011 Популярные патенты: 2021671 Машина для уборки льна-долгунца ... с возможностью ее перемещения по дополнительной раме, вдоль имеющихся осей шкивов основного конвейера, а устройство для отделения семенной части урожая от стеблей установлено на другой рамке с возможностью перемещения вдоль осей шкивов зажимного транспортера по имеющимся направляющим, закрепленным в верхней части рамы, причем рамки устройства для выпрямления ленты льна и устройство для отделения семенной части урожая соединены кинематической связью с возможностью перемещения их в противоположные стороны. 2. Машина по п.1, отличающаяся тем, что кинематическая связь выполнена в виде троса, взаимодействующего с имеющимися блоками, установленными на рамах. MM4A - Досрочное прекращение ... 2180475 Устройство для поштучной подачи предметов, в частности семян сельскохозяйственных культур ... неподвижная в круговом направлении шайба с отверстием, диаметр которого равен диаметру каналов бункера, а центр лежит на окружности, проходящей через центры указанных каналов, которые выполнены с возможностью, по меньшей мере, частичного поочередного совмещения с отверстием в упомянутой шайбе при повороте бункера, а средство для подачи сжатого газа в полость бункера выполнено с возможностью подачи сжатого газа к упомянутому отверстию в шайбе. 5. Устройство по одному из пп. 1-4, отличающееся тем, что устройство снабжено цилиндрической стенкой между верхней и нижней частями бункера, расположенной соосно с ними и ограничивающей центральную полость бункера, вдоль периметра нижней ... 2160533 Способ профилактики и коррекции транспортного стресса у крупного рогатого скота ... 8,2 кг (1,92%); 10,1 кг (2,35%) и 6,5 кг (1,53%). Следовательно, скармливание убойному молодняку в течение семи суток до транспортировки корня солодки позволило сократить потери живой массы в среднем на 7,6 кг (1,7%). Наибольшим сокращением потерь живой и убойной массы характеризовался молодняк, получавший корень солодки в количестве 3,0 г/кг живой массы - 10,1 кг (2,35%) и 9,8 кг (4,2%) соответственно. Применение корня солодки в течение 8 суток до транспортировки (табл. 4) позволило сохранить потери живой массы в среднем на 8,55 кг (2,0%) и увеличить (сохранить) массу туши на 6,7 кг (2,9%), а внутреннего сала - на 1,9 кг (14,39%). Максимальный эффект получен при использовании ... 2105446 Плоскорежущая лапа ... предназначено для использования в сельскохозяйственном машиностроении; для заявленного изобретения в том виде, как оно охарактеризовано в независимом пункте формулы изобретения, подтверждена возможностью его осуществления с помощью вышеописанных в заявке или известных до даты приоритете средств и методов; средство, воплощающее заявленное изобретение при его осуществлении, способно обеспечить достижение усматриваемого заявителем технического результата. Следовательно, изобретение соответствует требованию "промышленная применимость" по действующему законодательству. ФОРМУЛА ИЗОБРЕТЕНИЯ 1. Плоскорежущая лапа, включающая стойку с рабочей кромкой и задней стенкой, на ... 2253964 Способ отделения семенной части урожая льна от стеблей и устройство для его осуществления ... в то же время уменьшает повреждение (расплющивание) стеблей. За счет того, что первый прочес ленты производят, начиная с вершин растений, с постепенным увеличением зоны очеса, уменьшается усилие, действующее со стороны зубьев на стебли. Расчесывание и паралпелизацию стеблей выполняют с ориентированием их в направлении перпендикуляра к длине ленты. Поэтому уменьшается боковое давление на стебли и нахлестывание последних на зубья. Из-за того, что два соседних зуба, действующих на одну и ту же порцию стеблей, расположены на одинаковом расстоянии от плоскости торцов шкивов зажимного транспортера, ликвидируется изгибающее усилие на стебли со стороны соседних зубьев.Таким образом, ... |
Еще из этого раздела: 2248687 Способ весеннего боронования озимых культур и зубовая борона для его осуществления 2056737 Способ диагностики морозоустойчивости плодовых культур 2188534 Способ уборки льна-долгунца 2296457 Устройство для магнитно-импульсной обработки растений 2260943 Способ подращивания личинок осетровых рыб 2234219 Композиция для отпугивания паразитов 2055465 Система приготовления и подачи питательного раствора в теплице 2159526 Устройство для навешивания сельскохозяйственных орудий на трактор 2275804 Способ повышения продуктивности птицы 2446659 Способ и устройство для органического возделывания зерновых культур |
Изобретения в сельском хозяйстве
Обработка почвы в сельском и лесном хозяйствах
Посадка, посев, удобрение
Уборка урожая, жатва
Обработка и хранение продуктов полеводства и садоводства
Садоводство, разведение овощей, цветов, риса, фруктов, винограда, лесное хозяйство
Новые виды растений или способы их выращивания
Производство молочных продуктов
Животноводство, разведение и содержание птицы, рыбы, насекомых, рыбоводство, рыболовство
Поимка, отлов или отпугивание животных
Консервирование туш животных, или растений или их частей
Биоцидная, репеллентная, аттрактантная или регулирующая рост растений активность химических соединений или препаратов
Хлебопекарные печи, машины и прочее оборудование для хлебопечения
Машины или оборудование для приготовления или обработки теста
Обработка муки или теста для выпечки, способы выпечки, мучные изделия
|
|
||
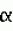 -D-галактозидазы. Получают клетку кофейного растения, которая включает нуклеиновую кислоту, транскрибируемую в рибонуклеиновую кислоту, которая является антисмысловой к мРНК, происходящей из гена
-D-галактозидазы. Получают клетку кофейного растения, которая включает нуклеиновую кислоту, транскрибируемую в рибонуклеиновую кислоту, которая является антисмысловой к мРНК, происходящей из гена 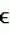 = 18300 (специфичный для рН 10,2) и превращали в ммоль·мин -1·мг белка-1. Общее содержание белка определяли в пробах, экстрагированных водным буфером, по методу Бредфорда (Bradford, Anal. Biochem., 72 (1976), 248-254). Для экспрессии активности каждую пробу экстрагировали и разливали на порции, анализ проводили в трех параллелях, результаты выражали в виде средних значений.
= 18300 (специфичный для рН 10,2) и превращали в ммоль·мин -1·мг белка-1. Общее содержание белка определяли в пробах, экстрагированных водным буфером, по методу Бредфорда (Bradford, Anal. Biochem., 72 (1976), 248-254). Для экспрессии активности каждую пробу экстрагировали и разливали на порции, анализ проводили в трех параллелях, результаты выражали в виде средних значений.








