Способ получения производных 2-анилинопиримидина или их кислотно-аддитивных солейПатент на изобретение №: 2017735 Автор: Адольф Хубеле[DE] Патентообладатель: Циба-Гейги АГ (CH) Дата публикации: 15 Августа, 1994 Изображения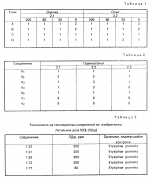 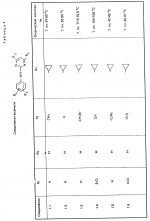 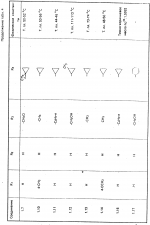 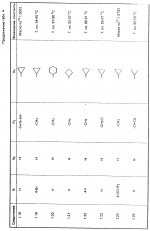 Использование: в сельском хозяйстве как обладающий фунгицидной и инсектицидной активностью. Сущность изобретения: способ получения производных 2 - анилинопиримидина общей формулы I 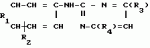 , где R1 - H; галоген; R2 - H, галоген, метил; R3 - (C1-C4) алкил, незамещенный или замещенный галогеном, циклопропил, R4 - цикло - пропил, незамещенный или замещенный галогеном, метилом или их кислотно-адитивных солей, заключающийся в том, что мочевину вводят во взаимодействие с дикетоном формулы II; R3-C(O)CH2C(O)R4 в присутствии кислоты в инертном растворителе при 20 - 140В°С и после этого циклизуют при температуре кипения флегмы с образованием 2-оксипиримидина формулы III , где R1 - H; галоген; R2 - H, галоген, метил; R3 - (C1-C4) алкил, незамещенный или замещенный галогеном, циклопропил, R4 - цикло - пропил, незамещенный или замещенный галогеном, метилом или их кислотно-адитивных солей, заключающийся в том, что мочевину вводят во взаимодействие с дикетоном формулы II; R3-C(O)CH2C(O)R4 в присутствии кислоты в инертном растворителе при 20 - 140В°С и после этого циклизуют при температуре кипения флегмы с образованием 2-оксипиримидина формулы III 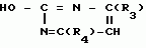 гидроксигруппу в полученном соединении в присутствии или отсутствии растворителя под действием избыточного количества PO(Hal)3 при температурах 50 - 110В°С заменяют галоидом и полученное соединение формулы II гидроксигруппу в полученном соединении в присутствии или отсутствии растворителя под действием избыточного количества PO(Hal)3 при температурах 50 - 110В°С заменяют галоидом и полученное соединение формулы II 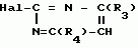 вводят во взаимодействие с производным анилина формулы I вводят во взаимодействие с производным анилина формулы I 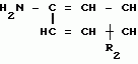 при 60 - 120В°С в инертном растворителе в присутствии или отсутствии кислоты, целевой продукт выделяют в свободном виде или в виде соли. 4 табл.
Изобретение относится к способам получения производных 2-анилинопиримидина или их кислотно-аддитивных солей - новых биологически активных соединений, которые могут найти применение в сельском хозяйстве. Известны производные N-пиримидиланилинов, обладающие способностью поражать паразитирующие на растениях грибы. Однако их фунгицидная и инсектицидная активность недостаточно высоки. Цель изобретения - способ получения новых производных 2-анилинопиримидина или их кислотно-аддитивных солей, малотоксичных соединений и обладающих более высокой инсектицидной активностью одновременно при хорошей совместимости с растениями. Поставленная цель достигается описываемым способом получения производных 2-анилинопиримидина формулы 1 при 60 - 120В°С в инертном растворителе в присутствии или отсутствии кислоты, целевой продукт выделяют в свободном виде или в виде соли. 4 табл.
Изобретение относится к способам получения производных 2-анилинопиримидина или их кислотно-аддитивных солей - новых биологически активных соединений, которые могут найти применение в сельском хозяйстве. Известны производные N-пиримидиланилинов, обладающие способностью поражать паразитирующие на растениях грибы. Однако их фунгицидная и инсектицидная активность недостаточно высоки. Цель изобретения - способ получения новых производных 2-анилинопиримидина или их кислотно-аддитивных солей, малотоксичных соединений и обладающих более высокой инсектицидной активностью одновременно при хорошей совместимости с растениями. Поставленная цель достигается описываемым способом получения производных 2-анилинопиримидина формулы 1 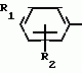 NH NH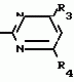 где R1 - водород или галоид; R2 - водород, галоид или метил; R3 - алкил (С1-С4), замещенный галоидом (С1-С4) алкил, циклопропил; R4 - циклопропил незамещенный или замещенный 1-3 раза галоидом или метилом, или их кислотно-аддитивных солей, заключающийся в том, что мочевину вводят во взаимодействие с дикетоном формулы II R3- где R1 - водород или галоид; R2 - водород, галоид или метил; R3 - алкил (С1-С4), замещенный галоидом (С1-С4) алкил, циклопропил; R4 - циклопропил незамещенный или замещенный 1-3 раза галоидом или метилом, или их кислотно-аддитивных солей, заключающийся в том, что мочевину вводят во взаимодействие с дикетоном формулы II R3- 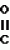 - CH2- - CH2- 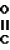 - R4 значения радикалов указаны выше, в присутствии кислоты в инертном растворителе при 20-140оС и после этого циклизуют при температуре кипения флегмы с образованием 2-гидроксипиримидина формулы III HO - R4 значения радикалов указаны выше, в присутствии кислоты в инертном растворителе при 20-140оС и после этого циклизуют при температуре кипения флегмы с образованием 2-гидроксипиримидина формулы III HO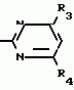 гидроксигруппу в полученном соединении в присутствии или отсутствии растворителя под действием избыточного количества РО(Наl)3 при температуре от 50 до 100оС заменяют галогеном и полученное соединение формулы IV Hal гидроксигруппу в полученном соединении в присутствии или отсутствии растворителя под действием избыточного количества РО(Наl)3 при температуре от 50 до 100оС заменяют галогеном и полученное соединение формулы IV Hal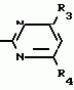 где R3 и R4 указаны выше; Наl - галоид, приводят во взаимодействие с производным анилина формулы V где R3 и R4 указаны выше; Наl - галоид, приводят во взаимодействие с производным анилина формулы V 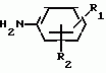 где R1 и R2 указаны выше, при 60-120оС в инертном растворителе, в присутствии или отсутствии кислоты и целевой продукт выделяют в свободном виде или в виде кислотно-аддитивных солей. П р и м е р 1. Получение 2-гидрокси-4-метил-6-циклопропилпиримидина. HO где R1 и R2 указаны выше, при 60-120оС в инертном растворителе, в присутствии или отсутствии кислоты и целевой продукт выделяют в свободном виде или в виде кислотно-аддитивных солей. П р и м е р 1. Получение 2-гидрокси-4-метил-6-циклопропилпиримидина. HO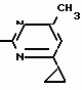 6 г (100 ммолей) мочевины и 12,6 г (100 ммолей) 1-циклопропил-1,3-бутадиона при комнатной температуре смешивают в 35 мл этанола с 15 мл концентрированной соляной кислоты. После 10-дневного стояния при комнатной температуре испаряют на роторном испарителе при температуре бани максимально 45оС. Остаток растворяют в 20 мл этанола, при этом очень быстро осаждается гидрохлорид реакционного продукта. При перемешивании добавляют 20 мл диэтилового эфира, выпавшие белые кристаллы отфильтровывают и промывают смесью этанола и диэтилового эфира и высушивают. В результате испарения фильтрата и перекристаллизации из смеси этанола и диэтилового эфира (1:2) получают дополнительное количество гидрохлорида. Выход гидрохлорида 12,6 г (65,7 ммолей), 67,5% от теории. П р и м е р 2. Получение 2-хлор-4-метил-6-циклопропилпиримидина (соед. 3.1). 6 г (100 ммолей) мочевины и 12,6 г (100 ммолей) 1-циклопропил-1,3-бутадиона при комнатной температуре смешивают в 35 мл этанола с 15 мл концентрированной соляной кислоты. После 10-дневного стояния при комнатной температуре испаряют на роторном испарителе при температуре бани максимально 45оС. Остаток растворяют в 20 мл этанола, при этом очень быстро осаждается гидрохлорид реакционного продукта. При перемешивании добавляют 20 мл диэтилового эфира, выпавшие белые кристаллы отфильтровывают и промывают смесью этанола и диэтилового эфира и высушивают. В результате испарения фильтрата и перекристаллизации из смеси этанола и диэтилового эфира (1:2) получают дополнительное количество гидрохлорида. Выход гидрохлорида 12,6 г (65,7 ммолей), 67,5% от теории. П р и м е р 2. Получение 2-хлор-4-метил-6-циклопропилпиримидина (соед. 3.1). 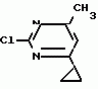 52,8 г (0,24 ммоля) гидрохлорида 2-гидрокси-4-метил-6-циклопропилпиримидина при перемешивании при комнатной температуре вносят в смесь 100 мл (1,1 ммоля) оксихлорида фосфора и 117 г (0,79 ммоля) диэтиленанилина, при этом температура поднимается до 63оС. После нагревания в течение 2 ч до 110оС охлаждают до комнатной температуры и реакционную смесь при перемешивании переносят в смесь воды со льдом и метиленхлорида. Органическую фазу отделяют и промывают до нейтральной реакции насыщенным водным раствором гидрокарбоната натрия. После испарения растворителя получают 116,4 г масла, которое состоит из продукта реакции и диэтиленанилина. Отделение диэтиленанилина и очистку сырого реакционного продукта осуществляют с помощью колончатой хроматографии через силикагель (гексан) диэтилацетат 3:1. Через несколько дней закристаллизовавшееся бесцветное масло имеет показатель преломления nD25 1,5418. Выход 35,7 г (0,21 ммол, 87,5 т теории). Т.пл. 33-34оС. П р и м е р 3. Получение 2-(м-фторфениламино)-4-метил-6-циклопропил-пиримидана. 52,8 г (0,24 ммоля) гидрохлорида 2-гидрокси-4-метил-6-циклопропилпиримидина при перемешивании при комнатной температуре вносят в смесь 100 мл (1,1 ммоля) оксихлорида фосфора и 117 г (0,79 ммоля) диэтиленанилина, при этом температура поднимается до 63оС. После нагревания в течение 2 ч до 110оС охлаждают до комнатной температуры и реакционную смесь при перемешивании переносят в смесь воды со льдом и метиленхлорида. Органическую фазу отделяют и промывают до нейтральной реакции насыщенным водным раствором гидрокарбоната натрия. После испарения растворителя получают 116,4 г масла, которое состоит из продукта реакции и диэтиленанилина. Отделение диэтиленанилина и очистку сырого реакционного продукта осуществляют с помощью колончатой хроматографии через силикагель (гексан) диэтилацетат 3:1. Через несколько дней закристаллизовавшееся бесцветное масло имеет показатель преломления nD25 1,5418. Выход 35,7 г (0,21 ммол, 87,5 т теории). Т.пл. 33-34оС. П р и м е р 3. Получение 2-(м-фторфениламино)-4-метил-6-циклопропил-пиримидана. 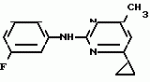 Раствор 5,5 г (50 ммолей) 3-фторанилина и 9,3 г (55 ммолей) 2-хлор-4-метил-6-циклопропил-пиримидана в 100 мл этанола при перемешивании добавлением 5 мл концентрированной соляной кислоты доводят до рН 1 и непосредственно после этого нагревают 18 ч до температуры кипения флегмы. После охлаждения до комнатной температуры коричневую эмульсию доводят до щелочной реакции добавлением 10 мл 30%-ного аммиака, выливают в 100 мл воды со льдом и дважды экстрагируют диэтиловым эфиром порциями по 150 мл. Соединенные экстракты промывают 50 мл воды, высушивают над сульфатом натрия, фильтруют и испаряют растворитель. Оставшиеся желтоватые кристаллы очищают перекристаллизацией из смеси диизопропиловый эфир (петролейный эфир). Т. кип. 50-70оС. Белые кристаллы плавятся при 87-89оС. Выход 8,3 г (34 ммоля, 68% от теории). П р и м е р 4. Получение 2-(4-фторфениламино)-4-метил-6-циклопропилпиримидина. F Раствор 5,5 г (50 ммолей) 3-фторанилина и 9,3 г (55 ммолей) 2-хлор-4-метил-6-циклопропил-пиримидана в 100 мл этанола при перемешивании добавлением 5 мл концентрированной соляной кислоты доводят до рН 1 и непосредственно после этого нагревают 18 ч до температуры кипения флегмы. После охлаждения до комнатной температуры коричневую эмульсию доводят до щелочной реакции добавлением 10 мл 30%-ного аммиака, выливают в 100 мл воды со льдом и дважды экстрагируют диэтиловым эфиром порциями по 150 мл. Соединенные экстракты промывают 50 мл воды, высушивают над сульфатом натрия, фильтруют и испаряют растворитель. Оставшиеся желтоватые кристаллы очищают перекристаллизацией из смеси диизопропиловый эфир (петролейный эфир). Т. кип. 50-70оС. Белые кристаллы плавятся при 87-89оС. Выход 8,3 г (34 ммоля, 68% от теории). П р и м е р 4. Получение 2-(4-фторфениламино)-4-метил-6-циклопропилпиримидина. F NH NH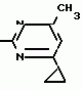 5 г (30 ммолей) 2-хлор-4-метил-6-циклопропилпиримидина растворяют в 50 мл абсолютированного метанола и при перемешивании при комнатной температуре смешивают с 3,3 г (30 ммолей) 4-фторанилина. При температуре масляной бани 85-90оС непосредственно после этого при перемешивании нагревают 19 ч при температуре кипения флегмы. После охлаждения в течение получаса прикапывают в 300 мл воды, которая содержит 1,2 г (30 ммолей) гидроокиси натрия. Очень скоро осаждаются бежевые кристаллы, которые отсасывают после перемешивания в течение последующего часа и промывают водой. После высушивания получают 6,8 г (28 ммолей) желтоватых кристаллов, которые плавятся при 89-91оС, выход 93,9% от теории. Таким же образом могут быть получены следующие соединения формулы 1. Получение 2-фениламино-4-метил-6-циклопропил-пиримидин-фосфата 5 г (30 ммолей) 2-хлор-4-метил-6-циклопропилпиримидина растворяют в 50 мл абсолютированного метанола и при перемешивании при комнатной температуре смешивают с 3,3 г (30 ммолей) 4-фторанилина. При температуре масляной бани 85-90оС непосредственно после этого при перемешивании нагревают 19 ч при температуре кипения флегмы. После охлаждения в течение получаса прикапывают в 300 мл воды, которая содержит 1,2 г (30 ммолей) гидроокиси натрия. Очень скоро осаждаются бежевые кристаллы, которые отсасывают после перемешивания в течение последующего часа и промывают водой. После высушивания получают 6,8 г (28 ммолей) желтоватых кристаллов, которые плавятся при 89-91оС, выход 93,9% от теории. Таким же образом могут быть получены следующие соединения формулы 1. Получение 2-фениламино-4-метил-6-циклопропил-пиримидин-фосфата  NH NH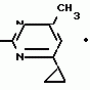 H3PO4 4 г (18 ммоль) 2-фенил-4-метил-6-циклопропил-пиримидина в 250 мл абсолютного диэтилового эфира при комнатной температуре, при быстром перемешивании и в течение 10 мин по каплям смешивают с 2,19 г (19 ммолей) 85%-ной р.а. ортофосфорной кислоты. Образующийся белый осадок отфильтровывают и дополнительно промывают 20 мл абсолютного диэтилового эфира. Кристаллы белого цвета плавятся при 188-191оС; выход: 5,6 г (17,3 ммоль=96% от теории). Получение 2-фениламино-4-метил-6-циклопропил-пиримидин-нитрата H3PO4 4 г (18 ммоль) 2-фенил-4-метил-6-циклопропил-пиримидина в 250 мл абсолютного диэтилового эфира при комнатной температуре, при быстром перемешивании и в течение 10 мин по каплям смешивают с 2,19 г (19 ммолей) 85%-ной р.а. ортофосфорной кислоты. Образующийся белый осадок отфильтровывают и дополнительно промывают 20 мл абсолютного диэтилового эфира. Кристаллы белого цвета плавятся при 188-191оС; выход: 5,6 г (17,3 ммоль=96% от теории). Получение 2-фениламино-4-метил-6-циклопропил-пиримидин-нитрата 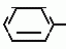 NH NH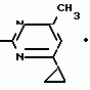 HNO3 12 г (53 ммоль) 2-фениламино-4-метил-6-циклопропил-пиримидина в 180 мл абсолютного диэтилового эфира при комнатной температуре и быстром перемешивании, в течение 20 мин по каплям смешивают с 5,81 г (60 ммолей) р.а. 65% -ной азотной кислоты. Тотчас образующийся белый осадок отфильтровывают и дополнительно промывают 20 мл абсолютного диэтилового эфира. Белого цвета, слабо-бежеватые кристаллы плавятся при 151-153оС с разложением, выход 14,7 г (52 ммолей, 96% от теории). Аналогично осуществленным в примерах способам дополнительно получают следующие соли: HNO3 12 г (53 ммоль) 2-фениламино-4-метил-6-циклопропил-пиримидина в 180 мл абсолютного диэтилового эфира при комнатной температуре и быстром перемешивании, в течение 20 мин по каплям смешивают с 5,81 г (60 ммолей) р.а. 65% -ной азотной кислоты. Тотчас образующийся белый осадок отфильтровывают и дополнительно промывают 20 мл абсолютного диэтилового эфира. Белого цвета, слабо-бежеватые кристаллы плавятся при 151-153оС с разложением, выход 14,7 г (52 ммолей, 96% от теории). Аналогично осуществленным в примерах способам дополнительно получают следующие соли: 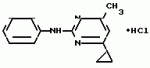 Т.пл. 151-154оС Т.пл. 151-154оС 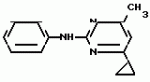 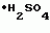 Т.пл. 183-185оС Т.пл. 183-185оС  NH NH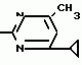 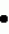 1/2 H2SO4 Т.пл. 200-202оС Подтверждение активности солей соединений формулы 1 1. Соли-соединения: А) 1/2 H2SO4 Т.пл. 200-202оС Подтверждение активности солей соединений формулы 1 1. Соли-соединения: А) 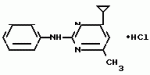 В) В) 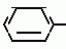 NH NH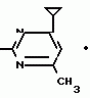 H2SO4 С) H2SO4 С)  NH NH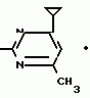 1/2 H2SO4 D) 1/2 H2SO4 D) 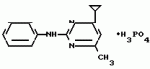 2. Опыты. 2.1. Действие против Botrytis cinerea на яблоках. Искусственно поврежденные яблоки обрабатывают тем, что капают на места повреждения приготовленный из смачивающегося порошка активного вещества бульон для опрыскивания (0,02, 0,006, 0,002, 0,0006 активного вещества). Обработанные плоды затем инокулируют суспензией спор гриба и в течение недели инкубируют при высокой влажности воздуха примерно при 20оС. При оценке подсчитывают подгнившие места повреждений и из этого делают вывод о фунгицидном действии испытуемого вещества. Соединения по изобретению (см. табл. 1) снизили поражение Botrytis до 0-10%. Сравнительным образом необработанные, но инфицированные контрольные растения показывают поражение Botrytis=100%. 2.2. Действие против Venturia inaegualis на яблоневых побегах. Яблоневые черенки со свежими побегами длиной 10-20 см опрыскивают приготовленным из смачивающегося порошка биологически активного вещества бульоном для опрыскивания (0,02, 0,006, 0,002, 0,0006% активного вещества). Спустя 24 ч обработанные растения инфицируют суспензией конидий гриба. Растения затем инкубируют в течение 5 дней при относительной влажности воздуха 90-100% и в течение следующих 10 дней выдерживают в теплице при 20-24оС. Поражение паршой оценивают спустя 15 дней после инфекции. Сравнительным образом необработанные, однако инфицированные контрольные растения показывают поражение Venturia=100%. Соединения по изобретению сокращают поражение на 0-10%. 3. Оценочная шкала: Оценка % активности 1 95 (Полное действие) 3 80-95 (Акцетуемое действие) 6 50-80 (недостаточное действие) 9 50 (никакого действия) Оценки с промежуточными значениями представляют собой средние значения результатов многих опытов. Результаты приведены в табл. 1. Отчет об испытании. Сравнение активности биологически активных веществ по изобретению с таковых из уровня техники. 1. Соединения по изобретению. Х1 2. Опыты. 2.1. Действие против Botrytis cinerea на яблоках. Искусственно поврежденные яблоки обрабатывают тем, что капают на места повреждения приготовленный из смачивающегося порошка активного вещества бульон для опрыскивания (0,02, 0,006, 0,002, 0,0006 активного вещества). Обработанные плоды затем инокулируют суспензией спор гриба и в течение недели инкубируют при высокой влажности воздуха примерно при 20оС. При оценке подсчитывают подгнившие места повреждений и из этого делают вывод о фунгицидном действии испытуемого вещества. Соединения по изобретению (см. табл. 1) снизили поражение Botrytis до 0-10%. Сравнительным образом необработанные, но инфицированные контрольные растения показывают поражение Botrytis=100%. 2.2. Действие против Venturia inaegualis на яблоневых побегах. Яблоневые черенки со свежими побегами длиной 10-20 см опрыскивают приготовленным из смачивающегося порошка биологически активного вещества бульоном для опрыскивания (0,02, 0,006, 0,002, 0,0006% активного вещества). Спустя 24 ч обработанные растения инфицируют суспензией конидий гриба. Растения затем инкубируют в течение 5 дней при относительной влажности воздуха 90-100% и в течение следующих 10 дней выдерживают в теплице при 20-24оС. Поражение паршой оценивают спустя 15 дней после инфекции. Сравнительным образом необработанные, однако инфицированные контрольные растения показывают поражение Venturia=100%. Соединения по изобретению сокращают поражение на 0-10%. 3. Оценочная шкала: Оценка % активности 1 95 (Полное действие) 3 80-95 (Акцетуемое действие) 6 50-80 (недостаточное действие) 9 50 (никакого действия) Оценки с промежуточными значениями представляют собой средние значения результатов многих опытов. Результаты приведены в табл. 1. Отчет об испытании. Сравнение активности биологически активных веществ по изобретению с таковых из уровня техники. 1. Соединения по изобретению. Х1  NH NH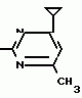 Х2 Х2 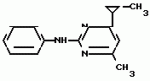 Х3 Х3 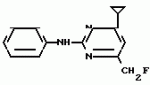 X4 X4 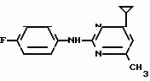 Х5 Х5 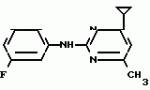 Y1 Y1 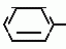 NH NH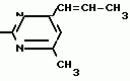 Y2 Y2 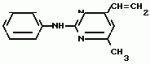 Соединения Y1 и Y2 известны, описаны ранее. 2. Осуществление опытов. 2.1. Действие против Botrytis cinerae на яблоках. Искусственно поврежденные яблоки обрабатывают тем, что на места повреждения капают приготовленный из смачивающегося порошка активного вещества бульон для опрыскивания (0,002% активного вещества). Обработанные плоды затем инокулируют суспензией спор гриба и инкубируют в течение недели при высокой влажности воздуха и примерно при 20оС. При оценке подсчитывают подгнившие места повреждения и из этого делают вывод о фунгицидном действии испытуемого вещества. Все соединения показали хорошую эффективность (поражение менее 20%). Сравнительным образом необработанные, но инфицированные контрольные растения показывают поражение Botrytis=100%. 2.2. Действие против Venturia inaegualu на яблоневых побегах. Яблоневые черенки со свежими побегами длиной 10-20 см опрыскивают приготовленным из смачивающегося порошка биологически активного вещества бульоном для опрыскивания (0,006% активного вещества). Спустя 24 ч обработанные растения инфицируют суспензией конидий гриба. Растения затем инкубируют в течение 5 дней при относительной влажности воздуха 90-100% и в течение 10 следующих дней выдерживают в теплице при 20-24оС. Поражение паршой оценивают спустя 15 дней после инфекции. Сравнительным образом необработанные, но инфицированные контрольные растения показывают поражение Venturia=100%. 2.3. Действие против Erysiphae graminis на ячмене. Высотой примерно 8 см растения ячменя опрыскивают приготовленным из смачивающегося порошка активного вещества бульоном для опрыскивания (0,006% активного вещества). Спустя 3-4 ч обработанные растения опыливают конидиями гриба. Инфицированные растения ячменя выдерживают в теплице примерно при 22оС и оценивают поражение грибом спустя 10 дней. Соединения табл. 1 показали по отношению к Erysiphae graminis хорошую эффективность (поражение менее 20%). Сравнительным образом необработанные, но инфицированные контрольные растения показывают поражение Erysiphae=100%. 3. Оценочная шкала Оценка % активности 1 95 (Полное действие) 3 80-95 (Акцептуемое действие) 6 50-80 (Недостаточное действие) 9 50 (Никакого действия). Оценки с промежуточными значениями представляют собой средние значения результатов многих опытов. 4. Результаты приведены в табл. 2. Соединения табл. 7 показали по отношению к Botrytis хорошую эффективность (поражение менее 20% ). Так, например, соединения N 1.1, 1.4, 1.6, 1.9, 1.12, 1.13, 1.16, 1.21, 1.32, 1.23, 1.29, 1.35, 1.36, 1.37, 1.38, 1.40, 1.42, 1.45, 1.46, 1.50а, 1.52, 1.55, 1.51, 1.59, 1.64, 1.66, 1.68, 1.69, 1.71, 1.72, 1.77, 1.81, 1.92, 1.93, 1.94 снизили поражение Botrytis до 0-10%. Необработанные зараженные контрольные растения были поражены Botrytis на 100%. П р и м е р 3.3. Действие против Erysiphae graminis на ячмене. а) Резидуально-протективное действие. Растения ячменя высотой около 8 см были опрысканы бульоном для разбрызгивания, приготовленным из смачивающегося порошка биологически активного вещества (0,006% активного вещества). Через 3-4 ч обработанные растения были опылены спорами гриба. Зараженные растения ячменя помещали в теплицу при температуре около 22оС и оценивали поражение грибом через 10 дней. Соединения табл. 4 показали по отношению к Erysiphae хорошую эффективность (поражение менее 20%). Так, соединения 1.1, 1.6, 1.12, 1.13, 1.33, 1.35, 1.29, 1.36, 1.37, 1.38, 1.40, 1.46, 1.50, 1.52, 1.51, 1,64, 1.77, 1.86 и 1.87 снизили поражение Erysiphae до 0-10%. Необработанные зараженные контрольные растения показали, напротив, поражение 100%. П р и м е р 2.4. Действие против Helwinthosporium gramineam. Зерна пшеницы пропитывали суспензией спор гриба и снова высушивали. Пропитанные зерна протравливали полученной из смачивающегося порошка суспензией испытываемого вещества (600 млн-1 активного вещества, считая на массу семян). Через два дня зерна помещали на соответствующие агарные тарелки и через четыре дня оценивали развитие колонии гриба вокруг зерна. Количество и величина колоний гриба служили для оценки испытываемого вещества. Соединения таблицы сильно препятствуют поражению грибом (0-10% поражения). П р и м е р 2.5. Действие против Colletotrichum lagenarium на огурцах. Растения огурцов после прорастания в течение 2 недель опрыскивали бульоном для опрыскивания, приготовленными из смачивающегося порошка биологически активного вещества (концентрация 0,002%). Через 2 дня растения заражали суспензией спор (1,5х105 спор/мл) гриба и инкубировали 36 ч при 23оС и высокой влажности воздуха. Инкубацию продолжали затем при нормальной влажности воздуха и температуре около 22-23оС. Поражения грибом оценивали через 8 дней после заражения. Необработанные, но зараженные контрольные растения были поражены грибом на 100%. Соединения из табл. 4 показали хорошую эффективность и предотвратили широкое поражение болезнью. Поражение грибом было снижено до 20% или менее. П р и м е р 2.6. а) Контактное действие против Nephotettix cineticeps и Nilaparvate lugens (Nymphen) Тест проводили на проросших растениях риса. Для этого высаживали в горшки (диаметр 5,5 см) соответственно по 4 растения (14-20 дней) высотой около 15 см. Растения опрыскивали на вращающейся тарелке 100 мл готовой водной суспензии, содержащей 400 млн-1 соответствующего биологически активного вещества. После высыхания разбрызганного слоя на каждое растение сажали по 40 нимф (личинок) испытуемых животных на третьей стадии развития. Чтобы препятствовать распространению цикад, растения с личинками окружали открытым с обеих сторон цилиндром и его накрывали металлической сеткой. Через 6 дней нимфы достигали стадия развития взрослых особей на обработанных растениях. Оценку уничтожения в процентах осуществляли через 6 дней после высаживания нимф. Опыт проводили приблизительно при 27оС, 60% относительной влажности воздуха и периоде освещенности 16 ч. б) Системное действие против Nilaparvate lugeus (вода). Растения риса приблизительно 10-дневного возраста (высота 10 см) помещали в пластиковые стаканы, которые содержали готовые водные эмульсии подлежащего испытанию биологически активного вещества с концентрацией 100 млн-1 и были закрыты пластиковой крышкой с дыркой. Корень растения риса через дыру в пластиковой крышке помещали в готовый испытуемый раствор. Затем на растения риса сажали на 20 нимф (личинок Nilaparvate lugens на стадии развития N2 и N3) и закрывали пластиковым цилиндром. Опыт проводили приблизительно при 26оС и 60% относительной влажности воздуха с периодом освещенности 16 ч. Через пять дней оценивали уничтоженных испытуемых животных по сравнению с необработанными контрольными. Таким образом было установлено, что биологически активное вещество, поступающее через корень, поражает испытуемых животных на верхних частях растений. Соединения из табл. 4 показали как в тесте а), так и в тесте б) сильное уничтожающее действие по отношению к вредителям риса. Степень уничтожения составляет 80% и более. С помощью соединений N 1.1, 1.6, 1.13, 1.36, 1.38, 1.50, 1.52 и 1.77 было достигнуто почти полное уничтожение (98-100%). Данные по токсичности, подтверждающие, что полученные соединения являются слаботоксичными, приведены в табл. 3. Токсичность на теплокровных соединений по изобретению Летальная доза 50% (ЛД50) Проведенные испытания показали, что соединения формулы 1 обладают очень благоприятным для практического использования биоцидным спектром для борьбы с насекомыми и фитопатогенными микроорганизмами, в частности грибами. Они обладают очень выгодными куративными, превентивными и, в частности, системными свойствами и могут быть использованы для защиты многих культурных растений. С помощью биологически активных веществ формулы I у растений или отдельных частей растений (фрукты, цветы, листья, стебель, клубни, корни) различных полезных культур можно ограничить или уничтожить появляющиеся повреждения, причем даже позднее выросшие части растений остаются защищенными, например, от фитопатогенных микроорганизмов. Соединения формулы 1 обладают биологической активностью против следующих классов фитопатогенных грибов: Fungi imperfecti (insbesondere Botrytis, Jerner Pycularia, Helminthos porium, Fusorium, septoria, Cercospora und Alternaria, Basidiomyceten (Z.B. Rhizootonia, Hemileia, Puccima). Кроме того, они действуют против класса аскомицетов (например, Z.B. Ventura und Erysiphe, Podoophaera, monilinia uncimula Plasmopara) и оомицетов (например, Z.B. Phitophthora, Pythim). Проведенные испытания показали, что соединения по изобретению со всеми характерными заместителями проявляют более высокую фунгицидную активность, чем известные соединения - аналоги. Кроме того, они малотоксичны и обладают инсектицидными свойствами. Соединения Y1 и Y2 известны, описаны ранее. 2. Осуществление опытов. 2.1. Действие против Botrytis cinerae на яблоках. Искусственно поврежденные яблоки обрабатывают тем, что на места повреждения капают приготовленный из смачивающегося порошка активного вещества бульон для опрыскивания (0,002% активного вещества). Обработанные плоды затем инокулируют суспензией спор гриба и инкубируют в течение недели при высокой влажности воздуха и примерно при 20оС. При оценке подсчитывают подгнившие места повреждения и из этого делают вывод о фунгицидном действии испытуемого вещества. Все соединения показали хорошую эффективность (поражение менее 20%). Сравнительным образом необработанные, но инфицированные контрольные растения показывают поражение Botrytis=100%. 2.2. Действие против Venturia inaegualu на яблоневых побегах. Яблоневые черенки со свежими побегами длиной 10-20 см опрыскивают приготовленным из смачивающегося порошка биологически активного вещества бульоном для опрыскивания (0,006% активного вещества). Спустя 24 ч обработанные растения инфицируют суспензией конидий гриба. Растения затем инкубируют в течение 5 дней при относительной влажности воздуха 90-100% и в течение 10 следующих дней выдерживают в теплице при 20-24оС. Поражение паршой оценивают спустя 15 дней после инфекции. Сравнительным образом необработанные, но инфицированные контрольные растения показывают поражение Venturia=100%. 2.3. Действие против Erysiphae graminis на ячмене. Высотой примерно 8 см растения ячменя опрыскивают приготовленным из смачивающегося порошка активного вещества бульоном для опрыскивания (0,006% активного вещества). Спустя 3-4 ч обработанные растения опыливают конидиями гриба. Инфицированные растения ячменя выдерживают в теплице примерно при 22оС и оценивают поражение грибом спустя 10 дней. Соединения табл. 1 показали по отношению к Erysiphae graminis хорошую эффективность (поражение менее 20%). Сравнительным образом необработанные, но инфицированные контрольные растения показывают поражение Erysiphae=100%. 3. Оценочная шкала Оценка % активности 1 95 (Полное действие) 3 80-95 (Акцептуемое действие) 6 50-80 (Недостаточное действие) 9 50 (Никакого действия). Оценки с промежуточными значениями представляют собой средние значения результатов многих опытов. 4. Результаты приведены в табл. 2. Соединения табл. 7 показали по отношению к Botrytis хорошую эффективность (поражение менее 20% ). Так, например, соединения N 1.1, 1.4, 1.6, 1.9, 1.12, 1.13, 1.16, 1.21, 1.32, 1.23, 1.29, 1.35, 1.36, 1.37, 1.38, 1.40, 1.42, 1.45, 1.46, 1.50а, 1.52, 1.55, 1.51, 1.59, 1.64, 1.66, 1.68, 1.69, 1.71, 1.72, 1.77, 1.81, 1.92, 1.93, 1.94 снизили поражение Botrytis до 0-10%. Необработанные зараженные контрольные растения были поражены Botrytis на 100%. П р и м е р 3.3. Действие против Erysiphae graminis на ячмене. а) Резидуально-протективное действие. Растения ячменя высотой около 8 см были опрысканы бульоном для разбрызгивания, приготовленным из смачивающегося порошка биологически активного вещества (0,006% активного вещества). Через 3-4 ч обработанные растения были опылены спорами гриба. Зараженные растения ячменя помещали в теплицу при температуре около 22оС и оценивали поражение грибом через 10 дней. Соединения табл. 4 показали по отношению к Erysiphae хорошую эффективность (поражение менее 20%). Так, соединения 1.1, 1.6, 1.12, 1.13, 1.33, 1.35, 1.29, 1.36, 1.37, 1.38, 1.40, 1.46, 1.50, 1.52, 1.51, 1,64, 1.77, 1.86 и 1.87 снизили поражение Erysiphae до 0-10%. Необработанные зараженные контрольные растения показали, напротив, поражение 100%. П р и м е р 2.4. Действие против Helwinthosporium gramineam. Зерна пшеницы пропитывали суспензией спор гриба и снова высушивали. Пропитанные зерна протравливали полученной из смачивающегося порошка суспензией испытываемого вещества (600 млн-1 активного вещества, считая на массу семян). Через два дня зерна помещали на соответствующие агарные тарелки и через четыре дня оценивали развитие колонии гриба вокруг зерна. Количество и величина колоний гриба служили для оценки испытываемого вещества. Соединения таблицы сильно препятствуют поражению грибом (0-10% поражения). П р и м е р 2.5. Действие против Colletotrichum lagenarium на огурцах. Растения огурцов после прорастания в течение 2 недель опрыскивали бульоном для опрыскивания, приготовленными из смачивающегося порошка биологически активного вещества (концентрация 0,002%). Через 2 дня растения заражали суспензией спор (1,5х105 спор/мл) гриба и инкубировали 36 ч при 23оС и высокой влажности воздуха. Инкубацию продолжали затем при нормальной влажности воздуха и температуре около 22-23оС. Поражения грибом оценивали через 8 дней после заражения. Необработанные, но зараженные контрольные растения были поражены грибом на 100%. Соединения из табл. 4 показали хорошую эффективность и предотвратили широкое поражение болезнью. Поражение грибом было снижено до 20% или менее. П р и м е р 2.6. а) Контактное действие против Nephotettix cineticeps и Nilaparvate lugens (Nymphen) Тест проводили на проросших растениях риса. Для этого высаживали в горшки (диаметр 5,5 см) соответственно по 4 растения (14-20 дней) высотой около 15 см. Растения опрыскивали на вращающейся тарелке 100 мл готовой водной суспензии, содержащей 400 млн-1 соответствующего биологически активного вещества. После высыхания разбрызганного слоя на каждое растение сажали по 40 нимф (личинок) испытуемых животных на третьей стадии развития. Чтобы препятствовать распространению цикад, растения с личинками окружали открытым с обеих сторон цилиндром и его накрывали металлической сеткой. Через 6 дней нимфы достигали стадия развития взрослых особей на обработанных растениях. Оценку уничтожения в процентах осуществляли через 6 дней после высаживания нимф. Опыт проводили приблизительно при 27оС, 60% относительной влажности воздуха и периоде освещенности 16 ч. б) Системное действие против Nilaparvate lugeus (вода). Растения риса приблизительно 10-дневного возраста (высота 10 см) помещали в пластиковые стаканы, которые содержали готовые водные эмульсии подлежащего испытанию биологически активного вещества с концентрацией 100 млн-1 и были закрыты пластиковой крышкой с дыркой. Корень растения риса через дыру в пластиковой крышке помещали в готовый испытуемый раствор. Затем на растения риса сажали на 20 нимф (личинок Nilaparvate lugens на стадии развития N2 и N3) и закрывали пластиковым цилиндром. Опыт проводили приблизительно при 26оС и 60% относительной влажности воздуха с периодом освещенности 16 ч. Через пять дней оценивали уничтоженных испытуемых животных по сравнению с необработанными контрольными. Таким образом было установлено, что биологически активное вещество, поступающее через корень, поражает испытуемых животных на верхних частях растений. Соединения из табл. 4 показали как в тесте а), так и в тесте б) сильное уничтожающее действие по отношению к вредителям риса. Степень уничтожения составляет 80% и более. С помощью соединений N 1.1, 1.6, 1.13, 1.36, 1.38, 1.50, 1.52 и 1.77 было достигнуто почти полное уничтожение (98-100%). Данные по токсичности, подтверждающие, что полученные соединения являются слаботоксичными, приведены в табл. 3. Токсичность на теплокровных соединений по изобретению Летальная доза 50% (ЛД50) Проведенные испытания показали, что соединения формулы 1 обладают очень благоприятным для практического использования биоцидным спектром для борьбы с насекомыми и фитопатогенными микроорганизмами, в частности грибами. Они обладают очень выгодными куративными, превентивными и, в частности, системными свойствами и могут быть использованы для защиты многих культурных растений. С помощью биологически активных веществ формулы I у растений или отдельных частей растений (фрукты, цветы, листья, стебель, клубни, корни) различных полезных культур можно ограничить или уничтожить появляющиеся повреждения, причем даже позднее выросшие части растений остаются защищенными, например, от фитопатогенных микроорганизмов. Соединения формулы 1 обладают биологической активностью против следующих классов фитопатогенных грибов: Fungi imperfecti (insbesondere Botrytis, Jerner Pycularia, Helminthos porium, Fusorium, septoria, Cercospora und Alternaria, Basidiomyceten (Z.B. Rhizootonia, Hemileia, Puccima). Кроме того, они действуют против класса аскомицетов (например, Z.B. Ventura und Erysiphe, Podoophaera, monilinia uncimula Plasmopara) и оомицетов (например, Z.B. Phitophthora, Pythim). Проведенные испытания показали, что соединения по изобретению со всеми характерными заместителями проявляют более высокую фунгицидную активность, чем известные соединения - аналоги. Кроме того, они малотоксичны и обладают инсектицидными свойствами.
Формула изобретенияСпособ получения производных 2-анилинопиримидина общей формулы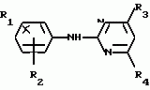 где R1 - водород или галоид; R2 - водород, галоид или метил; R3-(C1-C4)-алкил, замещенный галоидом C1 - C4-алкил, циклопропил; R4 - циклопропил, незамещенный или 1 - 3 раза замещенный галоидом или метилом, или их кислотно-аддитивных солей, отличающийся тем, что мочевину вводят во взаимодействия с дикетоном общей формулы R3- где R1 - водород или галоид; R2 - водород, галоид или метил; R3-(C1-C4)-алкил, замещенный галоидом C1 - C4-алкил, циклопропил; R4 - циклопропил, незамещенный или 1 - 3 раза замещенный галоидом или метилом, или их кислотно-аддитивных солей, отличающийся тем, что мочевину вводят во взаимодействия с дикетоном общей формулы R3-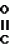 -CH2- -CH2-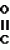 -R4 где R3 и R4 имеют указанные значения, в присутствии кислоты в инертном растворителе при 20 - 140oС и после этого циклизуют при температуре кипения флегмы с образованием 2-гидроксипиримидина общей формулы -R4 где R3 и R4 имеют указанные значения, в присутствии кислоты в инертном растворителе при 20 - 140oС и после этого циклизуют при температуре кипения флегмы с образованием 2-гидроксипиримидина общей формулы 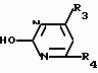 где R3 и R4 имеют указанные значения, гидроксигруппу в полученном соединении в присутствии или отсутствии растворителя под действием избыточного количества PO(Hal)3 при 50 - 100oС заменяют галогеном и полученное соединение общей формулы где R3 и R4 имеют указанные значения, гидроксигруппу в полученном соединении в присутствии или отсутствии растворителя под действием избыточного количества PO(Hal)3 при 50 - 100oС заменяют галогеном и полученное соединение общей формулы 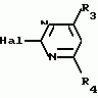 где R3 и R4 имеют указанные значения; Hal - галоид, приводят во взаимодействие с производным анилина общей формулы где R3 и R4 имеют указанные значения; Hal - галоид, приводят во взаимодействие с производным анилина общей формулы 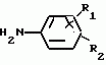 где R1 и R2 имеют указанные значения, при 60 - 120oС в инертном растворителе в присутствии или отсутствии кислоты, и целевой продукт выделяют в свободном виде или в виде кислотно-аддитивных солей. Приоритет по признакам: 28.09.87 при R3 - C1-C4-алкил, незамещенный или замещенный галоидом. 11.04.88 при R3 - циклопропил, незамещенный или замещенный метилом. где R1 и R2 имеют указанные значения, при 60 - 120oС в инертном растворителе в присутствии или отсутствии кислоты, и целевой продукт выделяют в свободном виде или в виде кислотно-аддитивных солей. Приоритет по признакам: 28.09.87 при R3 - C1-C4-алкил, незамещенный или замещенный галоидом. 11.04.88 при R3 - циклопропил, незамещенный или замещенный метилом.
PD4A - Изменение наименования обладателя патента Российской Федерации на изобретение Номер и год публикации бюллетеня: 7-1998 (73) Новое наименование патентообладателя: Новартис АГ (CH) Извещение опубликовано: 10.03.1998 MM4A Досрочное прекращение действия патента Российской Федерации на изобретение из-за неуплаты в установленный срок пошлины за поддержание патента в силе Дата прекращения действия патента: 25.01.1998 Номер и год публикации бюллетеня: 20-1999 Извещение опубликовано: 20.07.1999 Популярные патенты: 2473211 Приспособление для автоматической дойки молочного скота ... или проводное соединение к центральному процессору или компьютеру (см. также далее).Средства управления датчиком трехмерной камеры 100 определяют расстояние от объекта до каждого из фотодиодов путем измерения разницы фаз между светом, излучаемым инфракрасным светодиодом 108 трехмерной камеры 100 на объект, светом, возвращенным после отражения к трехмерной камере 100, т.е. к ее датчику изображения КМОП 110.В предпочтительном воплощении, инфракрасный светодиод 108 издает амплитудно-модулированный световой сигнал в волновой форме. Амплитудная модуляция сама имеет частоту повторяемости. После отражения этот световой сигнал отображается при помощи линзы 106 на датчике изображения ... 2471341 Стойло, устройство в стойле и способ монтажа указанного устройства ... в предназначенную для этого зону снаружи стойла. Пол в помещении для животных обычно делают из бетона, который является тяжелым и во время холодных дней очень некомфортабельным для животного для отдыха на нем. Было проверено, что коровы, живущие в комфортабельных окружающих условиях, производят больше молока. Пол в стойле, вследствие этого, часто застилают матом для животного для того, чтобы уменьшить ощущение холода при лежании на полу и обеспечить более комфортабельные окружающие условия для животного. Различные типы матов для животных для использования на полу в стойле раскрыты в EP 0 684 760 B1.Известные подгрудные доски и маты являются, однако, затратными по времени для ... 2192734 Устройство для производства прессованных кип из корней лекарственных растений ... части 38 вверх вдоль направляющих 2 и 3 происходит до тех пор, пока нижнее кольцо 42 средней части 38 не коснется верхнего кольца 43 нижней недвижной части 39. Рабочий объем камеры прессования увеличился более чем в три раза. Эти положения камеры прессования изображены на фиг.3 и 6. Повторяют догрузку сырьем полости камеры прессования 7. При завершении уплотнения сырья под рабочим давлением 20 МПа, оператор нижнюю часть 39, среднюю часть 38 и верхнюю часть 37 приводит в положения для обвязки и упаковки спрессованной кипы (см. фиг.7). После перемещения частей 37-39 камеры прессования 7 спрессованная кипа осталась в сжатом положении между нижней матрицей 5 и верхней подвижной ... 2106081 Животноводческая ферма с применением помещений круглой формы и способ содержания в ней, например, крупного рогатого скота ... в стойловых условиях производится только на выгульном дворе. Эту операцию осуществляет только агрегат для сбора навоза с поверхности пола. Вот по этой причине агрегат для сбора навоза загружается подстилкой только перед уборкой навоза и раскладки подстилки, в процессе которой он освобождается от подстилочного материала. Его основное положение - иметь емкость пустой. По этой причине конструкция зачищающего ножа, его шарнирная подвеска на раме агрегата предусматривает два положения: рабочее положение, когда он производит зачистку частиц корма, не захваченных скребками штангового транспортера, и нерабочее положение, когда он повернут в горизонтальное положение, поднят над ... 2485755 Способ выращивания посадочного материала ... условиях (в условиях ламинар-бокса) 0,025% раствором мертиолята в сочетании с жидким дезинфицирующим раствором "Белизна" (7% раствор) в течение 15 мин, с последующей 5-кратной промывкой стерильной дистиллированной водой. Для лучшего смачивания побегов во время основной стерилизации в раствор мертиолята рекомендуется добавить Твин 20 (0,08 0,12%).2 этап - Индукция развития основного пазушного побега на первичных эксплантах.Простерилизованные побеги разрезают в асептических условиях на сегменты величиной 1,5-2 см с одной пазушной почкой (культуральные экспланты). Экспланты в асептических условиях (в ламинар-боксе) помещают в вертикальном или слегка наклонном положении по ... |
Еще из этого раздела: 2157068 Способ управления роением в пчеловодческом хозяйстве 2204241 Способ определения поливных норм при капельном орошении томатов 2195801 Картофелекопатель швыряльного типа 2121252 Агротранспортная система 2216923 Способ выращивания льна-долгунца 2474105 Плодосъемник шолина 2400069 Способ защиты материалов от микробного разрушения 2062564 Способ оценки устойчивости растений к засухе северного и южного типа на ранних этапах онтогенеза 2437864 Способ микробиологической переработки птичьего помета 2452165 Высевающий аппарат зерновой сеялки с централизованным дозированием семян |
Изобретения в сельском хозяйстве
Обработка почвы в сельском и лесном хозяйствах
Посадка, посев, удобрение
Уборка урожая, жатва
Обработка и хранение продуктов полеводства и садоводства
Садоводство, разведение овощей, цветов, риса, фруктов, винограда, лесное хозяйство
Новые виды растений или способы их выращивания
Производство молочных продуктов
Животноводство, разведение и содержание птицы, рыбы, насекомых, рыбоводство, рыболовство
Поимка, отлов или отпугивание животных
Консервирование туш животных, или растений или их частей
Биоцидная, репеллентная, аттрактантная или регулирующая рост растений активность химических соединений или препаратов
Хлебопекарные печи, машины и прочее оборудование для хлебопечения
Машины или оборудование для приготовления или обработки теста
Обработка муки или теста для выпечки, способы выпечки, мучные изделия
|
|
||