Производные имидазолаПатент на изобретение №: 2014326 Автор: Рикуо Насу[JP], Казуми Сузуки[JP], Тосио Накадзима[JP], Кейитиро Ито[JP], Такеси Осима[JP], Хидеси Есимура[JP], Терумаса Комиедзи[JP] Патентообладатель: Исихара Сангио Кайся Лтд. (JP) Дата публикации: 15 Июня, 1994 Адрес для переписки: подача заявки30.07.1992 публикация патента15.06.1994 Изображения    Использование: в качестве фунгицида. Сущность изобретения: соединение ф - лы, где R1-CN - СN или CSNHR5 ; R5-H - Н, ацетил или пропионил; R2-H - Н, циклопропил, циклогексил, 2 - нафтил, алкил C1-C8 , C12 , 3-фторпропил, 3 - хлорпропил, 4 - хлорбутил, 5 - хлорпентил, гидроксипропил, гидроксибутил, метоксиметил, этоксиметил, фенетил, 1,2-дифенилэтил, 2, 2, 2-трифторэтокси, бензил, L - гидроксибензил, метилбензил, 2-фторбензил, аллил, 2 - бутенил, фенил, хлорфенил, фторфенил, 4 - бромфенил, 2,3-дихлорфенил, 3,4 - дихлорфенил, 4 - метилфенил, 3 - метилфенил, 2-метилфенил, 4-этилфенил, 4-изопропенилфенил, 4-трет-бутилфенил, 3,4-диметилфенил, 4-метоксифенил, 4-этоксифенил, 4-метил - 3 - хлорфенил, 4-метокси-3-хлорфенил, 3-метил-4-метоксифенил, 3,4-метилендиоксифенил, 4-(2  , 2 , 2 , 2 , 2 ) - трифторэтокси)фенил, 4-цианофенил, 4-нитрофенил, 2-фурил, 5-метил-2-фурил, 2-тиенил, 5-хлор-2-тиенил, 5-бром-2-тиенил, SOnR6 , R6-C1-C4 - алкил, аллил, фенил, бензил, 3-трифторметил-2-пиридил, 4-хлорфенил при n - 0; R6 - диметиламино, этил при n - 2 CONHR; R7 - фенил, 4 - хлорфенил, R3 - H, Cl, Br, I, циано, нитро, метил, этил, метилтио, фенилтио, 2 - фурил, трифторацетил, R4 - изопропил, диметиламино, диэтиламино, морфолино. Ф - ла 1: ) - трифторэтокси)фенил, 4-цианофенил, 4-нитрофенил, 2-фурил, 5-метил-2-фурил, 2-тиенил, 5-хлор-2-тиенил, 5-бром-2-тиенил, SOnR6 , R6-C1-C4 - алкил, аллил, фенил, бензил, 3-трифторметил-2-пиридил, 4-хлорфенил при n - 0; R6 - диметиламино, этил при n - 2 CONHR; R7 - фенил, 4 - хлорфенил, R3 - H, Cl, Br, I, циано, нитро, метил, этил, метилтио, фенилтио, 2 - фурил, трифторацетил, R4 - изопропил, диметиламино, диэтиламино, морфолино. Ф - ла 1: 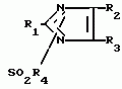 , , , , , , , , , , , , , , ,
, , , , , , , , , , , , , , , ОПИСАНИЕ ИЗОБРЕТЕНИЯ К ПАТЕНТУИзобретение относится к соединениям имидазола. Известно фунгицидное средство, использующее в качества действующего начала соединение формулы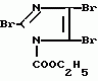 Однако оно недостаточно эффективно. Известно фунгицидное средство на основе соединения формулы NH Однако оно недостаточно эффективно. Известно фунгицидное средство на основе соединения формулы NH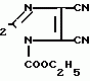 Однако оно также недостаточно эффективно при низких концентрациях. Заявленные соединения имидазола обладают усиленной фунгицидной активности. Производное имидазола имеет общую формулу I Однако оно также недостаточно эффективно при низких концентрациях. Заявленные соединения имидазола обладают усиленной фунгицидной активности. Производное имидазола имеет общую формулу I  где R1 - CN или CSNHR5; R5 - водород, ацетил, или пропионил, R2 - водород, циклопропил, циклогексил, 2-нафтил, алкил С1-С8, С12, 3-фторпропил, 3-хлорпропил, 4-хлорбутил, 5-хлорпентил, гидроксиметил, гидроксипропил, гидроксибутил, метоксиметил, этоксиметил, фенетил, 1,2-дифенилэтил, 2,2,2-трифторэтил, 2,2,2-трифторэтокси, бензил, L-гидроксибензил, метилбензил, 2-фторбензил, аллил, 2-бутенил, фенил, хлорфенил, фторфенил, 4-бромфенил, 2,3-дихлорфенил, 3,4-дихлорфенил, 4-метилфенил, 3-метилфенил, 2-метилфенил, 4-этилфенил, 4-изопропилфенил, 4-трет-бутилфенил, 3,4-диметилфенил, 4-метоксифенил, 4-этоксифенил, 4-метил-3-хлорфенил, 4-метокси-3-хлорфенил, 3-метил-4-метоксифенил, 3,4-метилендиоксифенил, 4-(2", 2", 2"-трифторэтокси)фенил, 4-цианофенил, 4-нитрофенил, 2-фурил, 5-метил-2-фурил, 2-тиенил, 5-хлор-2-тиенил, 5-бром-2-тиенил, SOnR6. R6 - алкил, С1-С4, аллил, фенил, бензил, 3-фторфенил-2-пиридил, 4-хлорфенил, при n = 0, R3 -диметиламино, этил при n = 2, CONHR7, R7 - фенил, 4-хлорфенил, R3 - водород, хлор, бром, йод, циано, нитро, метил, этил, метилтио, фенилтио, 2-фурил, трифторацетил, R4 - изопропил, диметиламино, диэтиламино, морфолино, в количестве 5-20 мас.ч., носитель - 60-93 мас.ч., поверхностно-активное вещество 2-20 мас.ч. Новое имидазоловое вещество, представленное общей формулой (1), может быть получено конкретно следующим способом. (А) где R1 - CN или CSNHR5; R5 - водород, ацетил, или пропионил, R2 - водород, циклопропил, циклогексил, 2-нафтил, алкил С1-С8, С12, 3-фторпропил, 3-хлорпропил, 4-хлорбутил, 5-хлорпентил, гидроксиметил, гидроксипропил, гидроксибутил, метоксиметил, этоксиметил, фенетил, 1,2-дифенилэтил, 2,2,2-трифторэтил, 2,2,2-трифторэтокси, бензил, L-гидроксибензил, метилбензил, 2-фторбензил, аллил, 2-бутенил, фенил, хлорфенил, фторфенил, 4-бромфенил, 2,3-дихлорфенил, 3,4-дихлорфенил, 4-метилфенил, 3-метилфенил, 2-метилфенил, 4-этилфенил, 4-изопропилфенил, 4-трет-бутилфенил, 3,4-диметилфенил, 4-метоксифенил, 4-этоксифенил, 4-метил-3-хлорфенил, 4-метокси-3-хлорфенил, 3-метил-4-метоксифенил, 3,4-метилендиоксифенил, 4-(2", 2", 2"-трифторэтокси)фенил, 4-цианофенил, 4-нитрофенил, 2-фурил, 5-метил-2-фурил, 2-тиенил, 5-хлор-2-тиенил, 5-бром-2-тиенил, SOnR6. R6 - алкил, С1-С4, аллил, фенил, бензил, 3-фторфенил-2-пиридил, 4-хлорфенил, при n = 0, R3 -диметиламино, этил при n = 2, CONHR7, R7 - фенил, 4-хлорфенил, R3 - водород, хлор, бром, йод, циано, нитро, метил, этил, метилтио, фенилтио, 2-фурил, трифторацетил, R4 - изопропил, диметиламино, диэтиламино, морфолино, в количестве 5-20 мас.ч., носитель - 60-93 мас.ч., поверхностно-активное вещество 2-20 мас.ч. Новое имидазоловое вещество, представленное общей формулой (1), может быть получено конкретно следующим способом. (А) 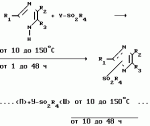  в которых радикалы R1/ R2/ R3 и R4 имеют те же самые значения/ которые указаны выше/ а Y является атомом галогена. В описанной общей формуле 1/ вещества/ в которых R1 является циано-группой/ также могут быть получены следующим образом: /B/ в которых радикалы R1/ R2/ R3 и R4 имеют те же самые значения/ которые указаны выше/ а Y является атомом галогена. В описанной общей формуле 1/ вещества/ в которых R1 является циано-группой/ также могут быть получены следующим образом: /B/  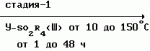 NC NC  В общей формуле (1-2), описанной выше, в которой R3 является группой - SR7, на стадии - 2 способа (В), описанной выше, вместо R3 - 1 также можно использовать группу R7SSR7. В приведенных выше формулах радикалы R2, R3, R4, R7 и Y имеют те же самые значения, которые описаны выше. В описанной выше общей формуле (1), вещества, в которых R1 является циано-группой и R3 представляет собой атом водорода, атом хлора или атом брома, также могут быть получены следующим способом. (С) В общей формуле (1-2), описанной выше, в которой R3 является группой - SR7, на стадии - 2 способа (В), описанной выше, вместо R3 - 1 также можно использовать группу R7SSR7. В приведенных выше формулах радикалы R2, R3, R4, R7 и Y имеют те же самые значения, которые описаны выше. В описанной выше общей формуле (1), вещества, в которых R1 является циано-группой и R3 представляет собой атом водорода, атом хлора или атом брома, также могут быть получены следующим способом. (С) 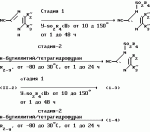 В общей формуле (1-4), описанной выше, в которой R2 является группой - SR7, на стадии - 2 способа (С) также может использоваться R7SSR7 вместо R2-Y; и если R2 является группой -CH(OH)-R13 (в которой R13 является алкильной группой или необязательно замещенной фенильной группой), на Стадии-2 описанного способа (С) вместо R2-Y, также может использоваться R13-CHO. В предшествующих формулах радикалы R2, R4 и R7имеют те же самые значения, которые описаны выше: R2 и R3 представляют собой одновременно атомы водорода, атомы хлора или брома; Y является атомом хлора, брома или иода. В общей формуле (1), вещества, в которых R1 является группой -CSNH2 или группой -CSNHOR6, также могут быть получены следующим способом: (Д) В общей формуле (1-4), описанной выше, в которой R2 является группой - SR7, на стадии - 2 способа (С) также может использоваться R7SSR7 вместо R2-Y; и если R2 является группой -CH(OH)-R13 (в которой R13 является алкильной группой или необязательно замещенной фенильной группой), на Стадии-2 описанного способа (С) вместо R2-Y, также может использоваться R13-CHO. В предшествующих формулах радикалы R2, R4 и R7имеют те же самые значения, которые описаны выше: R2 и R3 представляют собой одновременно атомы водорода, атомы хлора или брома; Y является атомом хлора, брома или иода. В общей формуле (1), вещества, в которых R1 является группой -CSNH2 или группой -CSNHOR6, также могут быть получены следующим способом: (Д)  где радикалы R2/ R3/ R4/ R6 и Y имеют указанные значения. Способ /А/ и Стадия-1 способов /В/ - /Д// описанных выше/ проводятся/ если это необходимо и желательно/ в присутствии растворителя и акцептора кислоты. Примеры раствотителя включают ароматические углеводороды/ такие как бензол/ толуол/ксиол/ хлорбензол/ и др; циклические и ациклические алифатические углеводороды/ такие как хлороформ/ четыреххлористый углерод/ хлористый метилен/ дихлорэтан/ трихлорэтан/ н-гесан/ циклогексан и др.; простые эфиры; также как диэтиловый эфир, диоксан, тетрагидрофуран и др.; кетоны, такие как ацетон, метилэтилкетон, метилизобутилкетон и др.; нитрилы, такие как ацетонитрил, пропионитрил и др.; и апротонные полярные растворители, такие как диметилформамид, N-метилпирролидон, диметилсульфоксид, сульфолан и другие. В качестве акцептора кислоты может использоваться любое из неорганических и органических оснований. Примеры неорганического основания включают гидроксиды щелочных металлов, такие как гидроксид натрия, гидроксид калия и др.; карбонаты щелочных или щелочно-земельных металлов, такие как безводный карбонат калия, безводный карбонат кальция и др.; гидриды щелочных металлов, такие как гидрид натрия; щелочные металлы, такие как металлический натрий и другие. Кроме того, в качестве органического основания может быть упомянут триэтиламин и другие. Описанная реакция может быть осуществлена в присутствии подходящего катализатора. В качестве катализатора может быть упомянут, например, катализатор фазового переноса, такой как производная четвертичного аммония. В качестве атома галогена, показанного как Y в общей формуле (III), описанной выше, могут быть упомянуты атом хлора, брома, иода и атом фтора, из которых предпочтительным является атом хлора. Пример синтеза 1. Синтез 2-циано-1-диметилсульфамоил-5-фенилтиоимидазола (соединение N 45-б). В четырехгорлую колбу загружают 12,0 г 2-циано-1-диметилсульфамоилимидазола (Compound N 1) и 240 мл осушенного тетрагидрофурана в потоке азота. Поддерживая температуру смеси при -75оС или ниже смесью сухого льда с ацетоном, к смеси постепенно, по каплям добавляют 41,3 мл раствора н-бутиллития в гексане (1,6 молярный) производство фирмы "Альдрих"). После завершения капельного добавления, систему выдерживают в течение 15 мин при той же температуре. Затем при -70оС или ниже к смеси по каплям добавляют раствор 17 г дифенилдисульфида в 30 мл тетрагидрофурана. При перемешивании в течение ночи температуру смеси постепенно повышают до комнатной. После завершения взаимодействия реакционную смесь выливают в воду. Проводят экстракцию 500 мл этилацетата. После промывания водой экстракт сушат над безводным сульфатом натрия. Этилацетат удаляют путем перегонки и остаток очищают хроматографически на колонке с силикагелем (проявляющий растворитель : хлористый метилен), получая 4,3 г 2-циано-1-диметилсульфамоил-5-фенилтио- имидазола (соединение N 45-б), имеющего температуру плавления 106-107оС. Пример синтеза 2. Синтез 4-хлор-2-циано-1-диметилсульфамоил-5-н-пропилами-дазола (соединение N 48-б). (1). 2-Циано-1-диметилсульфамоил-5-н-пропилимидазол (4,8 г), имеющий температуру плавления 51-52оС (соединение N 48-б), синтезируют путем взаимодействия 12,0 г 2-циано-1-диметилсульфамоилимидазола и 15,3 г н-пропилиодида по способу, который аналогичен описанному в примере синтеза 1. (2). 2-Циано-1-диметилсульфамоил-5-н-пропилимидазол (4,8 г), такой как получен выше в (1), 40 мл пиридина и 11,4 г хлористого пиридиния смешивают и смесь перемешивают 4 ч при 90оС. После завершения взаимодействия пиридин удаляют из реакционной смеси путем перегонки и остаток экстрагируют этилафетатом. Экстракт промывают водой и затем сушат над безводным сульфатом натрия. После этого этилацетат удаляют путем перегонки и остаток очищают хроматографически а колонке с силикагелем (проявляющий растворитель : смесь этилацетата и н-гексана) и при выделении получают 2,46 г 2-циано-4(5)-н-пропилимидазола (промежуточное соединение), имеющее температуру плавления 52-54оС. (3) 2-Циано-4(5)-н-пропилимидазол, такой как получен в (2), 80 мл хлороформа и 2,6 г N-хлорсукцинимида смешивают, и смесь подвергают взаимодействию в течение 4 ч при температуре кипения с обратным холодильником. После завершения взаимодействия к реакционной смеси добавляют 200 мл воды. Образовавшийся органический слой промывают водой и затем сушат над безводным сульфатом натрия. После сушки хлороформ удаляют путем перегонки, и остаток очищают хроматографически на колонке с силикагелем (проявляющий растворитель - смесь 1:1 этилацетата и н-гексана), и при выделении получают 2,2 г 4(5-хлор)2-циано-5(4)-н-пропилимидазола (промежуточное соединение), имеющего температура плавления 107-109оС. (4). 4(5)-Хлор-2-циано-5(4)-н-пропилимидазол (2,0 г) такой, как получен выше в (3), 30 мл ацетонитрила, 1,95 г безводного карбоната калия и 1,86 г хлористого диметилсульфамоила смешивают и после постепенного повышения температуры, смесь подвергают взаимодействию при температуре кипения с обратным холодильником в течение 1 ч. После завершения взаимодействия ацетонитрил удаляют путем отгонки из реакционной смеси. После вливания 100 мл воды к остатку, образовавшуюся смесь экстрагируют 50 мл хлористого метилена. Экстракт промывают водой и сушат над безводным сульфатом натрия. После этого хлористый метилен удаляют путем перегонки. Остатку дают отстояться в течение ночи, после чего анализ смеси показал, что один из двух изомеров в смеси разложился и превратился в исходный 4(5)-хлор-2-циано-5(4)-н-пропилимидазол. Остаток, содержащий другой изомер, очищают хроматографически на колонке с силикагелем (проявляющий растворитель : хлористый метилен) и при выделении получают 1,1 г 4-хлор-2-циано-1-диметилсульфамоил-5-н-пропилимидазола (соединение N 48-б), имеющего температуру плавления 64-66оС. Пример синтеза 3. Синтез 2-циано-1-диметилсульфамоил-4(5)-фенилимидазола (соединение N 1). (1). В 320 мл ацетона растворяют 23,04 г 4(5)-фенилимидазола и к раствору добавляют 12,14 г безводного карбоната калия. Смесь нагревают при температуре кипения с обратным холодильником в течение 2 ч. После охлаждения к смеси по каплям добавляют 45 мл ацетонового раствора, содержащего 25,26 г хлористого диметилсульфамоила. После завершения капельного добавления, смесь нагревают при температуре кипения с обратным холодильником в течение 4,5 ч, чтобы реакция завершилась. После завершения взаимодействия, реакционную смесь охлаждают и твердые вещества удаляют путем фильтрации. После удаления растворителя путем отгонки при пониженном давлении остаток очищают хроматографически на колонке с силикагелем (проявляющий растворитель : хлористый метилен), получая 27,8 г 1-диметилсульфамоил-4(5)-фенилимидазола, имеющего температуру плавления 96-100оС. (2). В 290 мл тетрагидрофурана растворяют 17 г 1-диметилсульфамоил-4(5)-фенилимидазола, такого как получен выше в (1). Этот раствор охлаждают до -70оС в токе азота и к смеси в течение 30 ми по каплям добавляют 51 мл 1,6-молярного раствора н-бутиллития в гексане. После завершения капельного добавления реакционную смесь перемешивают при -70оС в течение 30 мин. Затем к смеси добавляют по каплям 12 мл тетрагидрофуранового раствора, содержащего 6 г N,N-диметилформамида. После завершения капельного добавления реакционную смесь подвергают взаимодействию в течение 15 ч при перемешивании, в то время как ее температура медленно повышается до комнатной. После завершения взаимодействия реакционную смесь выливают в воду со льдом и экстрагируют этилацетатом. После промывания экстрагированного слоя водой, этот слой сушат над безводным сульфатом натрия. Отгоняют растворитель при пониженном давлении, и остаток очищают хроматографически на колонке с силикагелем (проявляющий растворитель - смесь 1:2 этилацетат : н-гексан), получая 12,8 г 1-диметилсульфамоил-2-формил-4(5)-фенилими- дазола, имеющего температуру плавления 86-89оС. (3). В 120 мл пиридина растворяют 11,16 г 1-диметилсульфамоил-2-формил-4(5)-фенилимидазола, такого как получен выше в (2), и 5,56 г хлористоводородного гидроксиламина, и 24 мл уксусного ангидрида добавляют по каплям к раствору при комнатной температуре. После завершения капельного добавления температуру смеси постепенно повышают и смесь реагирует при 100оС в течение 12 ч. После завершения взаимодействия растворитель из реакционной смеси удаляют путем перегонки при пониженном давлении. Затем к остатку добавляют 125 мл воды и выпавшее в осадок твердое вещество отделяют путем фильтрации. Неочищенный продукт растворяют в этилацетате и очищают хроматографически на колонке с силикагелем (проявляющий растворитель : этилацетат), получая 5,55 г 2-циано-4(5)-фенилимидазола, имеющего температуру плавления 208-205оС. (4). В 88 мл ацетона растворяют 1,7 г 2-циано-4(5)-фенилимидазола, такого как получен выше в (3), и к раствору добавляют 1,7 г безводного карбоната калия. Смесь нагревают при температуре кипения с обратным холодильником в течение 2 ч. После охлаждения к смеси по каплям добавляют 6 мл ацетонового раствора, содержащего 1,7 г хлористого диметилсульфамоила. После завершения капельного добавления смесь нагревают при температуре кипения с обратным холодильником 2 ч для завершения реакции. После завершения взаимодействия реакционную смесь охлаждают, и твердое вещество удаляют путем фильтрации. После удаления растворителя путем перегонки при пониженном давлении, остаток экстрагируют этилацетатом. Экстракт промывают водой и сушат над безводным сульфатом натрия. Растворитель удаляют путем перегонки при пониженном давлении и получают 2 г 2-циано-1-диметилсульфамоил-4(5)-фенил- имидазола (соедиение N 1), имеющего температуру плавления 101-102оС. Пример синтеза 4. Синтез 4(5)-хлор-2-циано-1-диметилсульфамоил-5(4)-фенил- имидазола (соединение N 7) и 4-хлор-2-циано-1-диметилсульфамоил-5-фенилимидазола (соединение N 7-б). (1). В 100 мл хлороформа растворяют 1,352 г 2-циано-4(5)-фенилимидазола и к раствору добавляют 1,175 г п-хлорсукцинимида. Эта смесь взаимодействует при нагревании до температуры кипения с обратным холодильником в течение 4 ч. После завершения взаимодействия реакционную смесь выливают в воду и экстрагируют хлороформом. После промывания водой экстрагированный слой сушат над безводным сульфатом атрия. Растворитель отгоняют при пониженном давлении, и остаток очищают хроматографически на колонке с силикагелем (проявляющий растворитель : хлористый метилен), получая 1,28 г 4(5)-хлор-2-циано-5(4)-фенилимидазола (промежуточное соединение), имеющего температуру плавления 149-151оС. (2). В 6 мл ацетона растворяют 0,43 г 4(5)-хлор-2-циано-5(4)-фенилимидазола, который получен в (1), к раствору добавляют 0,29 г безводного карбоната калия и 0,36 г хлористого диметилсульфамоила. Эта смесь взаимодействует при нагревании до температуры кипения с обратным холодильником в течение 30 мин. После завершения взаимодействия реакционную смесь выливают в воду и экстрагируют этилацетатом. После промывания водой экстрагированный слой сушат над безводным сульфатом натрия. Растворитель отгоняют при пониженном давлении, и остаток затем очищают хроматографически на колонке с силикагелем (проявляющий растворитель : хлористый метилен), получая 0,5 г 4(5)-хлор-2-циано-1-диметилсульфамоил-5(4)фенилимидазола (соединение N 7), имеющее температуру плавления 106-109оС. В результате анализа с помощью спектров ЯМР, описанное выше соединение является смесью изомеров 4-хлор-2-циано-1-диметилсульфа- моил-5-фенилимидазола и 5-хлор-2-циано-1-диметилсульфамоил-4-фенилимидазола в почти равных отношениях. (3). После выдерживания в течение 24 ч при комнатной температуре 2,9 г смеси этих изомеров, которая получена способом, аналогичным описанному в (2), ее очищают хроматографически на колонке с силикагелем (проявляющий растворитель : хлористый метилен), получая 1,15 г 4-хлор-2-циано-1-диметилсульфамоил-5-фенилимидазола (соединение N 7-о), имеющего температуру плавления 109-112оС. Кроме того, посредством очистки и выделения из этого соединения было также получено 0,7 г 4(5)-хлор-2-циано-5(4)-фенилимидазола (промежуточное соединение). Пример синтеза 5. Синтез 4(5)-хлор-2-циано-1-диметилсульфамоил-5(4)-(4)-метил- фенил)имидазола (соединение N 8) и 4-хлор-2-циано-1-диметилсульфамоил-5-(4- метилфенил)имидазола (соединение N 8-б). Смесь изомеров (соединение N 8), имеющая температуру плавления 101-108оС, 4-хлор-2-циано-1-диметилсульфамоил-5-(4-ме- тилфенил)имидазол и 5-хлор-2-циано-1-диметилсульфамоил-4-(4-метилфенил)имидазол, была получена из 4(5)-(4-метилфенил)имидазола в отношении 6: 4 способом, аналогичным примерам синтезов 4 и 5, которые описаны выше. После того, как 0,75 г смеси изомеров прореагируют при 40оС в течение 8 ч, реакционную смесь очищают хроматографически на колонке с силикагелем (проявляющий растворитель : хлористый метилен), получая 0,45 г 4-хлор-2-циано-1-диметилсульфамоил-5-(4-метилфенил)имидазола (соединение N 8-б), имеющего температуру плавления 133-134оС. Кроме того, путем очистки и выделения из этого соединения также получают 0,15 г 4(5)-хлор-2-циано-5(4)-(4-метилфенил)имидазола, имеющего температуру плавления 124-129оС. Пример синтеза 6. Синтез 4(5)-хлор-5(4)-(4-хлорефнил)-2-циано-1-диметилсульфамоил- имидазола (соединение N 12), 4-хлор-5-(4-хлорфенил)-2-циано-1-диметилсульфамо- илимидазола (соединение N 12-б) и 5-хлор-4-(4-хлорфенил-2-циано-1-диметилсульфа-моилимидазола (соединение N 12-а). Способом, который аналогичен примерам синтеза 4 и 5, описанным выше, 0,80 г изомерной смеси (соединение N 12), имеющей температуру плавления около 108оС, 4-хлор-5-(4-хлорфенил)-2-циано-1-диметил- сульфамоилимидазола и 5-хлор-4-(4-хлорфенил)-2-циано-1-диметилсульфамоилими- дазола, получают из 4(5)-(4-хлорфенил)-имидазола. Смесь изомеров очищают хроматографически на колонке с силикагелем (проявляющий растворитель : хлористый метилен). Элюат второй фракции концентрируют и подвергают перекристаллизации из хлористого метилена, получая 0,16 г 4-хлор-5-(4-хлорфенил) -2-циано-1-диметилсульфамо-илимидазола (соединение N 12-б), имеющего температуру плавления 117-120оС. Кроме того, элюат первой фракции концентрируют таким же образом, получая 0,50 г 5-хлор-4-(4-хлорфенил)-2-циано-1-диметил- сульфамоилимидазола (соединение N 12-а), имеющего температуру плавления 133-138оС. Пример синтеза 7. Синтез 1-диметилсульфамоил-4(5)-фенилимидазол-2-карбо- тиоамида (соединение N 23). В 30 мл диоксана растворяют 1,0 г 2-циано-1-диметилсульфамоил-4(5)-фенилими-дазол (соединение N 1) и к раствору добавляют 0,36 г триэтиламина. Смесь нагревают до температуры 40-50оС при перемешивании, вводят в нее газообразный сероводород в течение 1 ч и 25 мин. После этого смесь реагирует при 40-50оС еще в течение 50 мин. После завершения взаимодействия реакционную смесь охлаждают, выливают в воду и экстрагируют этилацетатом. После промывания водой экстрагированный слой сушат над безводным сульфатом натрия. Растворитель отгоняют при пониженном давлении и остаток очищают хроматографически на колонке с силикагелем (проявляющий растворитель - смесь 1:3 этилацетата и н-гексана), получая 0,8 г 1-диметилсульфамоил-4(5)-фенилимидазол-2-карботиоамида (соединение N 23), имеющего температуру плавления 155-175оС. Кроме того, в небольшом количестве получают кристаллы 4(5)-фенилимидазол-2-карботиоамида. Пример синтеза 8. Синтез 2-циано-1-изопропилсульфонил-4(5)-фенилимидазол (соединение N 32). При комнатной температуре смешивают 1 г 2-циано-4(5)-фенилимидазола, 0,98 г безводного карбоната калия и 30 мл ацетонитрила. После взаимодействия в течение 2 ч при температуре кипения реакционную смесь охлаждают, раствор 1,0 г хлористого изопропилсульфонила в 5 мл ацетонитрила добавляют к смеси. Эта смесь снова реагирует при температуре кипения в течение 1,5 ч. После завершения реакции реакционную смесь выливают в воду. Проводят экстракцию хлористым метиленом. После промывания водой экстракт сушат над безводным сульфатом натрия. Растворитель удаляют путем перегонки при пониженном давлении, остаток очищают хроматографически на колонке с силикагелем (проявляющий растворитель : хлористый метилен), получая 1,4 г 2-циано-1-изопропилсульфонил-4(5)-фенилимидазола (соединение N 32), имеющего температуру плавления 80-83оС. Пример синтеза 9. Синтез 4(5)-(2-тиенил)-2-циано-1-диметилсульфамоилимида-зола (соединение N 3). (1). К 150 мл формамида добавляют 25 г 2-(бромацетил)тиофена. Смесь подвергают взаимодействию при 180-190оС в течение 2 ч. После завершения взаимодействия реакционную смесь выливают в воду и добавляют в нее концентрированную соляную кислоту для того, чтобы сделать систему кислотной. Затем проводят промывание хлористым метиленом. После нейтрализации аммиачной водой, водную фазу экстрагируют хлористым метиленом. После промывания водой экстракт сушат над безводным сульфатом натрия. Растворитель удаляют путем перегонки при пониженном давлении, получая 11 г 4(5)-(2-тиенил)-имидазола. (2). К 200 мл ацетонитрила добавляют 11,6 г хлористого диметилсульфамоила, 11,1 г безводного карбоната калия и 11 г 4(5)-(2-тиенил)имидазола, который получен выше в (1). При перемешивании эта смесь реагирует в течение 2 ч. После завершения взаимодействия реакционную смесь выливают в воду. Проводят экстракцию этилацетатом. После промывания водой экстракт сушат над безводным сульфатом натрия. Растворитель удаляют путем перегонки при пониженном давлении, получая 14,5 г 4(5)-(2-тиенил)-1-диметилсульфамоилимидазола. (3). В 120 мл безводного тетрагидрофурана растворяют 9,5 г 4(5)-(2-тиенил)-1-диметилсульфамоилимидазола, который получен выше в (2). В токе азота при -78оС к раствору по каплям добавляют 26,2 мл 1,6-молярного раствора н-бутиллития в гексане, смесь перемешивают при той же температуре в течение 15 мин. Затем к смеси по каплям добавляют 20 мл тетрагидрофуранового раствора, в котором растворено 5,4 г N,N-диметилформамида. После завершения капельного добавления, температуру смеси постепенно повышают до комнатной для того, чтобы реакция завершилась. После завершения взаимодействия реакционную смесь выливают в воду. Проводят экстракцию этилацетатом. После промывания водой экстракт сушат над безводным сульфатом атрия. Растворитель удаляют путем перегонки при пониженном давлении, получая 5,4 г 4(5)-(2-тиенил)-2-формил-1-диметилсульфамоилимидазола. (4). В 54 мл пиридина растворяют 2,6 г хлористоводородного гидроксиламина и 5,4 г 4(5)-(2-тиенил)-2-формил-1-диметилсульфамоилимидазола, который получен в (3). Раствор перемешивают при комнатной температуре в течение 15 мин. Затем к раствору постепенно добавляют 10 мл уксусного ангидрида, после чего осуществляют реакцию при 60-70оС в течение 2 ч. После завершения взаимодействия, реакционную смесь выливают в воду. Проводят экстракцию этилацетатом. После промывания водой экстракт сушат над безводным сульфатом натрия. Растворитель удаляют путем перегонки при пониженном давлении и остаток очищают хроматографически на колонке с силикагелем (проявляющий растворитель - смесь 2:1 этилацетата и н-гексана), получая 1,2 г 4(5)-(2-тиенил)-2-цианоимидазола, имеющего темпеpатуpу плавления 195-203оС. (5). К 50 мл ацетонитрила добавляют 1,1 г хлористого диметилсульфамоила, 1,0 г безводного карбоната калия и 1,2 г 4(5)-(2-тиенил)-2-цианоимидазола, который получен выше в (4). Эта смесь взаимодействует при температуре кипения в течение 2 ч. После завершения взаимодействия реакционную смесь выливают в воду и экстрагируют этилацетатом. После высушивания экстракта над безводным сульфатом натрия растворитель удаляют путем перегонки при пониженном давлении, остаток очищают хроматографически на колонке с силикагелем (проявляющий растворитель - хлористый метилен), получая 1,3 г 4(5)-(2-тиенил)-2-циано-1-диметилсульфа- моилимидазола (соединение N 3), имеющего температуру плавления 145-150оС. Пример синтеза 10. Синтез 4(5)-хлор-2-циано-1-диметилсульфамоил-5(4)-изопро-пилимидазола (соединение N 125) и 4-хлор-2-циано-11-диметилсульфамоил-5-изопро-пилимидазола (соединение N 86-б). (1). Нагревают до 180оС 360 г формамида и добавляют к нему по каплям в течение 30 мин 102 г 1-гидрокси-3-метил-2-бутанола (приготовленного по способу, описанному Липшутцом и Морей в I.Org.Chem. том 48, 3745 (1983). После завершения капельного добавления смесь реагирует при 180оС в течение 1 ч. После завершения взаимодействия реакционную смесь охлаждают и выливают в ледяную воду. Образовавшуюся смесь подкисляют до рН между 4 и 5 аммиачной водой. К нему добавляют 5 г активированного древесного угля, смесь перемешивают в течение 1 ч. Активированный древесный уголь удаляют путем фильтрации, и фильтрат подщелачивают до рН 8 аммиачной водой. Затем проводят экстракцию хлористым метиленом, и экстракт сушат над безводным сульфатом натрия. Растворитель удаляют путем перегонки при пониженном давлении, получая 13 г 4(5)-изопропилимидазола. (2). В 300 мл ацетонитрила растворяют 11,8 4(5)-изопропилимидазола, который получен выше в (1), к раствору добавляют 18 г безводного карбоната калия. Смесь кипятят с обратным холодильником в течение 30 мин, после охлаждения к ней по каплям добавляют 17 г хлористого диметилсульфамоила. После завершения капельного добавления смесь кипятят, чтобы реакция завершилась. После завершения взаимодействия реакционную смесь охлаждают, выливают в воду и затем экстрагируют этилацетатом. Экстрагированный слой промывают водой и сушат над безводным сульфатом натрия. Растворитель удаляют путем перегонки при пониженном давлении, остаток очищают хроматографически на колонке с силикагелем (проявляющий растворитель : хлористый метилен), получая 13 г 1-диметилсульфамоил-4(:)-изопропилими-дазола. (3). В 200 мл тетрагидрофурана растворяют 13 г 1-диметилсульфамоил-4(5)-изопропилимидазола, который получен в (2). Этот раствор охлаждают до -70оС в токе азота и добавляют к нему по каплям в течение 15 мин 38 мл 1,6 молярного раствора н-бутиллития в гексане. После завершения капельного добавления смесь перемешивают при -70оС в течение 30 мин. После капельного добавления 5,6 г N,N-диметилформамида смесь реагирует при перемешивании в течение 15 мин, в то время как ее температура медленно повышается до комнатной. После завершения взаимодействия реакционную смесь выливают в ледяную воду и экстрагируют этилацетатом. Экстрагированный слой промывают водой и сушат над безводным сульфатом натрия. Растворитель отгоняют при пониженном давлении, получая 8,6 г 1-диметилсульфамоил-2-формил-4(5)-изопропилимидазола. (4). В 100 мл пиридина растворяют 8,5 г 1-диметилсульфамоил-2-формил-4(5)-изо- пропилимидазола, который получен в (3), 4,8 г хлористоводородного гидроксиламина, к этому раствору по каплям добавляют 10 мл уксусного ангидрида при комнатной температуре. После завершения капельного добавления, температуру смеси постепенно повышают, смесь реагирует 5 ч при 80-90оС. После завершения взаимодействия из реакционной смеси отгоняют растворитель при пониженном давлении. К остатку добавляют воду, смесь экстрагируют этилацетатом. Экстрагированный слой промывают разбавленной соляной кислотой и затем водой, сушат над безводным сульфатом натрия. Растворитель отгоняют перегонки при пониженном давлении, получая 2,35 г 2-циано-4(5)-изопропилимидазола (промежуточное соединение), имеющее температуру плавления 88-91оС. (5). В 80 мл метанола растворяют 2 г 2-циано-4(5)-изопропилимидазола, который получен выше в (4), и к раствору добавляют 2,1 г п-хлорсукцинимида. Смесь перемешивают при комнатной температуре в течение 20 ч и затем подвергают взаимодействию при 40оС в течение 8 ч. После завершения взаимодействия из реакционной смеси при пониженном давлении отгоняют метанол. К остатку добавляют воду, смесь экстрагируют этилацетатом. Экстрагированный слой промывают водой над безводным сульфатом натрия. Растворитель отгоняют при пониженном давлении, и остаток очищают хроматографически на колонке с силикагелем (проявляющий растворитель : хлористый метилен), получая 1,67 г 4(5)-хлор-циано-5(4)-изопропилимидазола, имеющего температуру плавления 84-87оС. (6). В 30 мл ацетонитрила растворяют 1,6 г 4(5)-хлор-2-циано-5(4)-изопропилимидазола, который получен выше в (5), к раствору добавляют 1,56 г безводного карбоната калия. Смесь кипятят с обратным холодильником в течение 30 мин. После охлаждения в нее добавляют 1,49 г диметилсульфамоилхлорида по каплям. После завершении капельного добавления смесь кипятят в течение 15 мин, чтобы взаимодействие завершилось. После окончания взаимодействия реакционную смесь охлаждают, выливают в воду и затем экстрагируют этилацетатом. Экстрагированный слой промывают водой и сушат над безводным сульфатом натрия. Растворитель отгоняют при пониженном давлении, остаток очищают хроматографически на колонке с силикагелем (проявляющий растворитель - хлористый метилен), получая 2,1 г 4(5)-хлор-2-циано-1-сульфамоил-5(4)-изопропилимидазола (соединение N 86). В результате анализа с помощью спектров ЯМР установлено, что описанное соединение является смесью изомеров 4-хлор-2-циано-1-диметилсульфамоил-5- изопропилимидазола и 5-хлор-2-циано-1-диметилсульфамоил-4-изопропилимидазола в примерном соотношении 2:1. (7). После выдерживания в течение 5 сут при комнатной температуре 2,1 г смеси изомеров, полученной в (6), подвергают хроматографической очистке на колонке с силикагелем (проявляющий растворитель - хлористый метилен), получая 1 г 4-хлор-2-циано-1-диметилсульфамоил-5-изопропил- имидазола (соединение N 86-б), имеющего температуру плавления 75-82оС (разлагается). Кроме того путем очистки и выделения из этого соединения также получают 4(5)-хлор-2-циано-5(4)-изопропилимидазол. Пример синтеза 11. Синтез 4-хлор-1-диметилсульфамоил-5-н-пропилимидазол-2-карботиоамида (соединение N 129-б). (1). В четырехгорлую колбу загружают 6, г 2-циано-4,5-дихлор-1-диметилсульфамоилимидазола, имеющего температуру плавления 100-103оС, и 180 мл осушенного тетрагидрофурана в токе азота. Поддерживая температуру смеси при -70оС или ниже (с помощью смеси сухой лед/ацетон) к смеси постепенно по каплям добавляют 15,3 мл 1,6 молярного раствора н-бутиллития в гексане (производство фирмы Альдрих). После завершения капельного добавления систему выдерживают при этой температуре в течение 15 мин. Затем к смеси при -70оС или ниже по каплям добавляют раствор 5,7 г н-проилиодида в 15 мл тетрагидрофурана. При перемешивании в течение ночи температура смеси постепенно повышается до комнатной. После завершения взаимодействия реакционную смесь выливают в воду. Проводят экстракцию хлористым метиленом (500 мл). После промывания водой экстракт сушат над безводным сульфатом натрия. Хлористый метилен удаляют путем перегонки, остаток очищают хроматографически на колонке с силикагелем (проявляющий растворитель - хлористый метилен) и затем снова очищают хроматографически на колонке с силикагелем (проявляющий растворитель - смесь этилацетата и н-гексана), получая 2,8 г 4-хлор-2-циано-1-диметилсульфамоил-5-н-пропилимидазола (соединение N 48-б), имеющего температуру плавления 66-68оС. (2). В четырехгорлую колбу загружают 2,7 г 4-хлор-2-циано-1-диметилсульфамоил-5-н-пропилимидазола, который получен в (1), 40 мл диоксана, 1,0 г триэтиламина и 0,8 г пиридина. В эту смесь вводят газообразный сероводород при 20-25оС, приблизительно в течение 30 мин, до тех пока не прореагируют исходные материалы. После завершения взаимодействия реакционную смесь выливают в воду, а выпавшие в осадок кристаллы отфильтровывают на фильтре Нутча и сушат. Образовавшиеся кристаллы очищают хроматографически на колонке с силикагелем (проявляющий растворитель - хлористый метилен) и выделяют, получая 2,3 г 4-хлор-1-диметилсульфамоил-5-н-пропилимидазола (соединение N 129-б), имеющего температуру плавления 160-162оС. Пример синтеза 12. Синтез N-пропионил-4-хлор-1-диметилсульфамоил-5-н-про-пилимидазола-2- карботиоамида (соединение N 121-б). В четырехгорлую колбу загружают 2,0 г 4-хлор-1-диметилсульфамоил-5-н-пропил-имидазол-2-карботиоамида (соединение N 121-в), 24 мл ацетона и 1,12 г пиридина. К смеси при 0-5оС по каплям добавляют 1,19 г хлористого пропионила. После завершения капельного добавления взаимодействие осуществляют при 30-35оС в течение 1 ч и при температуре кипения с обратным холодильником еще в течение 30 мин при перемешивании. После завершения взаимодействия, реакционную смесь выливают в воду и экстрагируют этилацетатом. Экстрагированный слой промывают водой и сушат над безводным сульфатом натрия. После этого этилацетат удаляют при перегонке, а остаток очищают хроматографически на колонке с силикагелем (проявляющий растворитель - хлористый метилен) и выделяют, получают 1,02 г N-пропионил-4-хлор-1-диметилсульфамоил-5-н-пропилимидазол-2- карботиоамида (соединение N 121-б), имеющего температуру плавления 150-152оС. Пример синтеза 13. Синтез 2-циано-1-диметилсульфамоил-4,5-дифенилтиоимида- зол (соединение N 38). (1). 2-Циано-1-диметилсульфамоил-5-фенилтиоимидазол (8,0 г, соединение N 45-б), полученный так же, как в примере синтеза N 1, описанном выше, 60 мл метанола и 60 мл 7%-ной соляной кислоты загружают в колбу, смесь подвергают взаимодействию при перемешивании при 40-50оС в течение 2 ч. После завершения взаимодействия реакционную смесь слегка подщелачивают аммиаком, осажденные кристаллы отделяют путем фильтрации и сушат, получая 4,2 г 2-циано-4(5)-фенилтиоимидазола, имеющего температуру плавления 166-169оС. (2). К смеси 4,2 г 2-циано-4(5)-фенилтиоимидазола, полученного выше в (1), 80 мл ацетонитрила и 3,1 г безводного карбоната калия добавляют 3,4 г хлористого диметилсульфамоила. Образовавшуюся смесь подвергают взаимодействию при температуре кипения с обратным холодильником в течение 1 ч. После завершения взаимодействия реакционную смесь охлаждают, твердые вещества отфильтровывают. Растворитель из фильтра удаляют путем перегонки, а остаток очищают хроматографически на колонке с силикагелем (проявляющий растворитель - хлористый метилен) и выделяют, получая 5,8 г 2-циано-1-диметилсульфамоил-4(5)-фенилтиоимидазола. (3). В четырехгорлую колбу загружают 5,8 г 2-циано-1-диметилсульфамоил-4(5)-фенилтиоимидазола, который получен в (2), 150 мл осушенного тетрагидрофурана в атмосфере азота и к этой смеси по каплям добавляют 12,9 мл 1,6-молярного раствора н-бутиллития в гексане (производство фирмы Канте Кагаку), причем температуру смеси поддерживают при -75оС или ниже (с помощью смеси сухой лед/ацетон). После завершения капельного добавления смесь выдерживают при той же температуре в течение 15 мин, по каплям добавляют к смеси при -70оС или ниже 20 мл раствора 3,2 г дифенилсульфида в тетрагидрофуране. После этого смеси дают нагреться до комнатной температуры. По окончании взаимодействия реакционную смесь экстрагируют этилацетатом. Экстракт промывают водой и сушат над безводным сульфатом натрия. Растворитель удаляют путем перегонки, остаток очищают хроматографически на колонке с силикагелем (проявляющий растворитель - хлористый метилен) и выделяют, получая 1,7 г 2-циано-1-диметилсульфамоил-4,5-дифенилтиоимидазола (соединение N 38), имеющего температуру плавления 98-101оС. Пример синтеза 14. Синтез 4-бром-2-циано-1-диметилсульфамоил-5-н-пропилими- дазола (соединение N 109-б). (1). 2-Циано-4,5-дибром-1-диметилсульфамоилимидазол, имеющий температуру плавления 118-120оС, синтезируют из 2-циано-4,5-диброимидазола, имеющего температуру плавления 200-203оС. (2). В четырехгорлую колбу емкостью 20 мл, загружают 5 г 2-циано-4,5-дибром-1-диметилсульфамоилимидазола, который получен в (1), и 120 мл осушенного тетрагидрофурана в токе азота. Поддерживая температуру смеси при -75оС или ниже (смесью сухой лед/ацетон), в нее постепенно по каплям добавляют 9,6 мл 1,6-молярного раствора н-бутиллития в гексане (производство фирмы Альдрих). После окончания капельного добавления систему выдерживают при той же температуре в течение 15 мин. Затем к смеси по каплям добавляют раствор 3,6 г иодистого п-пропила в 15 мл тетрагидрофурана при -75оС или ниже. При перемешивании смеси дают постепенно нагреться до комнатной температуры. После завершения взаимодействия реакционную смесь экстрагируют этилацетатом. После промывания водой экстракт сушат над безводным сульфатом натрия. Этилацетат удаляют путем перегонки, остаток очищают хроматографически на колонке с силикагелем (проявляющий растворитель - хлористый метилен), получая 2,1 г 4-бром-2-циано-1-диметилсульфамоил-5-н-пропил- имидазола (соединение N 109-б), имеющего температуру плавления 93-94оС. Типичные примеры имидазодовых веществ (общая формула (1)) изобретения приведены в табл. 1. Среди имидазодовых соединений изобретения приведенных в табл. 1, соединения в номерах которых имеется индекс "а" охватываются общей формулой (1-а) в общей формуле (1), приведенной выше, а соединения, в номерах которых имеется индекс "б", охватываются общей формулой (1-б) в общей формуле (1). R где радикалы R2/ R3/ R4/ R6 и Y имеют указанные значения. Способ /А/ и Стадия-1 способов /В/ - /Д// описанных выше/ проводятся/ если это необходимо и желательно/ в присутствии растворителя и акцептора кислоты. Примеры раствотителя включают ароматические углеводороды/ такие как бензол/ толуол/ксиол/ хлорбензол/ и др; циклические и ациклические алифатические углеводороды/ такие как хлороформ/ четыреххлористый углерод/ хлористый метилен/ дихлорэтан/ трихлорэтан/ н-гесан/ циклогексан и др.; простые эфиры; также как диэтиловый эфир, диоксан, тетрагидрофуран и др.; кетоны, такие как ацетон, метилэтилкетон, метилизобутилкетон и др.; нитрилы, такие как ацетонитрил, пропионитрил и др.; и апротонные полярные растворители, такие как диметилформамид, N-метилпирролидон, диметилсульфоксид, сульфолан и другие. В качестве акцептора кислоты может использоваться любое из неорганических и органических оснований. Примеры неорганического основания включают гидроксиды щелочных металлов, такие как гидроксид натрия, гидроксид калия и др.; карбонаты щелочных или щелочно-земельных металлов, такие как безводный карбонат калия, безводный карбонат кальция и др.; гидриды щелочных металлов, такие как гидрид натрия; щелочные металлы, такие как металлический натрий и другие. Кроме того, в качестве органического основания может быть упомянут триэтиламин и другие. Описанная реакция может быть осуществлена в присутствии подходящего катализатора. В качестве катализатора может быть упомянут, например, катализатор фазового переноса, такой как производная четвертичного аммония. В качестве атома галогена, показанного как Y в общей формуле (III), описанной выше, могут быть упомянуты атом хлора, брома, иода и атом фтора, из которых предпочтительным является атом хлора. Пример синтеза 1. Синтез 2-циано-1-диметилсульфамоил-5-фенилтиоимидазола (соединение N 45-б). В четырехгорлую колбу загружают 12,0 г 2-циано-1-диметилсульфамоилимидазола (Compound N 1) и 240 мл осушенного тетрагидрофурана в потоке азота. Поддерживая температуру смеси при -75оС или ниже смесью сухого льда с ацетоном, к смеси постепенно, по каплям добавляют 41,3 мл раствора н-бутиллития в гексане (1,6 молярный) производство фирмы "Альдрих"). После завершения капельного добавления, систему выдерживают в течение 15 мин при той же температуре. Затем при -70оС или ниже к смеси по каплям добавляют раствор 17 г дифенилдисульфида в 30 мл тетрагидрофурана. При перемешивании в течение ночи температуру смеси постепенно повышают до комнатной. После завершения взаимодействия реакционную смесь выливают в воду. Проводят экстракцию 500 мл этилацетата. После промывания водой экстракт сушат над безводным сульфатом натрия. Этилацетат удаляют путем перегонки и остаток очищают хроматографически на колонке с силикагелем (проявляющий растворитель : хлористый метилен), получая 4,3 г 2-циано-1-диметилсульфамоил-5-фенилтио- имидазола (соединение N 45-б), имеющего температуру плавления 106-107оС. Пример синтеза 2. Синтез 4-хлор-2-циано-1-диметилсульфамоил-5-н-пропилами-дазола (соединение N 48-б). (1). 2-Циано-1-диметилсульфамоил-5-н-пропилимидазол (4,8 г), имеющий температуру плавления 51-52оС (соединение N 48-б), синтезируют путем взаимодействия 12,0 г 2-циано-1-диметилсульфамоилимидазола и 15,3 г н-пропилиодида по способу, который аналогичен описанному в примере синтеза 1. (2). 2-Циано-1-диметилсульфамоил-5-н-пропилимидазол (4,8 г), такой как получен выше в (1), 40 мл пиридина и 11,4 г хлористого пиридиния смешивают и смесь перемешивают 4 ч при 90оС. После завершения взаимодействия пиридин удаляют из реакционной смеси путем перегонки и остаток экстрагируют этилафетатом. Экстракт промывают водой и затем сушат над безводным сульфатом натрия. После этого этилацетат удаляют путем перегонки и остаток очищают хроматографически а колонке с силикагелем (проявляющий растворитель : смесь этилацетата и н-гексана) и при выделении получают 2,46 г 2-циано-4(5)-н-пропилимидазола (промежуточное соединение), имеющее температуру плавления 52-54оС. (3) 2-Циано-4(5)-н-пропилимидазол, такой как получен в (2), 80 мл хлороформа и 2,6 г N-хлорсукцинимида смешивают, и смесь подвергают взаимодействию в течение 4 ч при температуре кипения с обратным холодильником. После завершения взаимодействия к реакционной смеси добавляют 200 мл воды. Образовавшийся органический слой промывают водой и затем сушат над безводным сульфатом натрия. После сушки хлороформ удаляют путем перегонки, и остаток очищают хроматографически на колонке с силикагелем (проявляющий растворитель - смесь 1:1 этилацетата и н-гексана), и при выделении получают 2,2 г 4(5-хлор)2-циано-5(4)-н-пропилимидазола (промежуточное соединение), имеющего температура плавления 107-109оС. (4). 4(5)-Хлор-2-циано-5(4)-н-пропилимидазол (2,0 г) такой, как получен выше в (3), 30 мл ацетонитрила, 1,95 г безводного карбоната калия и 1,86 г хлористого диметилсульфамоила смешивают и после постепенного повышения температуры, смесь подвергают взаимодействию при температуре кипения с обратным холодильником в течение 1 ч. После завершения взаимодействия ацетонитрил удаляют путем отгонки из реакционной смеси. После вливания 100 мл воды к остатку, образовавшуюся смесь экстрагируют 50 мл хлористого метилена. Экстракт промывают водой и сушат над безводным сульфатом натрия. После этого хлористый метилен удаляют путем перегонки. Остатку дают отстояться в течение ночи, после чего анализ смеси показал, что один из двух изомеров в смеси разложился и превратился в исходный 4(5)-хлор-2-циано-5(4)-н-пропилимидазол. Остаток, содержащий другой изомер, очищают хроматографически на колонке с силикагелем (проявляющий растворитель : хлористый метилен) и при выделении получают 1,1 г 4-хлор-2-циано-1-диметилсульфамоил-5-н-пропилимидазола (соединение N 48-б), имеющего температуру плавления 64-66оС. Пример синтеза 3. Синтез 2-циано-1-диметилсульфамоил-4(5)-фенилимидазола (соединение N 1). (1). В 320 мл ацетона растворяют 23,04 г 4(5)-фенилимидазола и к раствору добавляют 12,14 г безводного карбоната калия. Смесь нагревают при температуре кипения с обратным холодильником в течение 2 ч. После охлаждения к смеси по каплям добавляют 45 мл ацетонового раствора, содержащего 25,26 г хлористого диметилсульфамоила. После завершения капельного добавления, смесь нагревают при температуре кипения с обратным холодильником в течение 4,5 ч, чтобы реакция завершилась. После завершения взаимодействия, реакционную смесь охлаждают и твердые вещества удаляют путем фильтрации. После удаления растворителя путем отгонки при пониженном давлении остаток очищают хроматографически на колонке с силикагелем (проявляющий растворитель : хлористый метилен), получая 27,8 г 1-диметилсульфамоил-4(5)-фенилимидазола, имеющего температуру плавления 96-100оС. (2). В 290 мл тетрагидрофурана растворяют 17 г 1-диметилсульфамоил-4(5)-фенилимидазола, такого как получен выше в (1). Этот раствор охлаждают до -70оС в токе азота и к смеси в течение 30 ми по каплям добавляют 51 мл 1,6-молярного раствора н-бутиллития в гексане. После завершения капельного добавления реакционную смесь перемешивают при -70оС в течение 30 мин. Затем к смеси добавляют по каплям 12 мл тетрагидрофуранового раствора, содержащего 6 г N,N-диметилформамида. После завершения капельного добавления реакционную смесь подвергают взаимодействию в течение 15 ч при перемешивании, в то время как ее температура медленно повышается до комнатной. После завершения взаимодействия реакционную смесь выливают в воду со льдом и экстрагируют этилацетатом. После промывания экстрагированного слоя водой, этот слой сушат над безводным сульфатом натрия. Отгоняют растворитель при пониженном давлении, и остаток очищают хроматографически на колонке с силикагелем (проявляющий растворитель - смесь 1:2 этилацетат : н-гексан), получая 12,8 г 1-диметилсульфамоил-2-формил-4(5)-фенилими- дазола, имеющего температуру плавления 86-89оС. (3). В 120 мл пиридина растворяют 11,16 г 1-диметилсульфамоил-2-формил-4(5)-фенилимидазола, такого как получен выше в (2), и 5,56 г хлористоводородного гидроксиламина, и 24 мл уксусного ангидрида добавляют по каплям к раствору при комнатной температуре. После завершения капельного добавления температуру смеси постепенно повышают и смесь реагирует при 100оС в течение 12 ч. После завершения взаимодействия растворитель из реакционной смеси удаляют путем перегонки при пониженном давлении. Затем к остатку добавляют 125 мл воды и выпавшее в осадок твердое вещество отделяют путем фильтрации. Неочищенный продукт растворяют в этилацетате и очищают хроматографически на колонке с силикагелем (проявляющий растворитель : этилацетат), получая 5,55 г 2-циано-4(5)-фенилимидазола, имеющего температуру плавления 208-205оС. (4). В 88 мл ацетона растворяют 1,7 г 2-циано-4(5)-фенилимидазола, такого как получен выше в (3), и к раствору добавляют 1,7 г безводного карбоната калия. Смесь нагревают при температуре кипения с обратным холодильником в течение 2 ч. После охлаждения к смеси по каплям добавляют 6 мл ацетонового раствора, содержащего 1,7 г хлористого диметилсульфамоила. После завершения капельного добавления смесь нагревают при температуре кипения с обратным холодильником 2 ч для завершения реакции. После завершения взаимодействия реакционную смесь охлаждают, и твердое вещество удаляют путем фильтрации. После удаления растворителя путем перегонки при пониженном давлении, остаток экстрагируют этилацетатом. Экстракт промывают водой и сушат над безводным сульфатом натрия. Растворитель удаляют путем перегонки при пониженном давлении и получают 2 г 2-циано-1-диметилсульфамоил-4(5)-фенил- имидазола (соедиение N 1), имеющего температуру плавления 101-102оС. Пример синтеза 4. Синтез 4(5)-хлор-2-циано-1-диметилсульфамоил-5(4)-фенил- имидазола (соединение N 7) и 4-хлор-2-циано-1-диметилсульфамоил-5-фенилимидазола (соединение N 7-б). (1). В 100 мл хлороформа растворяют 1,352 г 2-циано-4(5)-фенилимидазола и к раствору добавляют 1,175 г п-хлорсукцинимида. Эта смесь взаимодействует при нагревании до температуры кипения с обратным холодильником в течение 4 ч. После завершения взаимодействия реакционную смесь выливают в воду и экстрагируют хлороформом. После промывания водой экстрагированный слой сушат над безводным сульфатом атрия. Растворитель отгоняют при пониженном давлении, и остаток очищают хроматографически на колонке с силикагелем (проявляющий растворитель : хлористый метилен), получая 1,28 г 4(5)-хлор-2-циано-5(4)-фенилимидазола (промежуточное соединение), имеющего температуру плавления 149-151оС. (2). В 6 мл ацетона растворяют 0,43 г 4(5)-хлор-2-циано-5(4)-фенилимидазола, который получен в (1), к раствору добавляют 0,29 г безводного карбоната калия и 0,36 г хлористого диметилсульфамоила. Эта смесь взаимодействует при нагревании до температуры кипения с обратным холодильником в течение 30 мин. После завершения взаимодействия реакционную смесь выливают в воду и экстрагируют этилацетатом. После промывания водой экстрагированный слой сушат над безводным сульфатом натрия. Растворитель отгоняют при пониженном давлении, и остаток затем очищают хроматографически на колонке с силикагелем (проявляющий растворитель : хлористый метилен), получая 0,5 г 4(5)-хлор-2-циано-1-диметилсульфамоил-5(4)фенилимидазола (соединение N 7), имеющее температуру плавления 106-109оС. В результате анализа с помощью спектров ЯМР, описанное выше соединение является смесью изомеров 4-хлор-2-циано-1-диметилсульфа- моил-5-фенилимидазола и 5-хлор-2-циано-1-диметилсульфамоил-4-фенилимидазола в почти равных отношениях. (3). После выдерживания в течение 24 ч при комнатной температуре 2,9 г смеси этих изомеров, которая получена способом, аналогичным описанному в (2), ее очищают хроматографически на колонке с силикагелем (проявляющий растворитель : хлористый метилен), получая 1,15 г 4-хлор-2-циано-1-диметилсульфамоил-5-фенилимидазола (соединение N 7-о), имеющего температуру плавления 109-112оС. Кроме того, посредством очистки и выделения из этого соединения было также получено 0,7 г 4(5)-хлор-2-циано-5(4)-фенилимидазола (промежуточное соединение). Пример синтеза 5. Синтез 4(5)-хлор-2-циано-1-диметилсульфамоил-5(4)-(4)-метил- фенил)имидазола (соединение N 8) и 4-хлор-2-циано-1-диметилсульфамоил-5-(4- метилфенил)имидазола (соединение N 8-б). Смесь изомеров (соединение N 8), имеющая температуру плавления 101-108оС, 4-хлор-2-циано-1-диметилсульфамоил-5-(4-ме- тилфенил)имидазол и 5-хлор-2-циано-1-диметилсульфамоил-4-(4-метилфенил)имидазол, была получена из 4(5)-(4-метилфенил)имидазола в отношении 6: 4 способом, аналогичным примерам синтезов 4 и 5, которые описаны выше. После того, как 0,75 г смеси изомеров прореагируют при 40оС в течение 8 ч, реакционную смесь очищают хроматографически на колонке с силикагелем (проявляющий растворитель : хлористый метилен), получая 0,45 г 4-хлор-2-циано-1-диметилсульфамоил-5-(4-метилфенил)имидазола (соединение N 8-б), имеющего температуру плавления 133-134оС. Кроме того, путем очистки и выделения из этого соединения также получают 0,15 г 4(5)-хлор-2-циано-5(4)-(4-метилфенил)имидазола, имеющего температуру плавления 124-129оС. Пример синтеза 6. Синтез 4(5)-хлор-5(4)-(4-хлорефнил)-2-циано-1-диметилсульфамоил- имидазола (соединение N 12), 4-хлор-5-(4-хлорфенил)-2-циано-1-диметилсульфамо- илимидазола (соединение N 12-б) и 5-хлор-4-(4-хлорфенил-2-циано-1-диметилсульфа-моилимидазола (соединение N 12-а). Способом, который аналогичен примерам синтеза 4 и 5, описанным выше, 0,80 г изомерной смеси (соединение N 12), имеющей температуру плавления около 108оС, 4-хлор-5-(4-хлорфенил)-2-циано-1-диметил- сульфамоилимидазола и 5-хлор-4-(4-хлорфенил)-2-циано-1-диметилсульфамоилими- дазола, получают из 4(5)-(4-хлорфенил)-имидазола. Смесь изомеров очищают хроматографически на колонке с силикагелем (проявляющий растворитель : хлористый метилен). Элюат второй фракции концентрируют и подвергают перекристаллизации из хлористого метилена, получая 0,16 г 4-хлор-5-(4-хлорфенил) -2-циано-1-диметилсульфамо-илимидазола (соединение N 12-б), имеющего температуру плавления 117-120оС. Кроме того, элюат первой фракции концентрируют таким же образом, получая 0,50 г 5-хлор-4-(4-хлорфенил)-2-циано-1-диметил- сульфамоилимидазола (соединение N 12-а), имеющего температуру плавления 133-138оС. Пример синтеза 7. Синтез 1-диметилсульфамоил-4(5)-фенилимидазол-2-карбо- тиоамида (соединение N 23). В 30 мл диоксана растворяют 1,0 г 2-циано-1-диметилсульфамоил-4(5)-фенилими-дазол (соединение N 1) и к раствору добавляют 0,36 г триэтиламина. Смесь нагревают до температуры 40-50оС при перемешивании, вводят в нее газообразный сероводород в течение 1 ч и 25 мин. После этого смесь реагирует при 40-50оС еще в течение 50 мин. После завершения взаимодействия реакционную смесь охлаждают, выливают в воду и экстрагируют этилацетатом. После промывания водой экстрагированный слой сушат над безводным сульфатом натрия. Растворитель отгоняют при пониженном давлении и остаток очищают хроматографически на колонке с силикагелем (проявляющий растворитель - смесь 1:3 этилацетата и н-гексана), получая 0,8 г 1-диметилсульфамоил-4(5)-фенилимидазол-2-карботиоамида (соединение N 23), имеющего температуру плавления 155-175оС. Кроме того, в небольшом количестве получают кристаллы 4(5)-фенилимидазол-2-карботиоамида. Пример синтеза 8. Синтез 2-циано-1-изопропилсульфонил-4(5)-фенилимидазол (соединение N 32). При комнатной температуре смешивают 1 г 2-циано-4(5)-фенилимидазола, 0,98 г безводного карбоната калия и 30 мл ацетонитрила. После взаимодействия в течение 2 ч при температуре кипения реакционную смесь охлаждают, раствор 1,0 г хлористого изопропилсульфонила в 5 мл ацетонитрила добавляют к смеси. Эта смесь снова реагирует при температуре кипения в течение 1,5 ч. После завершения реакции реакционную смесь выливают в воду. Проводят экстракцию хлористым метиленом. После промывания водой экстракт сушат над безводным сульфатом натрия. Растворитель удаляют путем перегонки при пониженном давлении, остаток очищают хроматографически на колонке с силикагелем (проявляющий растворитель : хлористый метилен), получая 1,4 г 2-циано-1-изопропилсульфонил-4(5)-фенилимидазола (соединение N 32), имеющего температуру плавления 80-83оС. Пример синтеза 9. Синтез 4(5)-(2-тиенил)-2-циано-1-диметилсульфамоилимида-зола (соединение N 3). (1). К 150 мл формамида добавляют 25 г 2-(бромацетил)тиофена. Смесь подвергают взаимодействию при 180-190оС в течение 2 ч. После завершения взаимодействия реакционную смесь выливают в воду и добавляют в нее концентрированную соляную кислоту для того, чтобы сделать систему кислотной. Затем проводят промывание хлористым метиленом. После нейтрализации аммиачной водой, водную фазу экстрагируют хлористым метиленом. После промывания водой экстракт сушат над безводным сульфатом натрия. Растворитель удаляют путем перегонки при пониженном давлении, получая 11 г 4(5)-(2-тиенил)-имидазола. (2). К 200 мл ацетонитрила добавляют 11,6 г хлористого диметилсульфамоила, 11,1 г безводного карбоната калия и 11 г 4(5)-(2-тиенил)имидазола, который получен выше в (1). При перемешивании эта смесь реагирует в течение 2 ч. После завершения взаимодействия реакционную смесь выливают в воду. Проводят экстракцию этилацетатом. После промывания водой экстракт сушат над безводным сульфатом натрия. Растворитель удаляют путем перегонки при пониженном давлении, получая 14,5 г 4(5)-(2-тиенил)-1-диметилсульфамоилимидазола. (3). В 120 мл безводного тетрагидрофурана растворяют 9,5 г 4(5)-(2-тиенил)-1-диметилсульфамоилимидазола, который получен выше в (2). В токе азота при -78оС к раствору по каплям добавляют 26,2 мл 1,6-молярного раствора н-бутиллития в гексане, смесь перемешивают при той же температуре в течение 15 мин. Затем к смеси по каплям добавляют 20 мл тетрагидрофуранового раствора, в котором растворено 5,4 г N,N-диметилформамида. После завершения капельного добавления, температуру смеси постепенно повышают до комнатной для того, чтобы реакция завершилась. После завершения взаимодействия реакционную смесь выливают в воду. Проводят экстракцию этилацетатом. После промывания водой экстракт сушат над безводным сульфатом атрия. Растворитель удаляют путем перегонки при пониженном давлении, получая 5,4 г 4(5)-(2-тиенил)-2-формил-1-диметилсульфамоилимидазола. (4). В 54 мл пиридина растворяют 2,6 г хлористоводородного гидроксиламина и 5,4 г 4(5)-(2-тиенил)-2-формил-1-диметилсульфамоилимидазола, который получен в (3). Раствор перемешивают при комнатной температуре в течение 15 мин. Затем к раствору постепенно добавляют 10 мл уксусного ангидрида, после чего осуществляют реакцию при 60-70оС в течение 2 ч. После завершения взаимодействия, реакционную смесь выливают в воду. Проводят экстракцию этилацетатом. После промывания водой экстракт сушат над безводным сульфатом натрия. Растворитель удаляют путем перегонки при пониженном давлении и остаток очищают хроматографически на колонке с силикагелем (проявляющий растворитель - смесь 2:1 этилацетата и н-гексана), получая 1,2 г 4(5)-(2-тиенил)-2-цианоимидазола, имеющего темпеpатуpу плавления 195-203оС. (5). К 50 мл ацетонитрила добавляют 1,1 г хлористого диметилсульфамоила, 1,0 г безводного карбоната калия и 1,2 г 4(5)-(2-тиенил)-2-цианоимидазола, который получен выше в (4). Эта смесь взаимодействует при температуре кипения в течение 2 ч. После завершения взаимодействия реакционную смесь выливают в воду и экстрагируют этилацетатом. После высушивания экстракта над безводным сульфатом натрия растворитель удаляют путем перегонки при пониженном давлении, остаток очищают хроматографически на колонке с силикагелем (проявляющий растворитель - хлористый метилен), получая 1,3 г 4(5)-(2-тиенил)-2-циано-1-диметилсульфа- моилимидазола (соединение N 3), имеющего температуру плавления 145-150оС. Пример синтеза 10. Синтез 4(5)-хлор-2-циано-1-диметилсульфамоил-5(4)-изопро-пилимидазола (соединение N 125) и 4-хлор-2-циано-11-диметилсульфамоил-5-изопро-пилимидазола (соединение N 86-б). (1). Нагревают до 180оС 360 г формамида и добавляют к нему по каплям в течение 30 мин 102 г 1-гидрокси-3-метил-2-бутанола (приготовленного по способу, описанному Липшутцом и Морей в I.Org.Chem. том 48, 3745 (1983). После завершения капельного добавления смесь реагирует при 180оС в течение 1 ч. После завершения взаимодействия реакционную смесь охлаждают и выливают в ледяную воду. Образовавшуюся смесь подкисляют до рН между 4 и 5 аммиачной водой. К нему добавляют 5 г активированного древесного угля, смесь перемешивают в течение 1 ч. Активированный древесный уголь удаляют путем фильтрации, и фильтрат подщелачивают до рН 8 аммиачной водой. Затем проводят экстракцию хлористым метиленом, и экстракт сушат над безводным сульфатом натрия. Растворитель удаляют путем перегонки при пониженном давлении, получая 13 г 4(5)-изопропилимидазола. (2). В 300 мл ацетонитрила растворяют 11,8 4(5)-изопропилимидазола, который получен выше в (1), к раствору добавляют 18 г безводного карбоната калия. Смесь кипятят с обратным холодильником в течение 30 мин, после охлаждения к ней по каплям добавляют 17 г хлористого диметилсульфамоила. После завершения капельного добавления смесь кипятят, чтобы реакция завершилась. После завершения взаимодействия реакционную смесь охлаждают, выливают в воду и затем экстрагируют этилацетатом. Экстрагированный слой промывают водой и сушат над безводным сульфатом натрия. Растворитель удаляют путем перегонки при пониженном давлении, остаток очищают хроматографически на колонке с силикагелем (проявляющий растворитель : хлористый метилен), получая 13 г 1-диметилсульфамоил-4(:)-изопропилими-дазола. (3). В 200 мл тетрагидрофурана растворяют 13 г 1-диметилсульфамоил-4(5)-изопропилимидазола, который получен в (2). Этот раствор охлаждают до -70оС в токе азота и добавляют к нему по каплям в течение 15 мин 38 мл 1,6 молярного раствора н-бутиллития в гексане. После завершения капельного добавления смесь перемешивают при -70оС в течение 30 мин. После капельного добавления 5,6 г N,N-диметилформамида смесь реагирует при перемешивании в течение 15 мин, в то время как ее температура медленно повышается до комнатной. После завершения взаимодействия реакционную смесь выливают в ледяную воду и экстрагируют этилацетатом. Экстрагированный слой промывают водой и сушат над безводным сульфатом натрия. Растворитель отгоняют при пониженном давлении, получая 8,6 г 1-диметилсульфамоил-2-формил-4(5)-изопропилимидазола. (4). В 100 мл пиридина растворяют 8,5 г 1-диметилсульфамоил-2-формил-4(5)-изо- пропилимидазола, который получен в (3), 4,8 г хлористоводородного гидроксиламина, к этому раствору по каплям добавляют 10 мл уксусного ангидрида при комнатной температуре. После завершения капельного добавления, температуру смеси постепенно повышают, смесь реагирует 5 ч при 80-90оС. После завершения взаимодействия из реакционной смеси отгоняют растворитель при пониженном давлении. К остатку добавляют воду, смесь экстрагируют этилацетатом. Экстрагированный слой промывают разбавленной соляной кислотой и затем водой, сушат над безводным сульфатом натрия. Растворитель отгоняют перегонки при пониженном давлении, получая 2,35 г 2-циано-4(5)-изопропилимидазола (промежуточное соединение), имеющее температуру плавления 88-91оС. (5). В 80 мл метанола растворяют 2 г 2-циано-4(5)-изопропилимидазола, который получен выше в (4), и к раствору добавляют 2,1 г п-хлорсукцинимида. Смесь перемешивают при комнатной температуре в течение 20 ч и затем подвергают взаимодействию при 40оС в течение 8 ч. После завершения взаимодействия из реакционной смеси при пониженном давлении отгоняют метанол. К остатку добавляют воду, смесь экстрагируют этилацетатом. Экстрагированный слой промывают водой над безводным сульфатом натрия. Растворитель отгоняют при пониженном давлении, и остаток очищают хроматографически на колонке с силикагелем (проявляющий растворитель : хлористый метилен), получая 1,67 г 4(5)-хлор-циано-5(4)-изопропилимидазола, имеющего температуру плавления 84-87оС. (6). В 30 мл ацетонитрила растворяют 1,6 г 4(5)-хлор-2-циано-5(4)-изопропилимидазола, который получен выше в (5), к раствору добавляют 1,56 г безводного карбоната калия. Смесь кипятят с обратным холодильником в течение 30 мин. После охлаждения в нее добавляют 1,49 г диметилсульфамоилхлорида по каплям. После завершении капельного добавления смесь кипятят в течение 15 мин, чтобы взаимодействие завершилось. После окончания взаимодействия реакционную смесь охлаждают, выливают в воду и затем экстрагируют этилацетатом. Экстрагированный слой промывают водой и сушат над безводным сульфатом натрия. Растворитель отгоняют при пониженном давлении, остаток очищают хроматографически на колонке с силикагелем (проявляющий растворитель - хлористый метилен), получая 2,1 г 4(5)-хлор-2-циано-1-сульфамоил-5(4)-изопропилимидазола (соединение N 86). В результате анализа с помощью спектров ЯМР установлено, что описанное соединение является смесью изомеров 4-хлор-2-циано-1-диметилсульфамоил-5- изопропилимидазола и 5-хлор-2-циано-1-диметилсульфамоил-4-изопропилимидазола в примерном соотношении 2:1. (7). После выдерживания в течение 5 сут при комнатной температуре 2,1 г смеси изомеров, полученной в (6), подвергают хроматографической очистке на колонке с силикагелем (проявляющий растворитель - хлористый метилен), получая 1 г 4-хлор-2-циано-1-диметилсульфамоил-5-изопропил- имидазола (соединение N 86-б), имеющего температуру плавления 75-82оС (разлагается). Кроме того путем очистки и выделения из этого соединения также получают 4(5)-хлор-2-циано-5(4)-изопропилимидазол. Пример синтеза 11. Синтез 4-хлор-1-диметилсульфамоил-5-н-пропилимидазол-2-карботиоамида (соединение N 129-б). (1). В четырехгорлую колбу загружают 6, г 2-циано-4,5-дихлор-1-диметилсульфамоилимидазола, имеющего температуру плавления 100-103оС, и 180 мл осушенного тетрагидрофурана в токе азота. Поддерживая температуру смеси при -70оС или ниже (с помощью смеси сухой лед/ацетон) к смеси постепенно по каплям добавляют 15,3 мл 1,6 молярного раствора н-бутиллития в гексане (производство фирмы Альдрих). После завершения капельного добавления систему выдерживают при этой температуре в течение 15 мин. Затем к смеси при -70оС или ниже по каплям добавляют раствор 5,7 г н-проилиодида в 15 мл тетрагидрофурана. При перемешивании в течение ночи температура смеси постепенно повышается до комнатной. После завершения взаимодействия реакционную смесь выливают в воду. Проводят экстракцию хлористым метиленом (500 мл). После промывания водой экстракт сушат над безводным сульфатом натрия. Хлористый метилен удаляют путем перегонки, остаток очищают хроматографически на колонке с силикагелем (проявляющий растворитель - хлористый метилен) и затем снова очищают хроматографически на колонке с силикагелем (проявляющий растворитель - смесь этилацетата и н-гексана), получая 2,8 г 4-хлор-2-циано-1-диметилсульфамоил-5-н-пропилимидазола (соединение N 48-б), имеющего температуру плавления 66-68оС. (2). В четырехгорлую колбу загружают 2,7 г 4-хлор-2-циано-1-диметилсульфамоил-5-н-пропилимидазола, который получен в (1), 40 мл диоксана, 1,0 г триэтиламина и 0,8 г пиридина. В эту смесь вводят газообразный сероводород при 20-25оС, приблизительно в течение 30 мин, до тех пока не прореагируют исходные материалы. После завершения взаимодействия реакционную смесь выливают в воду, а выпавшие в осадок кристаллы отфильтровывают на фильтре Нутча и сушат. Образовавшиеся кристаллы очищают хроматографически на колонке с силикагелем (проявляющий растворитель - хлористый метилен) и выделяют, получая 2,3 г 4-хлор-1-диметилсульфамоил-5-н-пропилимидазола (соединение N 129-б), имеющего температуру плавления 160-162оС. Пример синтеза 12. Синтез N-пропионил-4-хлор-1-диметилсульфамоил-5-н-про-пилимидазола-2- карботиоамида (соединение N 121-б). В четырехгорлую колбу загружают 2,0 г 4-хлор-1-диметилсульфамоил-5-н-пропил-имидазол-2-карботиоамида (соединение N 121-в), 24 мл ацетона и 1,12 г пиридина. К смеси при 0-5оС по каплям добавляют 1,19 г хлористого пропионила. После завершения капельного добавления взаимодействие осуществляют при 30-35оС в течение 1 ч и при температуре кипения с обратным холодильником еще в течение 30 мин при перемешивании. После завершения взаимодействия, реакционную смесь выливают в воду и экстрагируют этилацетатом. Экстрагированный слой промывают водой и сушат над безводным сульфатом натрия. После этого этилацетат удаляют при перегонке, а остаток очищают хроматографически на колонке с силикагелем (проявляющий растворитель - хлористый метилен) и выделяют, получают 1,02 г N-пропионил-4-хлор-1-диметилсульфамоил-5-н-пропилимидазол-2- карботиоамида (соединение N 121-б), имеющего температуру плавления 150-152оС. Пример синтеза 13. Синтез 2-циано-1-диметилсульфамоил-4,5-дифенилтиоимида- зол (соединение N 38). (1). 2-Циано-1-диметилсульфамоил-5-фенилтиоимидазол (8,0 г, соединение N 45-б), полученный так же, как в примере синтеза N 1, описанном выше, 60 мл метанола и 60 мл 7%-ной соляной кислоты загружают в колбу, смесь подвергают взаимодействию при перемешивании при 40-50оС в течение 2 ч. После завершения взаимодействия реакционную смесь слегка подщелачивают аммиаком, осажденные кристаллы отделяют путем фильтрации и сушат, получая 4,2 г 2-циано-4(5)-фенилтиоимидазола, имеющего температуру плавления 166-169оС. (2). К смеси 4,2 г 2-циано-4(5)-фенилтиоимидазола, полученного выше в (1), 80 мл ацетонитрила и 3,1 г безводного карбоната калия добавляют 3,4 г хлористого диметилсульфамоила. Образовавшуюся смесь подвергают взаимодействию при температуре кипения с обратным холодильником в течение 1 ч. После завершения взаимодействия реакционную смесь охлаждают, твердые вещества отфильтровывают. Растворитель из фильтра удаляют путем перегонки, а остаток очищают хроматографически на колонке с силикагелем (проявляющий растворитель - хлористый метилен) и выделяют, получая 5,8 г 2-циано-1-диметилсульфамоил-4(5)-фенилтиоимидазола. (3). В четырехгорлую колбу загружают 5,8 г 2-циано-1-диметилсульфамоил-4(5)-фенилтиоимидазола, который получен в (2), 150 мл осушенного тетрагидрофурана в атмосфере азота и к этой смеси по каплям добавляют 12,9 мл 1,6-молярного раствора н-бутиллития в гексане (производство фирмы Канте Кагаку), причем температуру смеси поддерживают при -75оС или ниже (с помощью смеси сухой лед/ацетон). После завершения капельного добавления смесь выдерживают при той же температуре в течение 15 мин, по каплям добавляют к смеси при -70оС или ниже 20 мл раствора 3,2 г дифенилсульфида в тетрагидрофуране. После этого смеси дают нагреться до комнатной температуры. По окончании взаимодействия реакционную смесь экстрагируют этилацетатом. Экстракт промывают водой и сушат над безводным сульфатом натрия. Растворитель удаляют путем перегонки, остаток очищают хроматографически на колонке с силикагелем (проявляющий растворитель - хлористый метилен) и выделяют, получая 1,7 г 2-циано-1-диметилсульфамоил-4,5-дифенилтиоимидазола (соединение N 38), имеющего температуру плавления 98-101оС. Пример синтеза 14. Синтез 4-бром-2-циано-1-диметилсульфамоил-5-н-пропилими- дазола (соединение N 109-б). (1). 2-Циано-4,5-дибром-1-диметилсульфамоилимидазол, имеющий температуру плавления 118-120оС, синтезируют из 2-циано-4,5-диброимидазола, имеющего температуру плавления 200-203оС. (2). В четырехгорлую колбу емкостью 20 мл, загружают 5 г 2-циано-4,5-дибром-1-диметилсульфамоилимидазола, который получен в (1), и 120 мл осушенного тетрагидрофурана в токе азота. Поддерживая температуру смеси при -75оС или ниже (смесью сухой лед/ацетон), в нее постепенно по каплям добавляют 9,6 мл 1,6-молярного раствора н-бутиллития в гексане (производство фирмы Альдрих). После окончания капельного добавления систему выдерживают при той же температуре в течение 15 мин. Затем к смеси по каплям добавляют раствор 3,6 г иодистого п-пропила в 15 мл тетрагидрофурана при -75оС или ниже. При перемешивании смеси дают постепенно нагреться до комнатной температуры. После завершения взаимодействия реакционную смесь экстрагируют этилацетатом. После промывания водой экстракт сушат над безводным сульфатом натрия. Этилацетат удаляют путем перегонки, остаток очищают хроматографически на колонке с силикагелем (проявляющий растворитель - хлористый метилен), получая 2,1 г 4-бром-2-циано-1-диметилсульфамоил-5-н-пропил- имидазола (соединение N 109-б), имеющего температуру плавления 93-94оС. Типичные примеры имидазодовых веществ (общая формула (1)) изобретения приведены в табл. 1. Среди имидазодовых соединений изобретения приведенных в табл. 1, соединения в номерах которых имеется индекс "а" охватываются общей формулой (1-а) в общей формуле (1), приведенной выше, а соединения, в номерах которых имеется индекс "б", охватываются общей формулой (1-б) в общей формуле (1). R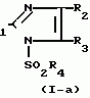 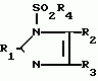  (1) Дополнительные характеристики соединений: соединение 18 Н-ЯМР (ацетон): 2,87 (С) м.д., 3,27 (С) м.д. 7,4-8,2 (м, 4Н) м.д. Найдено,%: С 36,4; Н 2,8; N 13,9. Вычислено,%: С 37,0; Н 2,6; N 14,4. Соединение 65-б Н-ЯМР (СДС13): 2,0-2,3 (м, 2Н) м.д. 2,7-3,3 (м, 8Н) м.д., 3,5-3,8 (т, 2Н) м.д., 6,97 (С, 1Н) м.д. Ниже описываются примеры испытаний фунгицидных композиций, предназначенных для уничтожения вредных микроорганизмов на сельскохозяйственных и садоводческих площадях в соответствии с изобретением. Стандарты оценки сельскохозяйственных и садоводческих фунгицидов удовлетворяют следующим критериям оценки, если не оговорено особо. Стандарты оценки. Эффект контроля определяют визуальным наблюдением степени заболевания испытуемого растения и выражают в соответствии со следующими 5 группами индексов контроля. (Индекс контроля) (Степень заболевания) 5: Поражение не наблюдается 4: Площадь, число или длительность поражения составляет менее 10% по сравнению с необработанным участком. 3: Площадь, число или длина поражений составляет менее 40% по сравнению с необработанным участком. 2: Площадь, число или длина поражений составляет менее 70% по сравнению с необработанным участком. 1: Площадь, число или длина поражений составляет менее 70% по сравнению с необработанным участком. Испытательный пример 1. Испытание на преветивное действие против настоящей мучнистой росы огурцов. Огурцы (культиватор : Сайс) культивируют в полиэтиленовой чаше диаметром 7,5 см. По достижении огурцами стадии одного листа, огуречные растения опрыскивают с помощью распылителя 10 мл раствора, полученного растворением препаративных форм по примерам 1-6,8,9 каждого из испытуемых соединений до определенной концентрации. После выдерживания чаш в температурной камере при 22-24оС в течение одного дня и одной ночи, проводят инокуляцию конидием грибка настоящей мучнистой росы (Sphacrotheca fuliqinca). Через десять дней после инокуляции используют площадь поражения первого листка и в соответствии со стандартами оценки приведенными выше, определяли индекс контроля. Полученные результаты представлены в табл. 2. Аналогичные результаты получены, когда используют любой из примеров получения форм. Испытательный пример 2. Испытание на превентивный эффект против антракноза огурцов. Огурцы (разновидность: Сайо) культивируют в полиэтиленовой чаше диаметром 7,5 см. После достижения огурцами стадии двух листьев огурцы опрыскивают из распылителя 10 мл раствора каждого из испытуемых соединений, взятых в определенной концентрации, полученного из препаративных форм. После выдерживания чаш в температурной камере при 22-24оС в течение одного дня и одной ночи, проводят инокуляцию суспензий спор грибка антракноза (Colletorechum lagenatium). Через семь дней после инокуляции исследуют площадь поражения первого листка и в соответствии со стандартами оценки, приведенными выше, определяют индекс контроля. Полученные результаты представлены в табл. 3. Испытательный пример 3. Испытание на превентивное действие против ложной мучнистой росы огурцов. Огурцы (разновидность: Сайо) культивируют в полиэтиленовой чаше диаметром 7,5 см. После достижения стадии двух листьев, огурцы опрыскивают 10 мл раствора каждого из испытуемых соединений взятых в определенной концентрации. После выдерживания чаш в термостате при 22-24оС в течение одного дня и одной ночи, проводят инокуляцию суспензией спор грибка ложной мучнистой росы (Pseudoperonospora eubensis). Через шесть дней после инокуляции площадь первого листка и в соответствии со стандартами оценки, приведенными выше, определяют индекс контроля. Полученные результаты представлены в табл. 4. Испытательный пример 4. Испытание на целебный эффект против ложной мучнистой росы огурцов. Огурцы (культиватор: Сайо) культивируют в полиэтиленовой чаше диаметром 7,5 см. После достижения стадии двух листьев, огурцы инокулируют суспензией опор грибка ложной мучнистой росы (Pseudoperonispora enbevsis). Через 7 ч после инокуляции огурцы опрыскивают с помощью распылителя 10 мл раствора каждого из испытуемых соединений, взятых в определенной концентрации. После выдерживания чаш в термостате при 22-24оС в течение 6 дней, исследуют площадь поражения первого листка и в соответствии со стандартами оценки приведенными выше, определяют индекс контроля. Полученные результаты представлены в табл. 5. Испытательный пример 5. Испытание на системную активность против ложной мучнистой росы огурцов. Огурцы (разновидность: Сайо) культивируют в полиэтиленовой чаше диаметром 7,5 см. После достижения огурцами двулистной стадии поверхность почвы с помощью пипетки смачивают 15 мл раствора каждого из испытуемых соединений взятых в определенной концентрации. После выдерживания чаш в термостате при 22-24оС в течение 2 дней, проводят инокуляцию суспензией спор грибка ложной мучнистой росы (Pseudoperonispora enbeusis). Через шесть дней после инокуляции исследуют площадь поражения первого листка, и в соответствии с описанными выше стандартами оценки, определяют индекс контроля. Полученные результаты представлены в табл. 6. Испытательный пример 6. Испытание на превентивный эффект против ранней гнили помидор. Помидоры (разновидность: Подероза) культивируют в полиэтиленовой чаше диаметром 7,5 см. После достижения помидорами стадии четырехлистника их опрыскивают с помощью распылителя 10 мл раствора каждого из испытуемых соединений, взятых в определенной концентрации. После выдерживания чаш в камере с постоянной температурой при 22-24оС в течение одного дня и одной ночи, проводят инокуляцию суспензией зооспорангия грибка ранней гили (Phytophera infestans). Через пять дней после инокуляции исследуют площадь поражения листьев и в соответствии со стандартами оценки приведенным выше, определяют индекс контроля. Полученные результаты представлены в табл. 7. Испытательный пример 7. Испытание на системную активность против ранней гнили помидор. Помидоры (разновидность: Подероза) культивируют в полиэтиленовой чаше диаметром 7,5 см. После достижения помидорами стадии четырехлистника, поверхность почвы с помощью пипетки смачивают 15 мл раствора каждого из испытуемых соединений взятых в определенной концентрации. После выдерживания чаш в камере с постоянной температурой при 22-24оС, в течение 2 дней, проводят инокуляцию суспензией зооспорангия грибка ранней гнили (Phytophtera infestaus). Через пять дней после иокуляции используют площадь поражения листьев и, в соответствии со стандартами оценки приведенным выше, определяют индекс контроля. Полученные результаты представлены в табл. 8. Испытательный пример 8. Испытание на превентивный эффект против пирикуляриоза риса. Рисовые растения (производитель: Чукио Асахи) культивируют в полиэтиленовой чаше диаметром 7,5 см. После достижения рисовыми растениями стадии четырехлистника, их опрыскивают из распылителя 20 мл раствора каждого из испытуемых соединений взятых в определенной концентрации. После выдерживания чаш в камере с постоянной температурой при 22-24оС в течение одного дня и одной ночи, проводят инокуляцию суспензией опор грибка пирикуляриоза (Pyricularia oryzae). Через пять дней после инокуляции исследуют степень поражения и в соответствии со стандартами оценки приведенным выше, определяли индекс контроля. Полученные результаты представлены в табл. 9. Испытательный пример 9. Испытание на превентивный эффект против пирикуляриоза риса. Рисовые растения (производитель: Чукио Асахи) культивируют в полиэтиленовой чаше диаметром 7,5 см. После достижения рисовыми растениями стадии пятилистника, их с помощью распылителя опрыскивают 20 мл раствора каждого из испытуемых соединений, взятых в определенной концентрации. После выдерживания чаш в камере с постоянной температурой при 22-24оС в течение одного дня и одной ночи, между частями листового влагалища с целью инокуляции помещают рисовую солому, в которой предварительно инкубируют грибок гнили оболочки (Rhizoctonia solani). После выдерживания чаш в инокуляционной камере при 28оС и влажности 100% в течение 5 дней, исследуют длину поражения и, в соответствии со стандартами оценки приведенными выше, определяли индекс контроля. Полученные результаты представлены в табл. 10. Испытательный пример 10. Испытание на превентивный эффект против корончатой ржавчины овса. Овес (производитель: Зеншин) культивируют в полиэтиленовой чаше диаметром 7,5 см. После достижения рисовыми растениями стадии двухлистника, их с помощью распрыскивателя опрыскивают 10 мл раствора каждого из испытуемых соединений, взятых в определенной концентрации. После выдерживания чаш в камере с постоянной температурой при 22-24оС в течение одного дня и одной ночи, проводят инокуляцию конидия грибков корончатой ржавчины. Через десять дней после инокуляции исследуют площадь поражения второго листка и в соответствии со стандартами оценки, приведенными выше, определяют индекс контроля. Полученные результаты представлены в табл. 11. Испытательный пример 11. Испытание на превентивный эффект против килы репы. Почву загрязненную грибком килы крестоцветник (Plasmodiaphоra brassical) помещают в чашу площадью 1/14.000 ара (1/140 м2) и поверхность почвы, с помощью пипетки, смачивают 20 мл раствора каждого из испытуемых соединений с концентрацией активного ингредиента 4 кг/10 ар и 1 кг/10 ар. Через день после обработки проводят перемешивание слоев почвы и высевают репу (производительность: Канамаши Кокабу). Репу выращивают в теплице. Через 30 дней после посева исследуют степень поражения килой, и в соответствии со стандартами оценки, приведенными ниже, определяют индекс контроля. Полученные результаты представлены в табл. 12. Испытательный пример 12. Антимикробиальное испытание (фитопатогенный грибок). Мицелиальные диски (проштампованные агаром) предварительно инкубированного Pythium aphanichermatum трансплантируют на картофельно-декстрозную агаровую среду (среда РДА), содержащую 100 ч/млн стрептомицина и 100 ч/млн каждого из испытуемых соединеий. После инкубирования в течение 48 ч при 22оС измеряют диаметр мицелия. Ингибирование гифального роста (%) определяют по следующему уравнению. Полученные результаты представлены в табл. 13. Ингибирование гифального роста (%)= 100 диаметр мицелия в обработанной чаше = ____________________________ х 100 диаметр мицелия в необработанной чаше Ниже приведены рецептурные примеры изобретения, однако соединения, доза в рецептуре, тип рецептур и т.п. изобретения не ограничиваются значениями указанными ниже. Рецептуpный пример 1 (смачиваемый порошок) Соединение N 7-б 20 мас.ч. Каолин 72 мас.ч. Лигнин сульфонат натрия 4 мас.ч. Алкилариловый эфир полиоксиэтилена 4 мас.ч. Указанные компоненты подвергают однородному перемешиванию. Рецептурный пример 2 (смачиваемый порошок) Соединение N 8-б 6 мас.ч. Диатомовая земля 88 мас.ч. Диалкилсульфо- сукцинат 2 мас.ч. Полиоксиэтилен алкиларил сульфат 4 мас.ч. Указанные компоненты подвергали равномерному смешиванию. Рецептурный пример 3 (смачиваемый порошок) Каолин 78 мас.ч. Конденсат бета-нафталин сульфоната натрия и формальдегида 2 мас.ч. Полиоксиэтилен алкиларил сульфат 5 мас.ч. Мелкозернистая смесь кремния 15 мас.ч. 80 мас.ч. указанных компонентов и 206 г соединения 11 перемешивают. Рецептурный пример 4 (смачиваемый порошок) Соединение N 48-б 10 мас.ч. Диатомовая земля 69 мас.ч. Порошок карбоната кальция 15 мас.ч. Диалкилсульфо- сукцинат 1 мас.ч. Полиоксиэтилен алкиларил сульфат 3 мас.ч. Конденсат бета-нафталин сульфоната натрия и формальдегида 2 мас.ч. Указанные компоненты подвергали равномерному перемешиванию. Рецептурный пример 5 (смачиваемый порошок) Соединение N 48-б 10 мас.ч. Диатомовая земля 69 мас.ч. Порошок карбоната кальция 15 мас.ч. Диалкилсульфо- сукцинат 1 мас.ч. Полиоксиэтилен алкиларил сульфат 3 мас.ч. Конденсат бета- нафталин сульфоната натрия и формаль- дегида 2 мас.ч. Указанные компоненты подвергали равномерному перемешиванию. Рецептурный пример 6 (смачиваемый порошок) Соединение N 7-б 20 мас.ч. Каолин 62,4 мас.ч. Мелкозернистая смесь кремния 12,8 мас.ч. Алкиларил сульфонат 1,6 мас.ч. Полиоксиэтилен алкиларил сульфат 2,4 мас.ч. Полиоксиэтилен алкилариловый эфир 0,8 мас.ч. Указанные компоненты подвергали равномерному перемешиванию. Рецептурный пример 7 (эмульгируемый концентрат) Соединение N 14 20 мас.ч. Ксилол 60 мас.ч. Полиоксиэтилен алкилариловый эфир 20 мас.ч. Указанные компоненты подвергали равномерному перемешиванию. Рецептурный пример 8 (эмульгируемый концентрат) Соединение N 98-б 10 мас.ч. Ксилол 70 мас.ч. Полиоксиэтилен алкилариловый эфир 20 мас.ч. Указанные компоненты подвергали равномерному перемешиванию. Рецептурный пример 9 (суспензионный концентрат) Соединение N 39 10 мас. ч. Кукурузное масло 77 мас.ч. Полиоксиэтилен касторовое масло 12 мас.ч. Комплекс бентонита с алкиламином 1 мас.ч. Указанные выше компоненты равномерно смешивают и измельчают в порошок. Рецептурный пример 10 (эмульгируемый концентрат), мас.ч.: Активный ингредиент (соединение 7-б) 5 П-метил-2-пирролидон 5 Ксилол 70 Полиоксиэтилен стирилфениловый эфир 10 Алкиларилсульфонат 10 Рецептурный пример 11 (эмульгируемый концентрат), мас.ч.: Активный ингредиент (соединение 7-б) 10 п-Метил-2-пирролидон 8 Ксилол 62 Полиоксиметилен стирилфениловый эфир 10 Алкиларилсульфонат 10 Рецептурный пример 12 (эмульгируемый концентрат), мас. ч.: Активный ингредиент (соединение 17-б) 20 п-Метил-2-пирролидон 15 Ксилол 45 Полиоксиэтилен стирилфениловый эфир 10 Алкиларилсульфонат 10 Рецептурный пример 13 (суспендируемый концентрат), мас.ч.: Активный ингредиент (соединение 7-б) 5 Оксиэтилированный полиарилфосфат 2 Квантовая смола (биополимер) 0,2 Магнийалюмосиликат 1 Вода 91,8 Рецептурный пример 14 (суспендируемый концентрат), мас.ч.: Активный ингредиент (соединение 7-б) 10 Оксиэтилированный полиарилфосфат 2 Ксантановая смола (биополимер) 0,2 Магнийалюмосиликат 0,5 Вода 87,3 Рецептурный пример 15 (суспендируемый концентрат), мас.ч.: Активный ингредиент (соединение 7-б) 20 Оксиэтилированный полиарилфосфат 2 Ксантановая смола (биополимер) 0,2 Магний алюминийсиликат 0,5 Вода 77,3 Рецептурный пример 16 (смачиваемый порошок), мас.ч.: Активный ингредиент (соединение 7-б) 5 Кизельгур 40 Меловой порошок 49 Диалкилсульфосукцинат 2 Полиоксиэтилен алкиларилсульфонат 4 (1) Дополнительные характеристики соединений: соединение 18 Н-ЯМР (ацетон): 2,87 (С) м.д., 3,27 (С) м.д. 7,4-8,2 (м, 4Н) м.д. Найдено,%: С 36,4; Н 2,8; N 13,9. Вычислено,%: С 37,0; Н 2,6; N 14,4. Соединение 65-б Н-ЯМР (СДС13): 2,0-2,3 (м, 2Н) м.д. 2,7-3,3 (м, 8Н) м.д., 3,5-3,8 (т, 2Н) м.д., 6,97 (С, 1Н) м.д. Ниже описываются примеры испытаний фунгицидных композиций, предназначенных для уничтожения вредных микроорганизмов на сельскохозяйственных и садоводческих площадях в соответствии с изобретением. Стандарты оценки сельскохозяйственных и садоводческих фунгицидов удовлетворяют следующим критериям оценки, если не оговорено особо. Стандарты оценки. Эффект контроля определяют визуальным наблюдением степени заболевания испытуемого растения и выражают в соответствии со следующими 5 группами индексов контроля. (Индекс контроля) (Степень заболевания) 5: Поражение не наблюдается 4: Площадь, число или длительность поражения составляет менее 10% по сравнению с необработанным участком. 3: Площадь, число или длина поражений составляет менее 40% по сравнению с необработанным участком. 2: Площадь, число или длина поражений составляет менее 70% по сравнению с необработанным участком. 1: Площадь, число или длина поражений составляет менее 70% по сравнению с необработанным участком. Испытательный пример 1. Испытание на преветивное действие против настоящей мучнистой росы огурцов. Огурцы (культиватор : Сайс) культивируют в полиэтиленовой чаше диаметром 7,5 см. По достижении огурцами стадии одного листа, огуречные растения опрыскивают с помощью распылителя 10 мл раствора, полученного растворением препаративных форм по примерам 1-6,8,9 каждого из испытуемых соединений до определенной концентрации. После выдерживания чаш в температурной камере при 22-24оС в течение одного дня и одной ночи, проводят инокуляцию конидием грибка настоящей мучнистой росы (Sphacrotheca fuliqinca). Через десять дней после инокуляции используют площадь поражения первого листка и в соответствии со стандартами оценки приведенными выше, определяли индекс контроля. Полученные результаты представлены в табл. 2. Аналогичные результаты получены, когда используют любой из примеров получения форм. Испытательный пример 2. Испытание на превентивный эффект против антракноза огурцов. Огурцы (разновидность: Сайо) культивируют в полиэтиленовой чаше диаметром 7,5 см. После достижения огурцами стадии двух листьев огурцы опрыскивают из распылителя 10 мл раствора каждого из испытуемых соединений, взятых в определенной концентрации, полученного из препаративных форм. После выдерживания чаш в температурной камере при 22-24оС в течение одного дня и одной ночи, проводят инокуляцию суспензий спор грибка антракноза (Colletorechum lagenatium). Через семь дней после инокуляции исследуют площадь поражения первого листка и в соответствии со стандартами оценки, приведенными выше, определяют индекс контроля. Полученные результаты представлены в табл. 3. Испытательный пример 3. Испытание на превентивное действие против ложной мучнистой росы огурцов. Огурцы (разновидность: Сайо) культивируют в полиэтиленовой чаше диаметром 7,5 см. После достижения стадии двух листьев, огурцы опрыскивают 10 мл раствора каждого из испытуемых соединений взятых в определенной концентрации. После выдерживания чаш в термостате при 22-24оС в течение одного дня и одной ночи, проводят инокуляцию суспензией спор грибка ложной мучнистой росы (Pseudoperonospora eubensis). Через шесть дней после инокуляции площадь первого листка и в соответствии со стандартами оценки, приведенными выше, определяют индекс контроля. Полученные результаты представлены в табл. 4. Испытательный пример 4. Испытание на целебный эффект против ложной мучнистой росы огурцов. Огурцы (культиватор: Сайо) культивируют в полиэтиленовой чаше диаметром 7,5 см. После достижения стадии двух листьев, огурцы инокулируют суспензией опор грибка ложной мучнистой росы (Pseudoperonispora enbevsis). Через 7 ч после инокуляции огурцы опрыскивают с помощью распылителя 10 мл раствора каждого из испытуемых соединений, взятых в определенной концентрации. После выдерживания чаш в термостате при 22-24оС в течение 6 дней, исследуют площадь поражения первого листка и в соответствии со стандартами оценки приведенными выше, определяют индекс контроля. Полученные результаты представлены в табл. 5. Испытательный пример 5. Испытание на системную активность против ложной мучнистой росы огурцов. Огурцы (разновидность: Сайо) культивируют в полиэтиленовой чаше диаметром 7,5 см. После достижения огурцами двулистной стадии поверхность почвы с помощью пипетки смачивают 15 мл раствора каждого из испытуемых соединений взятых в определенной концентрации. После выдерживания чаш в термостате при 22-24оС в течение 2 дней, проводят инокуляцию суспензией спор грибка ложной мучнистой росы (Pseudoperonispora enbeusis). Через шесть дней после инокуляции исследуют площадь поражения первого листка, и в соответствии с описанными выше стандартами оценки, определяют индекс контроля. Полученные результаты представлены в табл. 6. Испытательный пример 6. Испытание на превентивный эффект против ранней гнили помидор. Помидоры (разновидность: Подероза) культивируют в полиэтиленовой чаше диаметром 7,5 см. После достижения помидорами стадии четырехлистника их опрыскивают с помощью распылителя 10 мл раствора каждого из испытуемых соединений, взятых в определенной концентрации. После выдерживания чаш в камере с постоянной температурой при 22-24оС в течение одного дня и одной ночи, проводят инокуляцию суспензией зооспорангия грибка ранней гили (Phytophera infestans). Через пять дней после инокуляции исследуют площадь поражения листьев и в соответствии со стандартами оценки приведенным выше, определяют индекс контроля. Полученные результаты представлены в табл. 7. Испытательный пример 7. Испытание на системную активность против ранней гнили помидор. Помидоры (разновидность: Подероза) культивируют в полиэтиленовой чаше диаметром 7,5 см. После достижения помидорами стадии четырехлистника, поверхность почвы с помощью пипетки смачивают 15 мл раствора каждого из испытуемых соединений взятых в определенной концентрации. После выдерживания чаш в камере с постоянной температурой при 22-24оС, в течение 2 дней, проводят инокуляцию суспензией зооспорангия грибка ранней гнили (Phytophtera infestaus). Через пять дней после иокуляции используют площадь поражения листьев и, в соответствии со стандартами оценки приведенным выше, определяют индекс контроля. Полученные результаты представлены в табл. 8. Испытательный пример 8. Испытание на превентивный эффект против пирикуляриоза риса. Рисовые растения (производитель: Чукио Асахи) культивируют в полиэтиленовой чаше диаметром 7,5 см. После достижения рисовыми растениями стадии четырехлистника, их опрыскивают из распылителя 20 мл раствора каждого из испытуемых соединений взятых в определенной концентрации. После выдерживания чаш в камере с постоянной температурой при 22-24оС в течение одного дня и одной ночи, проводят инокуляцию суспензией опор грибка пирикуляриоза (Pyricularia oryzae). Через пять дней после инокуляции исследуют степень поражения и в соответствии со стандартами оценки приведенным выше, определяли индекс контроля. Полученные результаты представлены в табл. 9. Испытательный пример 9. Испытание на превентивный эффект против пирикуляриоза риса. Рисовые растения (производитель: Чукио Асахи) культивируют в полиэтиленовой чаше диаметром 7,5 см. После достижения рисовыми растениями стадии пятилистника, их с помощью распылителя опрыскивают 20 мл раствора каждого из испытуемых соединений, взятых в определенной концентрации. После выдерживания чаш в камере с постоянной температурой при 22-24оС в течение одного дня и одной ночи, между частями листового влагалища с целью инокуляции помещают рисовую солому, в которой предварительно инкубируют грибок гнили оболочки (Rhizoctonia solani). После выдерживания чаш в инокуляционной камере при 28оС и влажности 100% в течение 5 дней, исследуют длину поражения и, в соответствии со стандартами оценки приведенными выше, определяли индекс контроля. Полученные результаты представлены в табл. 10. Испытательный пример 10. Испытание на превентивный эффект против корончатой ржавчины овса. Овес (производитель: Зеншин) культивируют в полиэтиленовой чаше диаметром 7,5 см. После достижения рисовыми растениями стадии двухлистника, их с помощью распрыскивателя опрыскивают 10 мл раствора каждого из испытуемых соединений, взятых в определенной концентрации. После выдерживания чаш в камере с постоянной температурой при 22-24оС в течение одного дня и одной ночи, проводят инокуляцию конидия грибков корончатой ржавчины. Через десять дней после инокуляции исследуют площадь поражения второго листка и в соответствии со стандартами оценки, приведенными выше, определяют индекс контроля. Полученные результаты представлены в табл. 11. Испытательный пример 11. Испытание на превентивный эффект против килы репы. Почву загрязненную грибком килы крестоцветник (Plasmodiaphоra brassical) помещают в чашу площадью 1/14.000 ара (1/140 м2) и поверхность почвы, с помощью пипетки, смачивают 20 мл раствора каждого из испытуемых соединений с концентрацией активного ингредиента 4 кг/10 ар и 1 кг/10 ар. Через день после обработки проводят перемешивание слоев почвы и высевают репу (производительность: Канамаши Кокабу). Репу выращивают в теплице. Через 30 дней после посева исследуют степень поражения килой, и в соответствии со стандартами оценки, приведенными ниже, определяют индекс контроля. Полученные результаты представлены в табл. 12. Испытательный пример 12. Антимикробиальное испытание (фитопатогенный грибок). Мицелиальные диски (проштампованные агаром) предварительно инкубированного Pythium aphanichermatum трансплантируют на картофельно-декстрозную агаровую среду (среда РДА), содержащую 100 ч/млн стрептомицина и 100 ч/млн каждого из испытуемых соединеий. После инкубирования в течение 48 ч при 22оС измеряют диаметр мицелия. Ингибирование гифального роста (%) определяют по следующему уравнению. Полученные результаты представлены в табл. 13. Ингибирование гифального роста (%)= 100 диаметр мицелия в обработанной чаше = ____________________________ х 100 диаметр мицелия в необработанной чаше Ниже приведены рецептурные примеры изобретения, однако соединения, доза в рецептуре, тип рецептур и т.п. изобретения не ограничиваются значениями указанными ниже. Рецептуpный пример 1 (смачиваемый порошок) Соединение N 7-б 20 мас.ч. Каолин 72 мас.ч. Лигнин сульфонат натрия 4 мас.ч. Алкилариловый эфир полиоксиэтилена 4 мас.ч. Указанные компоненты подвергают однородному перемешиванию. Рецептурный пример 2 (смачиваемый порошок) Соединение N 8-б 6 мас.ч. Диатомовая земля 88 мас.ч. Диалкилсульфо- сукцинат 2 мас.ч. Полиоксиэтилен алкиларил сульфат 4 мас.ч. Указанные компоненты подвергали равномерному смешиванию. Рецептурный пример 3 (смачиваемый порошок) Каолин 78 мас.ч. Конденсат бета-нафталин сульфоната натрия и формальдегида 2 мас.ч. Полиоксиэтилен алкиларил сульфат 5 мас.ч. Мелкозернистая смесь кремния 15 мас.ч. 80 мас.ч. указанных компонентов и 206 г соединения 11 перемешивают. Рецептурный пример 4 (смачиваемый порошок) Соединение N 48-б 10 мас.ч. Диатомовая земля 69 мас.ч. Порошок карбоната кальция 15 мас.ч. Диалкилсульфо- сукцинат 1 мас.ч. Полиоксиэтилен алкиларил сульфат 3 мас.ч. Конденсат бета-нафталин сульфоната натрия и формальдегида 2 мас.ч. Указанные компоненты подвергали равномерному перемешиванию. Рецептурный пример 5 (смачиваемый порошок) Соединение N 48-б 10 мас.ч. Диатомовая земля 69 мас.ч. Порошок карбоната кальция 15 мас.ч. Диалкилсульфо- сукцинат 1 мас.ч. Полиоксиэтилен алкиларил сульфат 3 мас.ч. Конденсат бета- нафталин сульфоната натрия и формаль- дегида 2 мас.ч. Указанные компоненты подвергали равномерному перемешиванию. Рецептурный пример 6 (смачиваемый порошок) Соединение N 7-б 20 мас.ч. Каолин 62,4 мас.ч. Мелкозернистая смесь кремния 12,8 мас.ч. Алкиларил сульфонат 1,6 мас.ч. Полиоксиэтилен алкиларил сульфат 2,4 мас.ч. Полиоксиэтилен алкилариловый эфир 0,8 мас.ч. Указанные компоненты подвергали равномерному перемешиванию. Рецептурный пример 7 (эмульгируемый концентрат) Соединение N 14 20 мас.ч. Ксилол 60 мас.ч. Полиоксиэтилен алкилариловый эфир 20 мас.ч. Указанные компоненты подвергали равномерному перемешиванию. Рецептурный пример 8 (эмульгируемый концентрат) Соединение N 98-б 10 мас.ч. Ксилол 70 мас.ч. Полиоксиэтилен алкилариловый эфир 20 мас.ч. Указанные компоненты подвергали равномерному перемешиванию. Рецептурный пример 9 (суспензионный концентрат) Соединение N 39 10 мас. ч. Кукурузное масло 77 мас.ч. Полиоксиэтилен касторовое масло 12 мас.ч. Комплекс бентонита с алкиламином 1 мас.ч. Указанные выше компоненты равномерно смешивают и измельчают в порошок. Рецептурный пример 10 (эмульгируемый концентрат), мас.ч.: Активный ингредиент (соединение 7-б) 5 П-метил-2-пирролидон 5 Ксилол 70 Полиоксиэтилен стирилфениловый эфир 10 Алкиларилсульфонат 10 Рецептурный пример 11 (эмульгируемый концентрат), мас.ч.: Активный ингредиент (соединение 7-б) 10 п-Метил-2-пирролидон 8 Ксилол 62 Полиоксиметилен стирилфениловый эфир 10 Алкиларилсульфонат 10 Рецептурный пример 12 (эмульгируемый концентрат), мас. ч.: Активный ингредиент (соединение 17-б) 20 п-Метил-2-пирролидон 15 Ксилол 45 Полиоксиэтилен стирилфениловый эфир 10 Алкиларилсульфонат 10 Рецептурный пример 13 (суспендируемый концентрат), мас.ч.: Активный ингредиент (соединение 7-б) 5 Оксиэтилированный полиарилфосфат 2 Квантовая смола (биополимер) 0,2 Магнийалюмосиликат 1 Вода 91,8 Рецептурный пример 14 (суспендируемый концентрат), мас.ч.: Активный ингредиент (соединение 7-б) 10 Оксиэтилированный полиарилфосфат 2 Ксантановая смола (биополимер) 0,2 Магнийалюмосиликат 0,5 Вода 87,3 Рецептурный пример 15 (суспендируемый концентрат), мас.ч.: Активный ингредиент (соединение 7-б) 20 Оксиэтилированный полиарилфосфат 2 Ксантановая смола (биополимер) 0,2 Магний алюминийсиликат 0,5 Вода 77,3 Рецептурный пример 16 (смачиваемый порошок), мас.ч.: Активный ингредиент (соединение 7-б) 5 Кизельгур 40 Меловой порошок 49 Диалкилсульфосукцинат 2 Полиоксиэтилен алкиларилсульфонат 4
ФОРМУЛА ИЗОБРЕТЕНИЯПРОИЗВОДНЫЕ ИМИДАЗОЛА общей формулы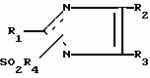 где R1 - CN или CSNHR5, R5 - водород, ацетил или пропионил; R2 - водород, циклопропил, циклогексил, 2-нафтил, алкил С1 - С8, С12, 3-фторпропил, 3-хлорпропил, 4-хлорбутил, 5-хлорпентил, гидроксипропил, гидроксибутил, метоксиметил, этоксиметил, фенетил, 1,2-дифенилэтил, 2,2,2-трифторэтокси, бензил, L-гидроксибензил, метилбензил, 2-фторбензил, аллил, 2-бутенил, фенил, хлорфенил, фторфенил, 4-бромфенил, 2,3-дихлорфенил, 3,4-дихлорфенил, 4-метилфенил, 3-метилфенил, 2-метилфенил, 4-этилфенил, 4-изопропилфенил, 4-трет-бутилфенил, 3,4-диметилфенил, 4-метоксифенил, 4-этоксифенил, 4-метил-3-хлорфенил, 4-метокси-3-хлорфенил, 3-метил-4-метоксифенил, 3,4-метилендиоксифенил, 4-(2", 2", 2"-трифторэтокси)фенил, 4-циано-фенил, 4-нитрофенил, 2-фурил, 5-метил-2-фурил, 2-тиенил, 5-хлор-2-тиенил, 5-бромо-2-тиенил, SOnR6; где R6 - алкил С1 - С4, аллил, фенил, бензил, 3-трифторметил-2-пиридил, 4-хлорфенил при n = 0, R6 - диметиламино, этил при n = 2, CONHR7, где R7 -фенил, 4-хлорфенил, R3 - водород, хлор, бром, йод, циано, нитро, метил, этил, метилтио, фенилтио, 2-фурил, трифторацетил, R4 - изопропил, диметиламино, диэтиламино, морфолино. где R1 - CN или CSNHR5, R5 - водород, ацетил или пропионил; R2 - водород, циклопропил, циклогексил, 2-нафтил, алкил С1 - С8, С12, 3-фторпропил, 3-хлорпропил, 4-хлорбутил, 5-хлорпентил, гидроксипропил, гидроксибутил, метоксиметил, этоксиметил, фенетил, 1,2-дифенилэтил, 2,2,2-трифторэтокси, бензил, L-гидроксибензил, метилбензил, 2-фторбензил, аллил, 2-бутенил, фенил, хлорфенил, фторфенил, 4-бромфенил, 2,3-дихлорфенил, 3,4-дихлорфенил, 4-метилфенил, 3-метилфенил, 2-метилфенил, 4-этилфенил, 4-изопропилфенил, 4-трет-бутилфенил, 3,4-диметилфенил, 4-метоксифенил, 4-этоксифенил, 4-метил-3-хлорфенил, 4-метокси-3-хлорфенил, 3-метил-4-метоксифенил, 3,4-метилендиоксифенил, 4-(2", 2", 2"-трифторэтокси)фенил, 4-циано-фенил, 4-нитрофенил, 2-фурил, 5-метил-2-фурил, 2-тиенил, 5-хлор-2-тиенил, 5-бромо-2-тиенил, SOnR6; где R6 - алкил С1 - С4, аллил, фенил, бензил, 3-трифторметил-2-пиридил, 4-хлорфенил при n = 0, R6 - диметиламино, этил при n = 2, CONHR7, где R7 -фенил, 4-хлорфенил, R3 - водород, хлор, бром, йод, циано, нитро, метил, этил, метилтио, фенилтио, 2-фурил, трифторацетил, R4 - изопропил, диметиламино, диэтиламино, морфолино.Популярные патенты: 2415542 Пневматический высевающий аппарат ... с соответствующими входами блока контроля, содержащего последовательно соединенные первый элемент И, счетчик импульсов, вычислитель и индикатор. При этом первый вход первого элемента И соединен с первым выходом первого триггера, первый и второй входы которого являются соответственно первым и вторым входами блока контроля. Второй выход первого триггера соединен через элемент задержки с входом установки нуля счетчика импульсов. При этом выход генератора импульсов соединен с вторым входом первого элемента И и через делитель и первый вход второго элемента И - с входом сдвига «вправо» сдвигового регистра. Второй вход второго элемента И соединен с выходом второго триггера, вход ... 2120752 Способ консервирования ксеногенных клеток печени ... для второй. Осадок промывают раствором Хенкса и центрифугируют, затем к осадку добавляют питательную среду 199 на растворе Хенкса в соотношении 10:1, разливают на поддон толщиной 50 мм и замораживают при температуре минус 35oС в течение 3 ч с последующей сублимационной сушкой при температуре минус 30oС в течение 36 ч с температурой досушивания 20oС. Функциональная активность высушенных клеток составляет 420%. Пример 2. Отбирают печень от клинически здорового животного четырехмесячного возраста массой 1100 г. Отделяют желчный пузырь и разделяют печень на доли. Затем через систему кровеносных сосудов проводят перфузию раствором Хенкса до соломенножелтого цвета печени. Для уменьшения ... 2005344 Способ облучения живых организмов или растений ... параметров режима облучения определяют площадь освещаемой поверхности объекта в зависимости от его геометрических параметров и угол рассеивания сформированного потока излучения гелий-неонового лазера, а для обеспечения получения объектом выбранной дозы энергии I определяют расстояние Н от центра рассеивания до облучаемого живого организма или растения по следующей зависимости: H ; Патентные исследования показали, что предлагаемое изобретение не известно из общедоступных источников информации, следовательно оно является новым. Предлагаемое изобретение имеет изобретательский уровень, так как оно явным образом не следует из уровня техники, известным по сведениям, общедоступным в ... 2129787 Инсектицидная композиция ... длительного периода времени из-за того, что скорость испарения бенфлутрина снижается, как показано в таблице 1. С другой стороны, сравнительные композиции (1), (2) и (3), которые содержат бис (2,3,3,3-тетрахлорпропил)эфир [S-421] и пиперонилбутилат [PBO] соответственно, где [S-421] и [PBO] являются известными синергистами, являются едва ли способными поддержать постоянный инсектицидный эффект в течение длительного периода времени, потому что большая часть бенфлутрина в качестве активного ингредиента испаряется на ранних стадиях. Примеры приготовления 3 и 4. Пример приготовления 3. С 10 мг бенфлутрина смешивают 60 мг МGК 264 и к полученной смеси добавляют 130 мг IP ... 2054862 Гидравлический режущий аппарат ... При этом значительно снижается КПД аппарата из-за увеличения расхода энергии на сжатие до рабочего давления значительного "вредного" объема дополнительного ресивера, не участвующего непосредственно в процессе резки растений струей жидкости. Кроме того, ужесточаются условия работы гидравлического аппарата с точки зрения техники безопасности. Таким образом, применение подобного устройства не обеспечило требуемой эффективности процесса резки сельскохозяйственных растений и других материалов, особенно в условиях автономного использования установки. Известен также гидравлический режущий аппарат [2] выбранный за прототип, содержащий гидроцилиндр с основной камерой низкого давления, ... |
Еще из этого раздела: 2272399 Зерноуборочный комбайн 2154931 Корнеуборочная машина 2238970 Штамм mycelia sterilia лх-1-продуцент комплекса биологически активных веществ, обладающих рострегуляторными свойствами 2285375 Способ обработки почвы и устройство для его осуществления 2040152 Способ выращивания корнеплодных культур в контролируемых условиях и установка для его осуществления 2157612 Способ уборки корней растений, преимущественно лакрицы, и устройство для его осуществления 2054872 Гербицидная композиция и способ борьбы с сорняками 2241322 Навесное устройство трактора 2182765 Имитатор звуков рыб 2496309 Зубчатое устройство для вычесывания домашних животных с механизмом выброса шерсти |
Изобретения в сельском хозяйстве
Обработка почвы в сельском и лесном хозяйствах
Посадка, посев, удобрение
Уборка урожая, жатва
Обработка и хранение продуктов полеводства и садоводства
Садоводство, разведение овощей, цветов, риса, фруктов, винограда, лесное хозяйство
Новые виды растений или способы их выращивания
Производство молочных продуктов
Животноводство, разведение и содержание птицы, рыбы, насекомых, рыбоводство, рыболовство
Поимка, отлов или отпугивание животных
Консервирование туш животных, или растений или их частей
Биоцидная, репеллентная, аттрактантная или регулирующая рост растений активность химических соединений или препаратов
Хлебопекарные печи, машины и прочее оборудование для хлебопечения
Машины или оборудование для приготовления или обработки теста
Обработка муки или теста для выпечки, способы выпечки, мучные изделия
|
|
||