Способ получения клонированной коровыПатент на изобретение №: 2205536 Автор: ЛИ Биеонг-Чун (KR), ШИН Тае-Янг (KR), РОХ Санг-Хо (KR), ЛИМ Дзеонг-Мук (KR), ПАРК Дзонг-Им (KR), ЧО Дзонг-Ки (KR), КИМ Ки-Ен (KR), ЛИ Еун-Сонг (KR), ШИН Соо-Дзунг (KR), КИМ Сунг-Ки (KR), СОНГ Кил-Янг (KR), ХВАНГ Воо-Сук (KR) Патентообладатель: ХВАНГ Воо-Сук (KR) Дата публикации: 10 Июня, 2003 Начало действия патента: 30 Июня, 2000 Адрес для переписки: 129010, Москва, ул. Б. Спасская, 25, стр.3, ООО "Юридическая фирма Городисский и Партнеры", Н.Г.Лебедевой, рег.№ 0112 Изображения   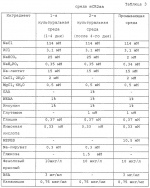 Изобретение относится к генетической инженерии, а в частности к методам клонирования животных. Способ получения клонированной коровы предусматривает получение линий донорских соматических клеток от коровы, выделение ооцитов из яичника коровы и их созревание in vitro. Далее удаляют клетки кулумуса, окружающие ооциты и получают энуклеированные реципиентные ооциты. Затем осуществляют перенос ядра донорных клеток в реципиентный ооцит с последующим электрослиянием и активацией электрослитых клеток, что приводит к получению эмбриона. Далее полученные эмбрионы постактивируют и культивируют in vitro. Подрощенные эмбрионы переносят в "суррогатных матерей" с последующим получением клонированного теленка. Данное изобретение применяется для производства фармацевтических препаратов или органов из клонированных коров, а также для проведения научно-исследовательских работ. 10 з.п.ф-лы, 12 табл., 4 ил. , , , , , , , , , , , ОПИСАНИЕ ИЗОБРЕТЕНИЯ К ПАТЕНТУИзобретение относится к способу получения клонированных коров - точнее, к способу получения клонированных коров, производных соматических клеток, включающему в себя созревание и последующую энуклеацию ооцитов in vitro, перенос ядер, слияние методом электротока и активацию эмбрионов, постактивацию и выращивание эмбрионов in vitro и перенос эмбрионов коровам-реципиентам. Изобретение также относится к эмбрионам и клонированным коровам, полученным с помощью вышеописанного способа. Длительное время рассматривается вопрос о том, что животных следует производить с помощью оплодотворения, вовлекающего мужские и женские половые клетки. Огромные усилия направлены на производство клонированных животных с идентичным внешним видом и генетическими характеристиками. Известно, что в течение 30 лет было возможным клонирование только земноводных, пока не был достигнут успех в получении клонированного потомства с помощью замещения пронуклеуса одноклеточной зиготы у мышей (см. McGrath and Solter, Science, 220:1300-1302, 1983). Несмотря на этот первый успех в клонировании животных, о подобном достижении в отношении промышленных животных (Wakayama et al., Nature, 394:369-374, 1998) стало известно значительно позднее, так как при получении клонированных мышей с использованием зрелых ооцитов и зиготных бластомеров после 2-клеточной стадии возникали некоторые проблемы, такие как снижение в перепрограммировании. Что касается получения клонированных промышленных животных с помощью ядерного переноса, сначала стало известно о получении потомства у овцы посредством применения бластомеров 8-16-клеточной зиготы в качестве донорских клеток (см. Wiladsen, Nature, 320, 63-65, 1986). С этого времени считают, что в результате ядерного переноса клонируются только бластомеры зиготы с тотипотентностью, благодаря которой клетка может дифференцироваться в любую клетку. Однако благодаря постоянным усилиям исследователей первая клонированная овца была получена в результате введения ядер из соматических клеток (см. Wilmut et al., Nature, 385, 810-813, 1997), что, таким образом, внесло поправку в предшествующую эволюционную теорию и предоставило возможность сообщить о многих удачных примерах в получении клонированных коров (см. Wells et al., Reprod. Fertil. and Develop., 10, 369-378, 1998) и свиней. Однако доказано, что способы предыдущего уровня техники мало соответствуют требованиям в том смысле, что количество эмбрионов, полученных посредством переноса ядер, оказалось относительно низким, что приводило к низкому уровню производства клонированных животных. При таких обстоятельствах имеются серьезные причины для исследования и разработки улучшенного способа для производства эмбрионов, происходящих из соматических клеток, с точки зрения количественного выхода эмбрионов, полученных посредством переноса ядра. Согласно данному изобретению обнаружено следующее: количественный выход эмбрионов, полученных в результате переноса ядер, можно резко увеличить посредством уменьшения времени манипуляции с ооцитами и улучшения ядерного переноса и степени активации, когда донорские клетки перемещаются в энуклеированные ооциты, в результате чего могут быть эффективным способом получены клонированные коровы, производные соматических клеток. Поэтому главным аспектом данного изобретения является обеспечение способом получения клонированных коров с помощью переноса ядер соматических клеток. Другой аспект изобретения заключается в обеспечении клонированными коровьими эмбрионами с помощью вышеупомянутого способа. Еще один аспект заключается в обеспечении клонированными коровами, производными соматических клеток, с помощью вышеупомянутого способа. Вышеупомянутые и другие аспекты и особенности данного изобретения станут очевидными из следующего описания, представленного вместе с сопровождающими чертежами. Фигура 1 является фотографией донорских соматических клеток. Фигура 2 является фотографией, демонстрирующей процесс разрезания блестящей оболочки реципиентного ооцита с помощью удерживающей пипетки и разрезающей пипетки. На фигуре 3 представлена фотография, демонстрирующая процесс энуклеации посредством удаления первичного полярного тельца и ядра из реципиентного ооцита. Фигура 4 является фотографией, демонстрирующей процесс переноса соматической клетки в энуклеированный ооцит с помощью удерживающей пипетки и инъецирующей пипетки. Способ данного изобретения для получения клонированных коров включает в себя следующие стадии: приготовление линий донорских соматических клеток, полученных от коров; созревание ооцитов, полученных из яичника in vitro; удаление клеток, скапливающихся (скопление клеток) в окружении ооцитов; разрезание части блестящей оболочки зрелых ооцитов и выжимание порции цитоплазмы, включающей в себя первичное полярное тельце, чтобы получить энуклеированные реципиентные ооциты; перенос ядра в реципиентный ооцит посредством инъекции донорских клеток в энуклеированные ооциты с последующим электрослиянием и активацией клеток, слитых методом электрошока для получения эмбрионов; постактивацию и выращивание эмбрионов in vitro; и перенос выращенных эмбрионов коровам-реципиентам для производства клонированных телят. Способ изобретения для получения клонированных коров в дальнейшем иллюстрируется следующим образом. Стадия 1: Приготовление донорских клеток Линии соматических клеток, извлеченных из коров, получали в качестве донорских клеток: хотя виды коров не являются ограничивающим фактором для донорских клеток, для последних предпочтительны корейские коровы (Bostaurus coreanae) и Гольстейн (Holstein; Bos taurus). Полученные от коров клеточные линии включают в себя клетки, извлеченные из жидкости, промывающей матку, эндометрия, маточной трубы, уха или мышцы, скоплений клеток и эмбриональных фибробластов, которые приготавливались с помощью общепринятого известного способа (см. Mather & Barnes, Methods in Cell Biology, Vol. 57, Animal Cell Culture Methods, Academic Press, 1998) с некоторыми модификациями. Например, клетки получали добавлением PBS (забуференного фосфатом физиологического раствора), содержащего 1% пенициллина-стрептомицина (Gibco; 10000 Ед/мл пенициллина, 10 мг/мл стрептомицина), в промывающую матку жидкость и последующего центрифугирования. Клетки, собранные из промывающей матку жидкости, выращивали в DMEM (модифицированная Дульбекко среда Игла), дополненной заменимыми аминокислотами, 10% FBS (фетальная бычья сыворотка) и 1% пенициллином-стрептомицином в условиях 39oС, 5% СО2. Эпителиальные клетки матки, полученные из эндометрия или маточной трубы, промывались упомянутым PBS, трипсинизировались и культивировались в тех же условиях, которые описаны выше. Что касается скопления клеток, то для отделения скопления клеток, окружающих ооцит, комплексы скопление-ооцит обрабатывались раствором гиалуронидазы. Скопление клеток трипсинизировали в течение 30-60 мин в среде 5% СО2 при 39oС до выращивания их таким же способом, как описанный выше. Что касается фибробластов уха и фетальных фибробластов, то их получали с внутренней стороны кожи, граничащей с хрящевой тканью, и из ткани, извлеченной из туловища и конечностей плода, соответственно, посредством асептического промывания и измельчения ткани с последующей обработкой трипсином и коллагеназой II типа в среде 5% СО2 при 39oС. Эти клетки выращивались аналогично тому, как описано выше для линий соматических донорских клеток. Линии соматических клеток поддерживались субкультивированием, культивированием в минимальной сывороточной среде или замораживанием. Субкультивирование донорских клеточных линий осуществлялось заменой старой среды на новую после трипсинизации с определенными интервалами. Выращивание в минимальной сывороточной среде проводилось с использованием DMEM, дополненной 0,5% FBS и способа Wilmut et al. (см. Wilmut et al., Nature, 385: 810-813, 1997). Поддерживаемые таким образом клеточные линии использовались на более поздней стадии в качестве донорских клеток. Стадия 2: Приготовление реципиентных ооцитов Незрелые ооциты, извлеченные из яичника, подвергались созреванию in vitro: незрелые ооциты отбирались из яичника в промывную среду ТСМ199, содержащую 10 мМ HEPES(N-[гидроксиэтил]пиперазин-N"-[2-этансульфоновая кислота] ), и созревали посредством выращивания клеток в культуральной среде ТСМ199 (содержащей Na-пируват, пенициллин-стрептомицин), дополненной эстрадиолом, FSH (фолликуло-стимулирующий гормон) и FBS в течение 16-22 ч в среде 5% СО2 при 39oС. Стадия 3: Энуклеация реципиентных ооцитов После удаления скоплений клеток, окружающих зрелые реципиентные ооциты, и разрезания части блестящей оболочки ооцитов, из ооцитов удалялась порция цитоплазмы, содержащая первичное полярное тельце, для получения энуклеированных ооцитов: сначала скопления клеток, окружающие зрелые ооциты, перемещались физическим способом отбирающей пипеткой в промывающую среду ТСМ199, содержащую гиалуронидазу. Затем обнаженные ооциты промывались промывающей средой ТСМ199 и переносились в раствор цитохалазина В. Для энуклеации обнаженных ооцитов разрезающей пипеткой проникали через участок блестящей оболочки обнаженных ооцитов, чтобы сделать разрез, через который из ооцитов может быть выдавлено от 10 до 15% цитоплазмы, содержащей первичное полярное тельце. Энуклеированные ооциты промывались и инкубировались в культуральной среде ТСМ199. Вышеупомянутый раствор цитохалазина В готовился разведением цитохалазина В, растворенного в DMSO (диметилсульфоксид), культуральной средой ТСМ199. Стадия 4: Слияние донорских клеток с реципиентными ооцитами методом электрошока и активация клеток, слитых методом электрошока Донорские клетки переносились в реципиентные ооциты с последующим электрослиянием и активацией клеток, слитых методом электрошока: перед введением донорских клеток в реципиентные ооциты энуклеированные ооциты промывались культуральной средой ТСМ199 и переносились в раствор РНА-Р (фитогемагглютинина). Затем донорские клетки переносились в энуклеированные ооциты введением донорских клеток в разрез, сделанный в блестящей оболочке ооцитов в растворе РНА-Р. Электрослияние осуществлялось с помощью электроклеточного манипулятора (ВТХ ЕСМ2001). Реконструированные эмбрионы в растворе маннита, дополненного промывающим раствором ТСМ199, помещались в камеру с двумя электродами, по одному на каждой стороне. Перед размещением эмбрионов с их донорскими клетками в камере со стороны катода камера заполнялась раствором маннита. После того как эмбрионы подверглись электрослиянию посредством нанесения импульса DC (плотность тока) от 0,75 до 2,00 кВ/см дважды в течение 15 мкс каждый раз с односекундным интервалом эмбрионы, слитые методом электрошока, промывались раствором маннита и промывающей средой ТСМ199, инкубировались в растворе цитохалазина В и активировались. Электрослияние и активация происходят одновременно при условии, что электрослияние осуществлялось в среде маннита, содержащей Са2+. Иначе активация проводилась после электрослияния. Если электрослияние выполнялось в маннитной среде в отсутствие Ca2+, стадия активации осуществлялась посредством инкубации эмбрионов в растворе иономицина в темноте. Затем иономицин удалялся из эмбрионов промыванием их промывающей средой ТСМ199, содержащей FBS или BSA. Упомянутый раствор иономицина готовился разбавлением иономицина, растворенного в DMSO, промывающей средой ТСМ199, содержащей BSA. Стадия 5: Постактивация и выращивание эмбрионов in vitro Эмбрионы подвергались постактивации и культивировались in vitro: активированные эмбрионы, инкубированные в промывающей среде ТСМ199, содержащей FBS или BSA, подвергались постактивации посредством инкубации в растворе циклогексимида или в растворе DAMP (4-диметиламинопурина) и выращивались in vitro в среде 5% СО2 или смеси 5% СО2, 7% СО2 и 88% N2. Вышеупомянутый раствор циклогексимида или раствор DAMP готовился добавлением циклогексимида, растворенного в этаноле, или DAMP к среде для культивирования in vitro, соответственно. Среда для культивирования in vitro включает в себя среду mTALP (см. Таблицу 1), среду mSOF (см. Таблицу 2) и среду mCR2aa (см. Таблицу 3), каждая из которых содержит NaСl, KCl, NаНСО3, NaH2PO4, CaCl2, Na-лактат, глюкозу, феноловый красный, BSA, канамицин, незаменимые аминокислоты, заменимые аминокислоты и L-глутамин. Возможно, что выращенные in vitro эмбрионы сохранялись в замороженном состоянии для последующего использования и оттаивались, когда оказывалось необходимым их применение. Для замораживания эмбрионов они промывались PBS, содержащим FBS, переносились в среду замораживания, содержащую пенициллин-стрептомицин, CaCl2, глюкозу, MgCl2, Na-пируват и PBS. Затем в среде для замораживания эмбрионы медленно замораживались с последующим быстрым замораживанием в жидком N2. Когда замороженные эмбрионы вынимали из жидкого Ns и оттаивали, они содержались на воздухе в течение приблизительно 5 с, а затем оттаивались в теплой воде. Для удаления среды замораживания из оттаянных эмбрионов эмбрионы последовательно помещались в среды, содержащие глицерин от высокой до низкой концентрации. Стадия 6: Получение клонированных коров Выращенные in vitro эмбрионы переносились в коровы-реципиенты: эмбрионы в PBS имплантировались в матку коров-реципиентов. Основываясь на вышеописанном способе, в настоящем изобретении получены эмбрионы: эмбрионы Bos taurus coreanae/TcEar и SNU2 (Бычий эмбрион NT), при использовании клеток уха корейской коровы и (Bos taurus coreanae) и Гольстейн (Holstein) в качестве доноров ядер, соответственно. Эти два вида эмбрионов переданы на депонирование в Корейскую коллекцию видов культур, КСТС (Korean Collection for Type Cultures; KRIBB 52, Oundong, Yusongku, Taejon, 305-333, Republic of Korea) 31 декабря 1999 и 10 марта 2000, под регистрационными номерами КСТС 0719ВР и КСТС 0753ВР, соответственно. В результате переноса этих эмбрионов коровам-реципиентам получено нормальное клонированное потомство. В дальнейшем данное изобретение иллюстрируется следующими примерами, которые не предназначены для ограничения изобретения. Пример 1: Приготовление донорских клеток и реципиентных ооцитов Для приготовления донорских клеток ткань, расположенную с внутренней стороны кожи уха, получали у корейских коров (Bos taurus coreanae), промывали PBS (забуференный фосфатом физиологический раствор, Gibco BRL, Life Technologies, USA) и измельчали до размера 100 меш. Затем ткань инкубировали в PBS, содержащем 0,25% трипсина, 1 мМ ЭДТА и 1 мг/мл коллагеназы II типа, в течение 1 ч в среде 5% СО2 при 39oС. После переваривания ткани ферментами ткань центрифугировали при 1500 оборотов в минуту в течение 2 мин и суспендировали в DMEM (модифицированная Дульбекко среда Игла, Gibco BRL, Life Technologies, USA), дополненной 10% FBS, 1% NEAA (заменимые аминокислоты) и 1% пенициллина-стрептомицина. Для получения линии соматических клеток суспензию переносили в чашки для клеточной культуры и инкубировали в условиях 39oС, 5% СО2. Вслед за этим клетки трипсинизировали в растворе, содержащем 0,25% трипсина и 1 мМ ЭДТА, количество клеток устанавливали так, чтобы аликвоты клеток в эппендорфных пробирках содержали 2 104 клеток/мл. Фигура 1 изображает соматические клетки, выделенные в качестве однотипных клеток для ядерного донора. С другой стороны, что касается реципиентных ооцитов, то фолликулы, размер которых составлял приблизительно 2-6 мм в диаметре, отсасывали из яичников корейских коров шприцем 10 мл с иглой 18G. Затем фолликулярную жидкость переносили в чашки, 100 мм, с сеткой (длина между линиями составляла 1 см), начерченной на дне чашки, и отбирали ооциты с однородной цитоплазмой и достаточным количеством слоев скоплений клеток вокруг них. Отобранные ооциты промывали три раза 2 мл промывающей среды ТСМ199 (см. Таблицу 4) в 35 мм чашках и впоследствии один раз культуральной средой ТСМ199 (см. Таблицу 5). Наконец, для получения реципиентных ооцитов ооциты выращивали в культуральной среде ТСМ199, содержащей 0,1% раствора эстрадиола (см. Таблицу 6), 2,5% раствор фолликуло-стимулирующего гормона (см. Таблицу 7) и 10% FBS. Пример 2: Перенос ядер соматических клеток Приготовленные в Примере 1 реципиентные ооциты промывали один раз промывающей средой ТСМ199 и переносили в 0,1% раствор гиалуронидазы (Sigma Chemical Co., USA), полученный смешиванием 1 мл промывающей среды ТСМ199 с 111 мкл исходного раствора гиалуронидазы (10 мг/мл промывающей среды ТСМ199). После того как скопления клеток были отделены от ооцитов в присутствии 0,1% гиалуронидазы, обнаженные ооциты промывали три раза и инкубировали в промывающей среде ТСМ199. Затем ооциты переносили в раствор цитохалазина В (Sigma Chemical Co. , USA), приготовленный смешиванием 1 мл промывающей среды ТСМ199, содержащей 10% FBS, с 1 мкл исходного раствора цитохалазина (7,5 мг/мл DMSO), и, используя микроманипулятор, разрезали блестящую оболочку каждого ооцита, чтобы сделать разрез, через который можно выдавить от 10 до 15% цитоплазмы ооцита для создания энуклеированного ооцита. Стадия энуклеации точнее поясняется следующим образом: рабочую чашку помещали на стол микроманипулятора, а микроманипулятор оснащали удерживающей пипеткой на его левой ручке и разрезающей пипеткой на его правой ручке. Затем устанавливали положение удерживающей пипетки и разрезающей пипетки в направлении 9 часов и 3 часов, соответственно, и настраивали для свободного движения во всех направлениях посредством размещения пипетки-контролера в середине. В дальнейшем эти две пипетки настраивали так, чтобы не допустить их соприкосновения с рабочей чашкой и, посредством движения пипеток вверх и вниз над микрокапелькой, устанавливали их кончики в середине микрокапельки. Затем ооциты переносили из промывающей среды ТСМ199 в раствор цитохалазина В, используя промывающие ротовые пипетки (>200 мкм внутренний диаметр). Микроманипулятор сначала фокусировали на ооците, используя его ручку грубой настройки и ручку тонкой настройки, и далее фокус регулировали движением двух пипеток вверх и вниз. Ооцит размещали, ориентируя его первичное полярное тельце в направлении 12 часов, а удерживающую пипетку размещали близко к ооциту в направлении 9 часов от ооцита, чтобы фиксировать ооцит посредством применения гидравлического давления. На фигуре 2 представлен процесс разрезания блестящей оболочки ооцита удерживающей и разрезающей пипетками. Как показано на фигуре 2, разрезающая пипетка 2 пронизывает ооцит в направлении от 1 часа к 11 часам с особой осторожностью, чтобы не повредить цитоплазму ооцита. После этого, чтобы отделить ооцит 3, к удерживающей пипетке 1 применяли гидравлическое давление, и эту пипетку приводили в контакт с разрезающей пипеткой, пронизывающей блестящую оболочку, окаймляющую верхнюю часть первичного полярного тельца, чтобы трением двух пипеток разрезать часть блестящей оболочки. Сделанный выше разрез на ооците использовали как для энуклеации, так и для введения донорских клеток. На фигуре 3 изображен процесс энуклеации, в результате которого из ооцита удаляется первичное полярное тельце и ядро. Как показано на фигуре 3, ооцит 3 размещали, ориентируя его разрез вертикально, при этом для предотвращения его движения удерживали удерживающей пипеткой 3 за его нижнюю часть и мягко надавливали на его верхнюю часть разрезающей пипеткой 2, чтобы получить энуклеированный ооцит. Энуклеированный ооцит промывали три раза промывающей средой ТСМ199 и инкубировали в культуральной среде ТСМ199. После этого полученные ранее донорские клетки переносили в энуклеированные ооциты с помощью микроманипулятора. Сначала 4 мкл инъецируемой микрокапельки наносили на середину рабочей чашки, используя раствор РНА-Р, полученный смешиванием 400 мкл промывающего раствора ТСМ199 и 100 мкл исходного раствора РНА-Р (фитогемагглютинина) (0,5 мг/мл в промывающем растворе ТСМ199). И затем две микрокапельки донорских клеток наносили, одну выше, а другую ниже инъецируемой микрокапельки, на ту же самую рабочую чашку, используя PBS, содержащий 1% FBS. После того как эти микрокапельки были покрыты сверху минеральным маслом, рабочую чашку помещали на стол микроманипулятора. Установленную на микроманипуляторе разрезающую пипетку заменили инъекционной пипеткой. Энуклеированные ооциты промывали три раза промывающей средой ТСМ199 и переносили в инъекционную микрокапельку. Донорские клетки набирали в инъекционную пипетку и вносили в инъекционную микрокапельку. На фигуре 4 представлен процесс переноса соматических клеток в энуклеированный ооцит. Как показано на фигуре 4, чтобы получить реконструированный эмбрион, энуклеированный ооцит размещали, ориентируя его разрез по направлению 1 часа, фиксировали с помощью удерживающей пипетки и вводили донорскую клетку через разрез, применяя инъекционную пипетку и гидравлическое давление. Эмбрион промывали три раза промывающей средой ТСМ199 и инкубировали в ней. Пример 3: Слияние методом электрошока и активация Реконструированный эмбрион подвергали слиянию методом электрошока, используя электроклеточный манипулятор (ЕСМ 2001, ВТХ, USA), с последующей активацией. 15 мкл раствора маннита, содержащего 0,28 М маннита, 0,5 мМ HEPES (рН 7,2), 0,1 мМ MgS04 и 0,05% BSA, добавляли к культуральной среде, содержащей реконструированные эмбрионы, используя ротовую пипетку для промывания. После одноминутной инкубации в вышеописанной среде эмбрионы инкубировали в течение 1 мин в растворе маннита, дополненного промывающим раствором ТСМ199, и, наконец, переносили в раствор маннита, используя ротовую пипетку для промывания. Камеру (камера 3,2 мм, 453) электроклеточного манипулятора заполняли раствором маннита, дополненным промывающей средой ТСМ199, а затем в камеру помещали эмбрионы с частью их донорских клеток со стороны катода. После того как эмбрионы были дважды подвергнуты электрослиянию посредством нанесения импульса DC от 0,75 до 2,00 кВ/см в течение 15 мкс, каждый раз с односекундным интервалом, эмбрионы переносили в промывающую среду ТСМ199 и промывали этой средой три раза вместо раствора маннита. Для того чтобы активировать слитые методом электрошока эмбрионы, последние инкубировали в темноте в течение 4 мин в растворе иономицина (Sigma Chemical Co., USA), который представлял собой промывающую среду ТСМ199, содержащую 5 мкМ иономицина и 1% BSA. Исходный раствор иономицина был приготовлен растворением 1 мг иономицина в 1,34 мл DMSO. Для удаления иономицина из эмбрионов активированные эмбрионы инкубировали в течение 5 мин в 35 мм чашке, содержащей промывающую среду ТСМ199, дополненную 10% FBS. Пример 4: Постактивация и выращивание in vitro эмбрионов, слитых методом электрошока Активированные эмбрионы подвергали постактивации в течение 4 ч в 25 мкл раствора циклогексимида (Sigma Chemical Co., USA), приготовленного добавлением исходного раствора циклогексимида (10 мг/мл в этаноле) к среде для культивирования in vitro, mTALP, в конечной концентрации 10 мкг/мл. Затем производили отбор эмбрионов и выбранные эмбрионы инкубировали в течение 7 дней в условиях 39oС, 5% CO2. При применении способа, описанного в примерах 1-4, получен эмбрион Bos taurus coreanae посредством использования клеток уха корейской коровы (Bos taurus coreanae) в качестве донора ядра, и эмбрион был передан для депонирования в Корейскую коллекцию видов культур, КСТС (Korean Collection for Type Cultures; KRIBB #52, Oun-dong, Yusong-ku, Taejon, 305-333, Republic of Korea) 31 декабря 1999 под регистрационным номером КСТС 0719ВР. Пример 5: Получение эмбриона при использовании клеток уха коровы Гольстейн Получен еще один эмбрион, SNU2 (Бычий эмбрион NT), с применением того же способа, который описан в Примерах 1-4, за исключением того, что использовали клетки уха и ооциты коровы Гольстейн в качестве донора ядра и реципиентного ооцита, соответственно. Эмбрион был передан для депонирования в Корейскую коллекцию видов культур, КСТС (Korean Collection for Type Cultures; KRIBB #52, Oundong, Yusong-ku, Taejon, 305-333, Republic of Korea) 31 декабря 1999 под регистрационным номером КСТС 0753ВР. Пример 6: Замораживание и оттаивание эмбрионов и имплантация Для длительного хранения эмбрионы замораживали. Сначала среду для замораживания (см. Таблицы 8 и 9) распределяли в 35 мм чашках, а холодильник устанавливали на поддержание температуры 5oС. Выбранные для замораживания эмбрионы промывали PBS, содержащим 10% FBS, и инкубировали в среде для замораживания в течение 20 мин. Затем эмбрионы втягивали в 25 мл французскую соломинку с тем, чтобы в середине соломинки находилась среда замораживания, содержащая эмбрионы, и два слоя воздуха на обоих концах. После закупоривания соломинки с обоих концов нагреванием с использованием нагретого пинцета ее помещали в холодильник, выдерживали при -5oС в течение 5 мин и удаляли пинцетом, предварительно охлажденным жидким N2. После удаления соломинку охлаждали до -30oС со скоростью -0,3oС/мин, когда температура достигла -30oС, выдерживали в течение 10 мин. Наконец, эмбрионы хранили в резервуаре с жидким N2. Для оттаивания замороженных эмбрионов в 35 мм чашках готовили среду для оттаивания, содержащую PBS, дополненный 20% FBS, добавляли глицерин, чтобы получить среды для оттаивания, содержащие 0, 3 и 6% глицерина (см. Таблицы 8 и 10). Затем замороженную соломинку доставали из жидкого N2, выдерживали на воздухе в течение 5 с и оттаивали в контейнере (>20 см в диаметре), содержащем теплую воду (30oС). После оттаивания соломинку разрезали по воздушным слоям на обоих концах, отбирали среду, содержащую эмбрионы. Эмбрионы исследовали под микроскопом. Для удаления из эмбрионов среды замораживания эмбрионы последовательно инкубировали в среде оттаивания, содержащей 6, 3 и 0% глицерина, каждую в течение 5 мин. Оттаянный эмбрион помещали в PBS, содержащий 20% FBS, набирали в 0,25 мл соломинку. А затем эмбрион переносили в матку коровы-реципиента. Пример 7: Сравнение эмбрионов, полученных при использовании различных доноров ядер Для сопоставления различий между эмбрионами, полученными в результате применения различных доноров ядер, эмбрионы Bos taurus coreanae/TcEar (KCTC 0719BP) и SNU2 (КСТС 0753ВР), полученные в примере 4 и примере 5, соответственно, имплантировали коровам-реципиентам, и сравнивали следующие параметры: количество ооцитов, слитых методом электрошока, степень электрослияния (%), степень деления (%), количество (%) развившихся морул/бластоцитов, количество перенесенных эмбрионов и количество (%) потомства (см. Таблицу 11). Количество (%) морул/бластоцитов представляет пропорцию эмбрионов, развившихся до надлежащей стадии при выращивании in vitro перед имплантацией к общему количеству эмбрионов, полученных посредством переноса ядер. Как видно из Таблицы 11, не выявлено никаких значительных различий между клетками уха корейской коровы и Гольстейн как доноров ядер, когда сравнивали оба варианта с точки зрения продукции и культивирования эмбрионов. Этот результат свидетельствует о том, что способ получения клонированных коров данного изобретения может быть применим для других видов коров без каких-либо особенностей. Кроме широкого применения для получения доноров ядер, способ данного изобретения может существенно улучшить количественный выход реконструированных эмбрионов, поскольку количество (%) морул/бластоцитов и степень доставки в данном изобретении значительно выше, чем в способах предыдущего уровня техники (см. Goto et al., Anim. Sci. Journal, 70: 243-245, 1999; Zakhartchenko et al., J. Reprod. Fertil., 115, 325-331, 1999; Hill et al., Biol. Reprod., 62, 1135-1140, 2000; Kubota et al., Proc. Natl. Acad. Sci., USA, 94, 990-995, 2000). Пример 8: Получение эмбрионов посредством использования клеток матки корейской коровы в качестве донора ядра Эмбрион был получен посредством тех же процедур, которые описаны в Примерах 1-4 за исключением того, что донорские клетки получали из матки корейской коровы. Пример 9: Сравнение эмбрионов, полученных при использовании различных донорских тканей Для сопоставления различий между эмбрионами, произведенными при использовании различных донорских тканей, эмбрионы, полученные в примерах 4 и 8, соответственно, имплантировали коровам-реципиентам, как описано в примере 6, и исследовали таким же образом, как в примере 7 (см. Таблица 12). Как видно из Таблицы 12, не выявлено никаких существенных различий между разными тканями, использованными в качестве донорских клеток, когда сравнивали два варианта с точки зрения получения и культивирования эмбрионов. Этот результат показывает, что способ получения клонированных коров данного изобретения может быть применен ко многим типам клеток скорее, чем к специфическим соматическим клеткам. Как четко проиллюстрировано и объяснено выше, данное изобретение обеспечивает способ получения клонированных коров, включающий стадии созревания ооцитов in vitro, приготовления донорских соматических клеток и энуклеированных ооцитов, переноса ядер, электрослияния и последующей активации, постактивации и выращивания in vitro, и перенос эмбрионов в коровы-реципиенты. В соответствии со способом получения клонированных коров изобретения, клонированные коровы, производные соматических клеток, могут быть получены эффективным способом с применением реконструированных эмбрионов, полученных при помощи весьма успешной техники переноса ядер, которая делает возможным массовое производство фармацевтических препаратов и органов в медицинской промышленности и животноводческой индустрии и способствует ее универсальному применению во многих других родственных областях. Из предшествующих описаний различные модификации изобретения кроме способов, представленных и описанных в заявке, окажутся очевидными специалистам в данной области. Такие модификации также остаются в рамках формулы изобретения. 104 клеток/мл. Фигура 1 изображает соматические клетки, выделенные в качестве однотипных клеток для ядерного донора. С другой стороны, что касается реципиентных ооцитов, то фолликулы, размер которых составлял приблизительно 2-6 мм в диаметре, отсасывали из яичников корейских коров шприцем 10 мл с иглой 18G. Затем фолликулярную жидкость переносили в чашки, 100 мм, с сеткой (длина между линиями составляла 1 см), начерченной на дне чашки, и отбирали ооциты с однородной цитоплазмой и достаточным количеством слоев скоплений клеток вокруг них. Отобранные ооциты промывали три раза 2 мл промывающей среды ТСМ199 (см. Таблицу 4) в 35 мм чашках и впоследствии один раз культуральной средой ТСМ199 (см. Таблицу 5). Наконец, для получения реципиентных ооцитов ооциты выращивали в культуральной среде ТСМ199, содержащей 0,1% раствора эстрадиола (см. Таблицу 6), 2,5% раствор фолликуло-стимулирующего гормона (см. Таблицу 7) и 10% FBS. Пример 2: Перенос ядер соматических клеток Приготовленные в Примере 1 реципиентные ооциты промывали один раз промывающей средой ТСМ199 и переносили в 0,1% раствор гиалуронидазы (Sigma Chemical Co., USA), полученный смешиванием 1 мл промывающей среды ТСМ199 с 111 мкл исходного раствора гиалуронидазы (10 мг/мл промывающей среды ТСМ199). После того как скопления клеток были отделены от ооцитов в присутствии 0,1% гиалуронидазы, обнаженные ооциты промывали три раза и инкубировали в промывающей среде ТСМ199. Затем ооциты переносили в раствор цитохалазина В (Sigma Chemical Co. , USA), приготовленный смешиванием 1 мл промывающей среды ТСМ199, содержащей 10% FBS, с 1 мкл исходного раствора цитохалазина (7,5 мг/мл DMSO), и, используя микроманипулятор, разрезали блестящую оболочку каждого ооцита, чтобы сделать разрез, через который можно выдавить от 10 до 15% цитоплазмы ооцита для создания энуклеированного ооцита. Стадия энуклеации точнее поясняется следующим образом: рабочую чашку помещали на стол микроманипулятора, а микроманипулятор оснащали удерживающей пипеткой на его левой ручке и разрезающей пипеткой на его правой ручке. Затем устанавливали положение удерживающей пипетки и разрезающей пипетки в направлении 9 часов и 3 часов, соответственно, и настраивали для свободного движения во всех направлениях посредством размещения пипетки-контролера в середине. В дальнейшем эти две пипетки настраивали так, чтобы не допустить их соприкосновения с рабочей чашкой и, посредством движения пипеток вверх и вниз над микрокапелькой, устанавливали их кончики в середине микрокапельки. Затем ооциты переносили из промывающей среды ТСМ199 в раствор цитохалазина В, используя промывающие ротовые пипетки (>200 мкм внутренний диаметр). Микроманипулятор сначала фокусировали на ооците, используя его ручку грубой настройки и ручку тонкой настройки, и далее фокус регулировали движением двух пипеток вверх и вниз. Ооцит размещали, ориентируя его первичное полярное тельце в направлении 12 часов, а удерживающую пипетку размещали близко к ооциту в направлении 9 часов от ооцита, чтобы фиксировать ооцит посредством применения гидравлического давления. На фигуре 2 представлен процесс разрезания блестящей оболочки ооцита удерживающей и разрезающей пипетками. Как показано на фигуре 2, разрезающая пипетка 2 пронизывает ооцит в направлении от 1 часа к 11 часам с особой осторожностью, чтобы не повредить цитоплазму ооцита. После этого, чтобы отделить ооцит 3, к удерживающей пипетке 1 применяли гидравлическое давление, и эту пипетку приводили в контакт с разрезающей пипеткой, пронизывающей блестящую оболочку, окаймляющую верхнюю часть первичного полярного тельца, чтобы трением двух пипеток разрезать часть блестящей оболочки. Сделанный выше разрез на ооците использовали как для энуклеации, так и для введения донорских клеток. На фигуре 3 изображен процесс энуклеации, в результате которого из ооцита удаляется первичное полярное тельце и ядро. Как показано на фигуре 3, ооцит 3 размещали, ориентируя его разрез вертикально, при этом для предотвращения его движения удерживали удерживающей пипеткой 3 за его нижнюю часть и мягко надавливали на его верхнюю часть разрезающей пипеткой 2, чтобы получить энуклеированный ооцит. Энуклеированный ооцит промывали три раза промывающей средой ТСМ199 и инкубировали в культуральной среде ТСМ199. После этого полученные ранее донорские клетки переносили в энуклеированные ооциты с помощью микроманипулятора. Сначала 4 мкл инъецируемой микрокапельки наносили на середину рабочей чашки, используя раствор РНА-Р, полученный смешиванием 400 мкл промывающего раствора ТСМ199 и 100 мкл исходного раствора РНА-Р (фитогемагглютинина) (0,5 мг/мл в промывающем растворе ТСМ199). И затем две микрокапельки донорских клеток наносили, одну выше, а другую ниже инъецируемой микрокапельки, на ту же самую рабочую чашку, используя PBS, содержащий 1% FBS. После того как эти микрокапельки были покрыты сверху минеральным маслом, рабочую чашку помещали на стол микроманипулятора. Установленную на микроманипуляторе разрезающую пипетку заменили инъекционной пипеткой. Энуклеированные ооциты промывали три раза промывающей средой ТСМ199 и переносили в инъекционную микрокапельку. Донорские клетки набирали в инъекционную пипетку и вносили в инъекционную микрокапельку. На фигуре 4 представлен процесс переноса соматических клеток в энуклеированный ооцит. Как показано на фигуре 4, чтобы получить реконструированный эмбрион, энуклеированный ооцит размещали, ориентируя его разрез по направлению 1 часа, фиксировали с помощью удерживающей пипетки и вводили донорскую клетку через разрез, применяя инъекционную пипетку и гидравлическое давление. Эмбрион промывали три раза промывающей средой ТСМ199 и инкубировали в ней. Пример 3: Слияние методом электрошока и активация Реконструированный эмбрион подвергали слиянию методом электрошока, используя электроклеточный манипулятор (ЕСМ 2001, ВТХ, USA), с последующей активацией. 15 мкл раствора маннита, содержащего 0,28 М маннита, 0,5 мМ HEPES (рН 7,2), 0,1 мМ MgS04 и 0,05% BSA, добавляли к культуральной среде, содержащей реконструированные эмбрионы, используя ротовую пипетку для промывания. После одноминутной инкубации в вышеописанной среде эмбрионы инкубировали в течение 1 мин в растворе маннита, дополненного промывающим раствором ТСМ199, и, наконец, переносили в раствор маннита, используя ротовую пипетку для промывания. Камеру (камера 3,2 мм, 453) электроклеточного манипулятора заполняли раствором маннита, дополненным промывающей средой ТСМ199, а затем в камеру помещали эмбрионы с частью их донорских клеток со стороны катода. После того как эмбрионы были дважды подвергнуты электрослиянию посредством нанесения импульса DC от 0,75 до 2,00 кВ/см в течение 15 мкс, каждый раз с односекундным интервалом, эмбрионы переносили в промывающую среду ТСМ199 и промывали этой средой три раза вместо раствора маннита. Для того чтобы активировать слитые методом электрошока эмбрионы, последние инкубировали в темноте в течение 4 мин в растворе иономицина (Sigma Chemical Co., USA), который представлял собой промывающую среду ТСМ199, содержащую 5 мкМ иономицина и 1% BSA. Исходный раствор иономицина был приготовлен растворением 1 мг иономицина в 1,34 мл DMSO. Для удаления иономицина из эмбрионов активированные эмбрионы инкубировали в течение 5 мин в 35 мм чашке, содержащей промывающую среду ТСМ199, дополненную 10% FBS. Пример 4: Постактивация и выращивание in vitro эмбрионов, слитых методом электрошока Активированные эмбрионы подвергали постактивации в течение 4 ч в 25 мкл раствора циклогексимида (Sigma Chemical Co., USA), приготовленного добавлением исходного раствора циклогексимида (10 мг/мл в этаноле) к среде для культивирования in vitro, mTALP, в конечной концентрации 10 мкг/мл. Затем производили отбор эмбрионов и выбранные эмбрионы инкубировали в течение 7 дней в условиях 39oС, 5% CO2. При применении способа, описанного в примерах 1-4, получен эмбрион Bos taurus coreanae посредством использования клеток уха корейской коровы (Bos taurus coreanae) в качестве донора ядра, и эмбрион был передан для депонирования в Корейскую коллекцию видов культур, КСТС (Korean Collection for Type Cultures; KRIBB #52, Oun-dong, Yusong-ku, Taejon, 305-333, Republic of Korea) 31 декабря 1999 под регистрационным номером КСТС 0719ВР. Пример 5: Получение эмбриона при использовании клеток уха коровы Гольстейн Получен еще один эмбрион, SNU2 (Бычий эмбрион NT), с применением того же способа, который описан в Примерах 1-4, за исключением того, что использовали клетки уха и ооциты коровы Гольстейн в качестве донора ядра и реципиентного ооцита, соответственно. Эмбрион был передан для депонирования в Корейскую коллекцию видов культур, КСТС (Korean Collection for Type Cultures; KRIBB #52, Oundong, Yusong-ku, Taejon, 305-333, Republic of Korea) 31 декабря 1999 под регистрационным номером КСТС 0753ВР. Пример 6: Замораживание и оттаивание эмбрионов и имплантация Для длительного хранения эмбрионы замораживали. Сначала среду для замораживания (см. Таблицы 8 и 9) распределяли в 35 мм чашках, а холодильник устанавливали на поддержание температуры 5oС. Выбранные для замораживания эмбрионы промывали PBS, содержащим 10% FBS, и инкубировали в среде для замораживания в течение 20 мин. Затем эмбрионы втягивали в 25 мл французскую соломинку с тем, чтобы в середине соломинки находилась среда замораживания, содержащая эмбрионы, и два слоя воздуха на обоих концах. После закупоривания соломинки с обоих концов нагреванием с использованием нагретого пинцета ее помещали в холодильник, выдерживали при -5oС в течение 5 мин и удаляли пинцетом, предварительно охлажденным жидким N2. После удаления соломинку охлаждали до -30oС со скоростью -0,3oС/мин, когда температура достигла -30oС, выдерживали в течение 10 мин. Наконец, эмбрионы хранили в резервуаре с жидким N2. Для оттаивания замороженных эмбрионов в 35 мм чашках готовили среду для оттаивания, содержащую PBS, дополненный 20% FBS, добавляли глицерин, чтобы получить среды для оттаивания, содержащие 0, 3 и 6% глицерина (см. Таблицы 8 и 10). Затем замороженную соломинку доставали из жидкого N2, выдерживали на воздухе в течение 5 с и оттаивали в контейнере (>20 см в диаметре), содержащем теплую воду (30oС). После оттаивания соломинку разрезали по воздушным слоям на обоих концах, отбирали среду, содержащую эмбрионы. Эмбрионы исследовали под микроскопом. Для удаления из эмбрионов среды замораживания эмбрионы последовательно инкубировали в среде оттаивания, содержащей 6, 3 и 0% глицерина, каждую в течение 5 мин. Оттаянный эмбрион помещали в PBS, содержащий 20% FBS, набирали в 0,25 мл соломинку. А затем эмбрион переносили в матку коровы-реципиента. Пример 7: Сравнение эмбрионов, полученных при использовании различных доноров ядер Для сопоставления различий между эмбрионами, полученными в результате применения различных доноров ядер, эмбрионы Bos taurus coreanae/TcEar (KCTC 0719BP) и SNU2 (КСТС 0753ВР), полученные в примере 4 и примере 5, соответственно, имплантировали коровам-реципиентам, и сравнивали следующие параметры: количество ооцитов, слитых методом электрошока, степень электрослияния (%), степень деления (%), количество (%) развившихся морул/бластоцитов, количество перенесенных эмбрионов и количество (%) потомства (см. Таблицу 11). Количество (%) морул/бластоцитов представляет пропорцию эмбрионов, развившихся до надлежащей стадии при выращивании in vitro перед имплантацией к общему количеству эмбрионов, полученных посредством переноса ядер. Как видно из Таблицы 11, не выявлено никаких значительных различий между клетками уха корейской коровы и Гольстейн как доноров ядер, когда сравнивали оба варианта с точки зрения продукции и культивирования эмбрионов. Этот результат свидетельствует о том, что способ получения клонированных коров данного изобретения может быть применим для других видов коров без каких-либо особенностей. Кроме широкого применения для получения доноров ядер, способ данного изобретения может существенно улучшить количественный выход реконструированных эмбрионов, поскольку количество (%) морул/бластоцитов и степень доставки в данном изобретении значительно выше, чем в способах предыдущего уровня техники (см. Goto et al., Anim. Sci. Journal, 70: 243-245, 1999; Zakhartchenko et al., J. Reprod. Fertil., 115, 325-331, 1999; Hill et al., Biol. Reprod., 62, 1135-1140, 2000; Kubota et al., Proc. Natl. Acad. Sci., USA, 94, 990-995, 2000). Пример 8: Получение эмбрионов посредством использования клеток матки корейской коровы в качестве донора ядра Эмбрион был получен посредством тех же процедур, которые описаны в Примерах 1-4 за исключением того, что донорские клетки получали из матки корейской коровы. Пример 9: Сравнение эмбрионов, полученных при использовании различных донорских тканей Для сопоставления различий между эмбрионами, произведенными при использовании различных донорских тканей, эмбрионы, полученные в примерах 4 и 8, соответственно, имплантировали коровам-реципиентам, как описано в примере 6, и исследовали таким же образом, как в примере 7 (см. Таблица 12). Как видно из Таблицы 12, не выявлено никаких существенных различий между разными тканями, использованными в качестве донорских клеток, когда сравнивали два варианта с точки зрения получения и культивирования эмбрионов. Этот результат показывает, что способ получения клонированных коров данного изобретения может быть применен ко многим типам клеток скорее, чем к специфическим соматическим клеткам. Как четко проиллюстрировано и объяснено выше, данное изобретение обеспечивает способ получения клонированных коров, включающий стадии созревания ооцитов in vitro, приготовления донорских соматических клеток и энуклеированных ооцитов, переноса ядер, электрослияния и последующей активации, постактивации и выращивания in vitro, и перенос эмбрионов в коровы-реципиенты. В соответствии со способом получения клонированных коров изобретения, клонированные коровы, производные соматических клеток, могут быть получены эффективным способом с применением реконструированных эмбрионов, полученных при помощи весьма успешной техники переноса ядер, которая делает возможным массовое производство фармацевтических препаратов и органов в медицинской промышленности и животноводческой индустрии и способствует ее универсальному применению во многих других родственных областях. Из предшествующих описаний различные модификации изобретения кроме способов, представленных и описанных в заявке, окажутся очевидными специалистам в данной области. Такие модификации также остаются в рамках формулы изобретения.
ФОРМУЛА ИЗОБРЕТЕНИЯ1. Способ получения клонированной коровы, который включает в себя стадии (i) получения линий донорных соматических клеток, полученных у коровы; (ii) созревания ооцитов, полученных из яичника in vitro; (iii) удаления скоплений клеток, окружающих ооциты, разрезания части блестящей оболочки зрелых ооцитов, чтобы образовалась щель, и выдавливания порции цитоплазмы, включающей в себя первичное полярное тельце, чтобы получить энуклеированные реципиентные ооциты; (iv) переноса ядра в реципиентный ооцит с помощью инъецирования цельных донорских клеток через щель в энуклеированные реципиентные ооциты с последующим электрослиянием и активацией полученных в результате электрослияния клеток, чтобы получить эмбрионы; (v) постактивации и культивирования эмбриона in vitro; (vi) переноса культивированного эмбриона в корову-реципиента с тем, чтобы подвергнуть эмбрион полной программе эмбрионального развития и родов, в результате чего будет получен клонированный теленок. 2. Способ получения клонированной коровы по п.1, отличающийся тем, что приготовленные на стадии (i) линии соматических клеток включают в себя клетки, собранные из промывающей матку жидкости, эндометрия, маточной трубы, уха или мышцы, скоплений клеток или фетальных фибробластов. 3. Способ получения клонированной коровы по п.1, отличающийся тем, что линии соматических клеток поддерживаются путем субкультивирования, культивирования на минимальной сывороточной среде или замораживания. 4. Способ получения клонированной коровы по п.1, отличающийся тем, что скопления клеток, окружающих ооциты, на стадии (iii) удаляются физически с помощью обдирающей пипетки после обработки гиалуронидазой. 5. Способ получения клонированной коровы по п.1, отличающийся тем, что энуклеация ооцита на стадии (iii) осуществляется посредством образования щели на ооците путем разрезания его микроманипулятором; размещения ооцита таким образом, чтобы полученная щель была сориентирована вертикально, и фиксирования нижней части ооцита удерживающей пипеткой, чтобы предотвратить движение клетки; сдавливания верхней части ооцита разрезающей пипеткой для выдавливания через щель 10-15% цитоплазмы ооцита, содержащей первичное полярное тельце. 6. Способ получения клонированной коровы по п.1, отличающийся тем, что электрослияние на стадии (iv) осуществляется дважды с односекундным интервалом путем приложения импульса постоянного тока от 0,75 до 2,00 кВ/см, каждый раз в течение 15 мкс. 7. Способ получения клонированной коровы по п.1, отличающийся тем, что активация на стадии (iv) происходит одновременно с электрослиянием, при условии, что электрослияние проводится в среде, содержащей Са2+. 8. Способ получения клонированной коровы по п.1, отличающийся тем, что активация на стадии (iv) проводится в растворе иономицина в темноте, при условии, что электрослияние выполняется в среде без Са2+. 9. Способ получения клонированной коровы по п.1, отличающийся тем, что постактивация на стадии (v) осуществляется путем культивирования эмбриона в растворе циклогексимида или в растворе DMAP (4-диметиламинопурина). 10. Способ получения клонированной коровы по п.1, отличающийся тем, что культивирование in vitro на стадии (v) осуществляется путем культивирования постактивированного эмбриона в среде mTALP, mSOF или mCR2aa. 11. Способ получения клонированной коровы по п.1, отличающийся тем, что, кроме того, включает в себя стадию хранения эмбриона, культивированного in vitro на стадии (v), для последующего использования после замораживания эмбриона в среде для замораживания, содержащей пенициллин-стрептомицин, СаСl2, глюкозу, MgClq2, Na-пируват и забуференный фосфатом физиологический раствор.Популярные патенты: 2075933 Композиция для иммунизации растений от различных фитопатогенов ... и бактериальных патогенов при предпосевной обработке семян и клубней и в период вегетации. Оценивали качество и количество собранного урожая. С помощью данной композиции удавалось индуцировать устойчивость вегетирующих растений, семян и клубней к ряду патогенных грибов, бактерий, вирусов и нематод. Пример 1. Картофель. Схема опыта. Вариант 1. Двукратное применение композиции: предпосадочное опрыскивание семенных клубней из расчета 1/4 таблетки композиции (0,075 г) и 7-8 л воды на 1 т клубней; опрыскивание растений в фазу бутонизации из расчета 1 таблетка композиции (0,3 г) и 400 л воды на 1 га. Вариант II. Двукратное применение препарата крезацин, 99,9% (этанол) кр. п. ... 2154931 Корнеуборочная машина ... После того, как корнеплоды, очистившись от примесей, попадают на полотно транспортера 8, и далее они транспортируются им на выгрузной элеватор 15, который и загружает ими транспортное средство. Для замены загруженного транспортного средства на свободное, без остановки корнеуборочной машины, с помощью гидроцилиндров 14, подключенных к гидросистеме корнеуборочной машины (на фиг. 1 не показано), поворачиваются плоскости 11 таким образом, что их нижние концы смыкаются и под щетками 10 образуется бункер для корнеплодов тарельчатой формы. При этом верхние части плоскостей 11 приближаются к валикам стенок 9 и все корнеплоды попадают в указанный бункер. Поперечный транспортер 8 и выгрузной ... 2154939 Способ выращивания кроликов и устройство для его осуществления ... ее в клетке, имеющей лазы с задвижками, затем после случки переводят самку в гнездовое отделение, в котором проводят окрол с последующим в нем содержанием крольчихи с крольчатами до достижения последними 15-дневного возраста, после чего крольчат временно, не более чем на час, изолируют в гнезде, а самку допускают к случке, при этом на 30 день производят отъем крольчат от крольчихи и перемещение их в выростное отделение, а затем в отделение доращивания секции для крольчат с помощью подвижно-поворотных перегородок при достижении крольчатами необходимого для реализации возраста их удаляют из клетки через открывающуюся торцевую стенку крайнего отделения клетки. 2. Способ по п. 1, ... 2076594 Установка для промышленного разведения дождевых червей ... субстрата при минимальной трудоемкости на этой операции. Таким образом, предлагаемое техническое решение обладает элементами новизны и промышленной полезности. На фиг. 1 показана принципиальная схема установки (цеха) для промышленного разведения дождевых червей из навоза и растительных остатков при круглогодичном использовании, вертикальный разрез по А-А; на фиг.2 то же, в плане; на фиг.3 -сечение Б-Б; на фиг.4 узел I верхний торец тоннеля с питающим бункером; на фиг.5 вариант исполнения бункера для эксплуатации в зимний период; на фиг.6 узел II размещение рыхлителей в тоннеле; на фиг.7 план В-В образование полости после рыхлителя; на фиг.8 узел соединения поддонов; на фиг.9 узел ... 2084132 Устройство для выращивания растений ... дна горшка равен минимальному радиусу вписанного в указанный многоугольник круга, касающегося хотя бы трех его сторон, а площадь сечения на расстоянии (0,65 1,00)H до дна горшка равна (1,0 0,9)S, где S площадь многоугольника, H высота горшка, причем в хотя бы один из горшков вмонтированы электроды или датчики влажности, и в хотя бы один из горшков вмонтированы датчики солевого состава, горшки установлены с возможностью перемещения относительно пленочного пористого материала, а приводы для перемещения держателей связаны с горшками через блок управления с датчиками влажности и солевого состава. Заявляемое изобретение позволяет достичь следующего технического результата. Выполнение ... |
Еще из этого раздела: 2492650 Микроэмульсионная бактерицидная композиция 2502793 Масло, семена и растения подсолнечника с модифицированным распределением жирных кислот в молекуле триацилглицерина 2475020 Способ подбора лучших сортов опылителей для насаждений яблони 2261597 Способ борьбы с нематодами - возбудителями болезней сельскохозяйственных растений 2272399 Зерноуборочный комбайн 2253239 Способ производства средства для обработки растений (варианты) 2080774 Способ изготовления брикетов для выращивания растений и устройство для его осуществления 2073513 Способ профилактики технологических стрессов молодняка крупного рогатого скота 2414113 Способ и комплекс для обработки зерна, семян или плодоовощной продукции озоном 2195808 Способ хранения корнеплодов, картофеля и капусты |
Изобретения в сельском хозяйстве
Обработка почвы в сельском и лесном хозяйствах
Посадка, посев, удобрение
Уборка урожая, жатва
Обработка и хранение продуктов полеводства и садоводства
Садоводство, разведение овощей, цветов, риса, фруктов, винограда, лесное хозяйство
Новые виды растений или способы их выращивания
Производство молочных продуктов
Животноводство, разведение и содержание птицы, рыбы, насекомых, рыбоводство, рыболовство
Поимка, отлов или отпугивание животных
Консервирование туш животных, или растений или их частей
Биоцидная, репеллентная, аттрактантная или регулирующая рост растений активность химических соединений или препаратов
Хлебопекарные печи, машины и прочее оборудование для хлебопечения
Машины или оборудование для приготовления или обработки теста
Обработка муки или теста для выпечки, способы выпечки, мучные изделия
|
|
||