Способ получения человеческого гранулоцитарного колониестимулирующего фактораПатент на изобретение №: 2207373 Автор: Прокофьев М.И., Городецкий С.И., Косоруков В.С., Мезина М.Н., Букреев Ю.М., Барышников А.Ю. Патентообладатель: ООО "Новэнерго", Прокофьев Михаил Иванович, Косоруков Вячеслав Станиславович Дата публикации: 27 Июня, 2003 Начало действия патента: 25 Апреля, 2002 Адрес для переписки: 142712, Московская обл., Ленинский р-н, п/о Горки Ленинские, ул. Новое шоссе, 89, кв.8, М.И.Прокофьеву Изображения 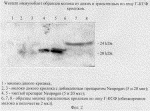 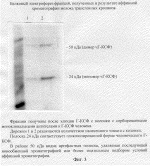 Предложен способ получения чГ-КСФ с молоком трансгенных животных. В качестве трансгенных животных были использованы кролики с гибридным геном h-GM-1 человека, который содержит геномную копию гена гранулоцитарного колониестимулирующего фактора человека и регуляторные элементы генов молока, направляющие выделение белка чГ-КСФ в молоко. Способ позволяет получать очищенный белок чГ-КСФ в гомогенном состоянии, пригодном для дальнейшего использования в фармакологии и получении лекарственной формы препарата чГ-КСФ. 4 з.п. ф-лы, 3 ил. Изобретение относится к биотехнологии. Гранулоцитарный колониестимулирующий фактор человека (чГ-КСФ) является гликопротеином, состоящим из 174 аминокислот. чГ-КСФ необходим для прогрессии от плюрипотентной стволовой клетки до зрелых дифференцированных клеток крови и обладает также способностью влиять на функцию последних. чГ-КСФ широко используется в онкологии для лечения нейтропении, а также с целью предупреждения миелосупрессии при интенсификации химиотерапии. Применение этого препарата позволяет резко уменьшить число опасных для жизни инфекционных осложнений, которые могут развиться у больных с нейтропенией, получающих цитостатики при злокачественных немиелоидных опухолевых заболеваниях, а также при трансплантации костного мозга (Morstyn G, et al. Clinical studies with granutients receiving cytoxic chemoterapy. Behring Inst. mitt., 1988, Aug. (83), 234-239.). Известен метод получения чГ-КСФ из таких источников, как кровь, где он присутствует в норме. Этот метод трудоемок и дорог в связи с низкой концентрацией биологически активных веществ и ограниченным количеством исходного сырья (Werner RG, Berthold W. Purification of proteins produced by biotechnological process. Arzneimittelforschung, 1988, Mart, 38(3):422-428). Другим недостатком этого метода является возможность присутствия в конечной продукции инфекционных для человека агентов, например, таких как вирусы. Известен также способ получения чГ-КСФ с использованием рекомбинантных микроорганизмов. Обычно в качестве продуцента используется адаптированный штамм Escherichia coli (Perez-perez J., et al. Supplementation improves the periplasmic production of human granulocyte-colony stimulating factor in Escherichia coli, Biochem. Biophys. Reg. Commun, 1995, 16, 210 (2), 524-529). Однако получение рекомбинантных белков с использованием прокариот не обеспечивает таких посттрансляционных модификаций как гликолизилирование, силиконирование, правильный фолдинг белка и отщепление лишнего метионина с N-конца белка, что приводит к снижению устойчивости и биологической активности получаемого препарата. В настоящее время имеется импортный препарат нейпоген (Neupogen, фирма Hofman la Roche), который представляет собой негликолизированный рекомбинантный человеческий гранулоцитарный колониестимулирующий фактор, имеющий на N-конце аминоскислотной цепи дополнительный метионин. Это высокоочищенный белок биологически активен, хотя и в меньшей степени, в сравнении с его гликозилированной формой чГ-КСФ. Известен метод получения гликолизированной формы гранулоцитарного колониестимулирующего фактора путем использования в качестве продуцента культуры клеток млекопитающих. Обычно для этого используется культура клеток яичника китайского хомячка (СНО) (Rotondaro L. et al., High-level expression of a cDNA for human granulocyte colony - stimulating factor in Chinese Hamster ovary cells. Effect ot 31-noncoding seguences mol. Biotechnol., 1997, Jun; 7(3), 231-240; Nolloway W. DNA technology in the production of glycosylated recombinant human granulocyte colony stimulating factor, Eur. J. Cancer, 1994; 30A Suppl. 3, 2-6; Nissen C. Glycosylation of recombinant human granulocyte colony stimulating factor: implications for stability and potency. Eur. J. Cancer, 1994, 30A, Suppl. 3, 12-14). Гликозилированная форма гранулоцитарного колониестимулирующего фактора в 2 раза превосходит по способности стимулировать рост колоний гранулоцитов и в 4 раза быстрее обеспечивает проявление положительного эффекта по сравнению с негликолизированным рекомбинантным белком, получаемым с использованием микроорганизмов. Несмотря на то, что в рекомбинантном белке в культуре клеток млекопитающих происходят все необходимые посттрансляционные модификации, концентрация получаемого рекомбинантного белка очень низкая, а сам процесс культивирования дорогостоящий и требует высокого технологического обеспечения. Известен метод получения рекомбинантных белков с использованием трансгенных животных, которые секретируют эти вещества с молоком (патент RU # 2157846 С1 "Способ получения трансгенного животного, экспрессирующего в молочной железе гранулоцитарный колониестимулирующий фактор человека и гибридный ген h-GM-1 для осуществления способа"). Метод базируется на микроинъекции генетической конструкции в пронуклеус оплодотворенной яйцеклетки в половые пути ложно беременной самки. Генетическая конструкция обеспечивает секрецию рекомбинантного белка только в молочной железе лактирующей трансгенной самки. Для этого структурный ген в генетической конструкции помещен под контроль регуляторных элементов генов белков молока. Этот метод, в отличие от использования культуры бактериальных клеток, обеспечивает получение высокой идентичности рекомбинантного белка нативному, выделенному из крови, и, по сравнению с использованием метода культуры клеток млекопитающих, значительно снижает стоимость получаемого продукта. Это обусловлено тем, что в молочной железе плотность продуцирующих клеток в 100 раз выше, чем в жидкой культуре: в тканях органа содержится 109 клеток/грамм, тогда как в культуре тканей 107 клеток/мл (Н. Meade а. С. Ziomer, Urine as a substitute for milk. Nature Biotechnology, 1998, v. l6, January, 21-22). К тому же стоимость содержания и доения трансгенных животных составляет лишь 1/10 часть стоимости обслуживания биореактора. Предложен способ получения гранулоцитарного колониестимулирующего фактора человека (чГ-КСФ) с молоком трансгенных животных. Последовательность ДНК гена, кодирующего белок чГ-КСФ представлена на фиг.1. Получение трансгенных животных является одним из наиболее перспективных направлений для получения различных рекомбинантных белков. Существует большое количество научно-исследовательских работ, позволяющих использовать данную технологию для получения трансгенных животных-продуцентов биологически активных белков человека. Спектр видов животных, способных выступить в роли продуцентов, достаточно широк: кролик (Brem G. et al. Expression of synthetic cDNA sequences encoding human insulin-like grows factor-1 in the mammary gland of transgenic rabbits. Gene, 1994, v. 149, p. 351-355), корова (Rudolph N.S. Biopharmaceutical production in transgenic livestock. Trends in Biotechnology, 1999, sept., v. 17, p. 367-374; van Berkel P.H. et al. Large scale production of recombinant human lactoferrin in the milk of transgenic cows. Nature biotechnology, 2002, v. 20, p. 484-487), коза (Ebert K.M. et al. Transgenic production of a variant of human tissue-type plasminogen activator in goat milk: generation of transgenic goats and analysis of expression. Biotechnology, 1991, v. 9, sept., p. 835-838), овца (Wright G. et al. High level expression of active human alpha-1-antiyrypsin in the milk of transgenic sheep. Biotechnology, 1991, v. 9, sept., p. 830-834), свинья (Velander W. et al. High-level expression of a heterologous protein in the milk of transgenic swine using the cDNA encoding human protein C. Proc. Natl. Acad. Sci. USA, 1992, v. 89, p. 12003-12007). Использование мышей для этих целей ограничено тем, что получаемый за время лактации объем молока не превышает 2-5 мл, что абсолютно нетехнологично. С точки зрения технологии получения трансгенных животных принципиального различия между перечисленными видами нет. Во всех случаях используется микроинъецирование генетической конструкции в пронуклеус оплодотворенной яйцеклетки с последующей подсадки ее в половые пути синхронизированной самки-реципиента. Введение генетического материала в животное с целью дальнейшей его экспрессии может осуществляться несколькими способами. - Микроинъецирование раствора генетического материала в пронуклеус оплодотворенной яйцеклетки является наиболее ранним разработанным методом. Этим методом получено наибольшее количество трансгенных животных в мировой практике (Juhani Janne et. al. Transgenic Animals as Bioproducers of Therapeutic Proteins Trends in Molecular Medicine, Annals of Medicine, 1992, v. 24, p. 273-280). - Инфекция ранних яйцеклеток, бластоцист, ранних предимплантационных эмбрионов и тканей взрослого животного (например, молочной железы) различными вирусными векторами. Наиболее часто используют ретровирусные и лентивирусные вектора (Rudolf Jaenisch. Transgenic Animals Science, 1988, v. 240, р. 1468-1473). - Перенос трансфецированных ядер эмбриональных или соматических клеток в энуклеированную яйцеклетку. Метод позволяет с большой эффективностью получать заведомо трансгенных животных с использованием заранее трансфецированной и проверенной культуры клеток соответствующего вида (Angelika E. Schnieke et. al. Human Factor IX Transgenic Sheep Produced by Transfer of Nuclei from Transfected Fetal Fibroblasts Science, 1997, v. 278, p. 2130-2133). В качестве трансгенных животных были использованы кролики с гибридным геном h-GM-1 человека, который содержит геномную копию гена гранулоцитарного колониестимулирующего фактора человека и регуляторные элементы генов молока, направляющие выделение белка чГ-КСФ в молоко. Исходных трансгенных самцов спаривали с нетрансгенными самками и получили трансгенное потомство. Определение трансгенности потомства проводили методом полимеразной цепной реакции с праймерами специфичными к последовательности вектора h-GM-1. Трансгенных самок спаривали с нетрансгенными или трансгенными самцами и, после родов, собирали молоко для выделения чГ-КСФ. Сбор молока проводили ручным или машинным доением после предварительной обработки животного окситоцином. Концентрацию и биологическую активность чГ-КСФ человека в молоке трансгенных кроликов определяли несколькими методами. Биологическую активность тестировали по степени стимулирования пролиферации и колониеобразования стволовых гранулоцитарных клеток костного мозга человека. Концентрацию белка чГ-КСФ в молоке тестировали иммуноферментным методом с использованием моноклональных антител против чГ-КСФ (ELISA). Выделение чГ-КСФ из молока трансгенных кроликов проводили следующим образом: молоко, собранное от крольчихи, центрифугировали на лабораторной центрифуге при 10 тыс. g в течение 30 минут. Удаляли жировую фракцию, отбирали супернатант и использовали его для дальнейшего выделения чГ-КСФ. Полученный раствор разводили в два раза буфером А (20мМ фосфат калия рН 6.5, 3.5М мочевины, 200мМ ЕДТА, 0.2мМ ДТТ) и интенсивно перемешивали на мешалке для. Эти достигалось разрушение мицелл молока и превращение его в истинный раствор белков. В полученный раствор добавляли 1/5 объема насыщенного раствора сульфата аммония (4М) до конечной концентрации 1М. Для контроля потерь белка чГ-КСФ в процессе выделения определяли его количество в растворе методом иммуноферментного анализа ELISA. Затем полученный раствор наносили на колонку К-16 (размер 20 см) заполненную октил-сефарозой (Octyl Sepharose 4 Fast Flow, кат 17-0946-10, фирмы "Амершам-Фармация"), уравновешенной в буфере В (10 мМ фосфата калия рН 6.5, 1.8М мочевины, 10мМ ЕДТА, 1М сульфата аммония, 0.2мМ ДТТ). Скорость прохождения раствора через колонку составляла 20 мл/час. Элюцию проводили с использованием линейного градиента с понижающейся концентрацией сульфата аммония до нуля и при повышении рН до 7.5, а детергента Tween-20 до 0.2% от буфера В к буферу С (10 мМ калий фосфата рН 6.5, 1.8М мочевины, 10мМ ЕДТА, 1М сульфата аммония, 0.2мМ ДТТ, 0.2% Tween-20). Скорость прохождения раствора через колонку составляла 20 мл/час. Всего собирали 22 фракции. Основная часть балластных белков выходит во фракциях 10-19. чГ-КСФ элюируется в конце градиента во фракциях 20-21. Потери активности чГ-КСФ в этом процессе составили 30%. Элюаты, содержащие чГ-КСФ, объединяли, разводили в 4 раза буфером (2мМ фосфат калия рН 7.2, 0.15М хлорид калия), и наносили на колонку К-9 (размер 6 см) наполненную иммуносорбентом с иммобилизованными на нем моноклональными антителами против чГ-КСФ (носитель активированная бромцианом sepharose 4B фирмы "Амершам-Фармация"). Промывали колонку буфером (2мМ фосфат калия рН 7.2, 0.5М хлорид калия) около 10 объемов колонки. Элюцию с колонки проводили 0.1М лимонной кислотой. Полученный элюат диализовали против буфера (2мМ фосфат калия рН 7.5), концентрировали различными методами и использовали для дальнейшей работы. Пример 1 Образцы молока для тестирования на присутствие чГ-КСФ и его биологическую активность брали от трансгенных кроликов. Молоко трансгенных кроликов перед тестированием фракционировали центрифугированием для отделения жировой фракции и испытывали в различных разведениях. Моделью для тестирования служили стволовые гемопоэтические клетки доноров костного мозга, культивируемые в полужидких питательных средах. Ядерные клетки костного мозга культивировали in vitro в среде RPMI 1640 с 0,3% агаром, 30% эмбриональной бычьей сывороткой (FBS) и содержащей необходимые компоненты для поддержания роста гемопоэтических клеток в краткосрочной культуре (14 дней) при 37oС в атмосфере 5% СО2. Результат роста клеток в соответствующих условиях оценивали по их количеству на 14 день культивирования визуальным подсчетом в камере Горяева. В качестве положительного контроля клетки культивировали с гранулоцитарным колониестимулирующим фактором человека, полученным из культуры клеток млекопитающих - стандартным коммерческим препаратом, используемым в клинической практике Granocyte (международное наименование филграстим, производство фирмы Rhone Poulenc Rorer). Отрицательным контролем считали рост клеток в присутствии экстрактов из молока нетрансгенного кролика в соответствующих разведениях, а также без исследуемых добавок. Одновременно прослеживали способность исследуемых клеток костного мозга в присутствии экстрактов из молока кроликов трансгенных по чГ-КСФ образовывать гранулоцитарно-макрофагальные колонии культивированием их в полужидкой среде с метилцеллюлозой (Metho Cult Medium), используемой для анализа гемопоэтических клеток на колониеобразование по методу, предложенному The Terry Fox Laboratory Media Preparation Service (1992). В качестве отрицательного контроля использовали интактные клетки (ИТК), а в качестве положительного контроля - коммерческий препарат чГ-КСФ Granocyte в разведениях от 1:10 до 1:10000. В культурах клеток, инкубированных с образцами экстрактов молока трансгенных кроликов, число жизнеспособных клеток в 2-3 раза превышало аналогичный показатель в контрольной интактной культуре стволовых клеток (с базовым содержанием ростового фактора) и в культуре с добавлением молока нетрансгенных кроликов. По морфологическим признакам клетки, выращенные в культуре с добавлением экстрактов из молока трансгенных кроликов, обладали более высокой степенью дифференцировки, чем клетки в культурах с отрицательным контролем. Ориентировочная концентрация белка чГ-КСФ, полученная на основе сравнения удельной биологической активности с препаратом Granocyte, в протестированных образцах молока составляет 50-100 мг/л в эквиваленте на активность препарата филграстим. Пример 2 Определение концентрации чГ-КСФ иммуноферментным методом проводили в иммунологических плашках на наборе ProCon G-CSF (производство фирмы 000 "Протеиновый контур", г. Санкт-Петербург). Буфера А, В и С поставляются в составе набора. Первые антитела (АТ-1) разводили в буфере Ар (100 мкл антител на 10 мл буферы). Вносили в лунку планшета 1 по 100 мкл раствора первых антител. Инкубировали планшет при непрерывном встряхивании в течение одного часа при комнатной температуре. Конъюгат вторых антител (АТ-2) разводили в 20 раз в буфере С. В лунку А2 добавляли 25 мкл стандарта чГ-КСФ (0,5 мкг/мл), тщательно перемешивали и титровали кратно 2, перенося по 25 мкл в следующую ячейку и тщательно перемешивали, до лунки Е1 (до концентрации стандарта 31,25 нг/мл). Лунка А1 оставалась для отрицательного контроля. В остальные лунки планшета 2 вносили по 25 мкл образцов обезжиренного молока. Во все ячейки планшета 2, содержащие образцы стандарта и испытуемые образцы, добавляли по 100 мкл раствора вторых антител. Планшет 2 инкубировали в течение 40-60 мин при комнатной температуре при непрерывном встряхивании. Удаляли жидкость из ячеек планшета 1 и трижды промывали буфером В 300 мкл на одну ячейку (состав буфера В согласно производителя набора). Проводили полную аспирацию оставшейся жидкости. Дважды промывали ячейки планшета струей дистиллированной воды. Осушали планшет путем постукивания по поверхности лабораторного стола. Готовили раствор субстрата с красителем. Для этого смешивали в равных отношениях растворы с маркировкой "Субстрат" и "Реагент", учитывая, что на 1 стрип требуется 3,2 мл готового раствора. Вносили во все лунки по 100 мкл раствора субстрата с красителем. Инкубировали стрипы 5-15 мин при комнатной температуре на шейкере. Наблюдали развитие голубой окраски. Останавливали реакцию добавленем 50 мкл раствора 1N серной кислоты в каждую лунку. Производили учет результатов с использованием автоматического фотометра для микропланшетов при длине волны 450 нм. Строили калибровочную кривую "оптическая плотность-концентрация" пользуясь данными по концентрациям, указанным для растворов стандартов. Определяли концентрацию чГ-КСФ в образцах. В качестве отрицательного контроля использовали молоко нетрансгенного кролика, а в качестве положительного контроля - коммерческий препарат чГ-КСФ, Granulocyte производства фирмы Rone Poulenc Rorer. Содержание чГ-КСФ в различных пробах молока трансгенных кроликов варьировало в пределах 20-100 мг/л. При сравнении данных по определяемому количеству чГ-КСФ в молоке с интактными казеиновыми мицеллами и в образцах с разрушенными мицеллами было получено увеличение показаний в 1,6 раза. Это говорит о том, что значительная часть белка чГ-КСФ содержится внутри мицеллярной структуры. Пример 3 Идентификацию чГ-КСФ в молоке трансгенных кроликов проводили методом электрофореза белков в полиакриламидном геле с последующим переносом на мембрану и окраской моноклональными антителами против чГ-КСФ конъюгированными с щелочной фосфатазой. В качестве отрицательного контроля использовали молоко нетрансгенного кролика, а в качестве положительного - коммерческий препарат негликозилированного чГ-КСФ Neupogen (фирма Amgen). Негликозилированная форма чГ-КСФ имеет молекулярную массу 19,6 кДа. Гликозилированная форма имеет молекулярную массу 23-24 кДа в зависимости от вариантов гликозилирования (Nicola N.A., J. Cell. physiol., 1981, 109, 253). На электрофорез наносили обезжиренные фракции молока от трансгенных и нетрансгенных кроликов, а также положительный контроль Neupogen в чистом виде и в смеси с молоком нетрансгенного кролика (фиг.2). После окраски мембраны специфическими антителами было обнаружено, что в пробах положительного контроля содержится белок размером около 20 кДа, а в пробах молока трансгенных кроликов содержится белок размером около 24 кДа, специфически связывающийся с моноклональными антителами против чГ-КСФ. Данные результаты показывают, что в молоке трансгенных кроликов содержится гликозилированная форма чГ-КСФ. Пример 4 Выделение чГ-КСФ из молока трансгенных кроликов проводили следующим образом: молоко, собранное от крольчихи, цент рифугировали на лабораторной центрифуге при 10 тыс. g в течение 30 минут. Удаляли жировую фракцию, отбирали супернатант и использовали его для дальнейшего выделения чГ-КСФ. Полученный раствор разводили в два раза буфером А (20мМ фосфат калия рН 6.5, 3.5М мочевины, 200мМ ЕДТА, 0.2мМ ДТТ) и интенсивно перемешивали на мешалке для. Эти достигалось разрушение мицелл молока и превращение его в истинный раствор белков. В полученный раствор добавляли 1/5 объема насыщенного раствора сульфата аммония (4М) до конечной концентрации 1М. Для контроля потерь белка чГ-КСФ в процессе выделения определяли его количество в растворе методом иммуноферментного анализа ELISA. Затем полученный раствор наносили на колонку К-16 (размер 20 см), заполненную октил-сефарозой (Octyl Sepharose 4 Fast Flow, кат 17-0946-10, фирмы "Амершам-Фармация"), уравновешенной в буфере В (10мМ фосфата калия рН 6.5, 1.8М мочевины, 10мМ ЕДТА, 1М сульфата аммония, 0.2мМ ДТТ). Скорость прохождения раствора через колонку составляла 20 мл/час. Элюцию проводили с использованием линейного градиента с понижающейся концентрацией сульфата аммония до нуля и при повышении рН до 7.5, а детергента Tween-20 до 0.2% от буфера В к буферу С (10 мМ калий фосфата рН 6.5, 1.8М мочевины, 10мМ ЕДТА, 1М сульфата аммония, 0.2мМ ДТТ, 0.2% Tween-20). Скорость прохождения раствора через колонку составляла 20 мл/час. Всего собирали 22 фракции. Основная часть балластных белков выходит во фракциях 10-19. чГ-КСФ элюируется в конце градиента во фракциях 20-21. Потери активности чГ-КСФ в этом процессе составили 30%. Элюаты, содержащие чГ-КСФ, объединяли, разводили в 4 раза буфером (2мМ фосфат калия рН 7.2, 0.15М хлорид калия), и наносили на колонку К-9 (размер 6 см), наполненную иммуносорбентом с иммобилизованными на нем моноклональными антителами против чГ-КСФ (носитель активированная бромцианом sepharose 4B фирмы "Амершам-Фармация"). Промывали колонку буфером (2мМ фосфат калия рН 7.2, 0.5М хлорид калия) около 10 объемов колонки. Элюцию с колонки проводили 0.1М лимонной кислотой. Фракции нейтрализовали 1М гидроксида калия и образцы наносили на PAG-SDS электрофорез. Часть проб осаждали трихлоруксусной кислотой, центрифугировали, осадки промывали 70% метанолом, растворяли в электродном буфере, доводили буфером для нанесения до требуемого объема, прогревали и наносили на гель. Окрашивали с помощью красителя Кумаси G-250 (фиг.3). Как видно на электрофореограмме в элюате содержится две полосы белка с молекулярной массой примерно 25 000 и 50 000 дальтон. Более легкая полоса соответствует размеру гликозилированного чГ-КСФ. Минорная тяжелая полоса является димерной формой чГ-КСФ. Данная технология может применяться для получения субстанции чГ-КСФ, используемой для приготовления лекарственной формы препарата. Список литературы 1. Morstyn G, et al. Clinical studies with granutients receiving cytoxic chemoterapy. Behring Inst. mitt., 1988, Aug. (83), 234-239. 2. Werner RG, Berthold W. Purification of proteins produced by biotechnological process. Arzneimittelforschung 1988 Mar; 38(3):422-428. 3. Perez-perez J., et al. Supplementation improves the periplasmic production of human granulocyte-colony stimulating factor in Escherichia coli, Biochem. Biophys. Reg. Commun, 1995, 16, 210 (2), 524-529. 4. Rotondaro L. et al. High-level expression of a cDNA for human granulocyte colony - stimulating factor in Chinese Hamster ovary cells. Effect ot 31-noncoding seguences mol., Biotechnol., 1997, Jun; 7(3) 231-240. 5. Nollowway DNA technology in the production of glycosylated recombinant human granulocyte colony stimulating factor, Eur. J. Cancer, 1994; 30A Suppl. 3., 2. 6. Nissen С. Glycosylation of recombinant human granulocyte colony stimulating factor: implications for stability and potency. Eur. J. Cancer, 1994, 30A, Suppl. 3, 12-14. 7. H. Meade а. С. Ziomer. Urine as a substitute for milk. Nature Biotechnology, 1998, v. l6, Jannary, 21-22. 8. Патент RU #2157846 Cl "Способ получения трансгенного животного, экспрессирующего в молочной железе гранулоцитарный колониестимулирующий фактор человека и гибридный ген h-GM-1 для осуществления способа". 9. Nicola N.A. J. Cell. physiol, 1981, 109, 253. 10. Brem G. et al. Expression of synthetic cDNA sequences encoding human insulin-like grows factor-1 in the mammary gland of transgenic rabbits. Gene, 1994, v. 149, p. 351-355. 11. Rudolph N.S. Biopharmaceutical production in transgenic livestock. Trends in Biotechnology, 1999, sept., v. 17, p. 367-374. 12. van Berkel P.H. et al. Large scale production of recombinant human lactoferrin in the milk of transgenic cows. Nature biotechnology, 2002, v. 20, p. 484-487. 13. Ebert K.M. et al. Transgenic production of a variant of human tissue-type plasminogen activator in goat milk: generation of transgenic goats and analysis of expression. Biotechnology, 1991, v. 9, sept., p. 835-838. 14. Wright G. et al. High level expression of active human alpha-1-antiyrypsin in the milk of transgenic sheep. Biotechnology, 1991, v. 9, sept., p. 830-834. 15. Velander W. et al. High-level expression of a heterologous protein in the milk of transgenic swine using the cDNA encoding human protein C. Proc. Natl. Acad. Sci. USA, 1992, v. 89, p. 12003-12007. 16. Juhani Janne et. al. Transgenic Animals as Bioproducers of Therapeutic Proteins Trends in Molecular Medicine, Annals of Medicine, 1992, v. 24, p. 273-280. 17. Rudolf Jaenisch. Transgenic Animals Science, 1988, v. 240, p. 1468-1473. 18. Angelika E. Schnieke et. al. , Human Factor IX Transgenic Sheep Produced by Transfer of Nuclei from Transfected Fetal Fibroblasts Science, 1997, v. 278, p. 2130-2133. Формула изобретения1. Способ получения человеческого гранулоцитарного колониестимулирующего фактора (чГ-КСФ), являющегося гликозилированной формой, идентичной нативному белку Г-КСФ человека, включающий стадии создания генетической конструкции ДНК, обеспечивающей экспрессию чГ-КСФ, которая несет геномные последовательности чГ-КСФ, приведенные на фиг.1, и включающей в себя некодирующие белок последовательности, введения конструкции в животное, получения трансгенного животного, продуцирующего чГ-КСФ в молоке лактирующей самки, выделения указанного чГ-КСФ, включающего центрифугирование, хроматографию и конечную доочистку целевого продукта. 2. Способ по п.1, отличающийся тем, что введение генетической конструкции в животное производится методами микроинъецирования в ядра эмбриональных клеток, различными способами трансфекции в клетки эмбрионов или взрослого животного. 3. Способ по п.1, в котором указанным животным является кролик, корова, коза, овца, свинья. 4. Способ по п. 1, отличающийся тем, что на стадии выделения чГ-КСФ проводят обезжиривание молока путем центрифугирования с последующей экстракцией гептаном, октаном или иным органическим растворителем, образующим с водой двухфазную структуру. 5. Способ по п.4, в котором обезжиренное молоко хроматографируют и доочищают на иммуносорбенте, несущем специфические антитела против чГ-КСФ.MM4A Досрочное прекращение действия патента Российской Федерации на изобретение из-за неуплаты в установленный срок пошлины за поддержание патента в силе Дата прекращения действия патента: 26.04.2004 Извещение опубликовано: 20.04.2006 БИ: 11/2006 Популярные патенты: 2420940 Энергосберегающий способ обеззараживания семян люпина от антракноза ... до необходимой температуры при конвективном подводе тепла в потоке нагретого до необходимой температуры теплоносителя. Теплоноситель при относительной влажности 30-40% продувают через слой семян толщиной, не превышающей 0,15-0,20 м. Семена в потоке теплоносителя при достигнутой температуре выдерживают в течение 1,5-2,0 часов. Температуру теплоносителя поддерживают на уровне, определяемом по соотношению: Топт=(123,9 125,0)-0,021W0 3+0,806W0 2-11,28W0, где W0 - исходная влажность семян, %; Топт - оптимальная температура теплоносителя при его относительной влажности в пределах 30-40%, °С. Изобретение позволит снизить энергозатраты на 35-40%, повысить надежность ... 2496298 Узел крепления пальцев подборщика ... прототипа, содержит кронштейн, жестко установленный на граблине. Пружинный палец закреплен на кронштейне посредством резьбового соединения, включающего болт, гайку, плоскую и пружинную шайбы.Отсутствие пружинного фиксатора и использование в узле крепления резьбового соединения повышает надежность крепления пальца и снижает вероятность захватывания стеблей крепежными элементами. Хотя и не исключает ее полностью, поскольку существует возможность захвата стеблей гайкой и выступающей частью болта. Другим недостатком прототипа является трудоемкость сборочно-разборочных операций при обслуживании подборщика, в частности то, что для монтажа и демонтажа пальцев требуется свинчивание и ... 2287923 Роторный энергосберегающий мостовой агрегат для сельскохозяйственных работ ... сумме составляет 24,8 кг/га, для РЭМА аналогичного тягового класса - 11,2 кг/га, т.е. в 2,2 раза меньше.Возможность производить перекрестный посев за один проход машины, при всех прочих равных условиях, дает прибавку урожая в среднем на 10%. Другим преимуществом перекрестного сева перед рядовым является то, что на пересечении рядов образуются решетки, связывающие ряды. При рядовом же севе ряды растений при созревании ложатся друг на друга, образуя эффект В«доминоВ» - полегание хлебов. Формула изобретения Роторный энергосберегающий мостовой агрегат для сельскохозяйственных работ, включающий раму, смонтированную на ней бесконечную направляющую, в которой установлен тяговый ... 2479996 Экологический комплекс для аквакультуры и рекультивации морских вод ... приводит к трудоемкости обслуживания комплекса. Задачей предлагаемого изобретения является улучшение качества биологической очистки морской воды.Поставленная задача достигается тем, что в экологический комплекс для рекультивации морских вод и аквакультуры, содержащий вертикальные коллекторы для культивирования моллюсков, подвешенные на горизонтальных тросах, аэратор, устройства для выращивания водорослей, поплавки, ловушки осадков, которые содержат конические элементы, основания которых обращены вверх для сбора осадков, а вершины вниз для подачи осадков в сборные элементы, согласно изобретению дополнительно включены культиватор корма для моллюсков, помпа, распределительная ... 2498561 Способ тандемного возделывания сельскохозяйственных культур для повышения производства пищевых зерновых культур ... с сентября до апреля в агроклимате Индо-Гангских равнин.В данном изобретении предложен способ тандемного возделывания сельскохозяйственных культур для повышения производства пищевых зерновых культур при использовании сортов культур с признаками фенологической пластичности и устойчивости к температуре. Зерновая хлебопекарная пшеница и горчица для производства масла из семян представляют собой традиционные сельскохозяйственные культуры зимнего сезона (раби) в равнинах северной Индии/Индо-Гангских равнинах. Данная область испытывает понижающиеся уровни теплой погоды и долгие дни в сентябре, октябре и ноябре, прогрессирующее повышение и затем снижение холодных условий и короткие дни ... |
Еще из этого раздела: 2228022 Способ ведения виноградных кустов 2402189 Роликовая сортировальная машина 2060618 Пневматический высевающий аппарат 2015633 Способ переработки отходов животноводческих комплексов и устройство для его осуществления 2165141 Тепличный гидропонный комплекс 2080765 Комбайн для уборки овощей 2057432 Биологический состав кузнецова для подсочки деревьев, в том числе каучуконосов (варианты), и способ его приготовления 2178965 Картофелекопатель ручной мотыжный 2160981 Способ создания плантаций солодки голой на обесструктуренных почвах в орошаемом земледелии 2289908 Способ получения рассады стевии |
Изобретения в сельском хозяйстве
Обработка почвы в сельском и лесном хозяйствах
Посадка, посев, удобрение
Уборка урожая, жатва
Обработка и хранение продуктов полеводства и садоводства
Садоводство, разведение овощей, цветов, риса, фруктов, винограда, лесное хозяйство
Новые виды растений или способы их выращивания
Производство молочных продуктов
Животноводство, разведение и содержание птицы, рыбы, насекомых, рыбоводство, рыболовство
Поимка, отлов или отпугивание животных
Консервирование туш животных, или растений или их частей
Биоцидная, репеллентная, аттрактантная или регулирующая рост растений активность химических соединений или препаратов
Хлебопекарные печи, машины и прочее оборудование для хлебопечения
Машины или оборудование для приготовления или обработки теста
Обработка муки или теста для выпечки, способы выпечки, мучные изделия
|
|
||