Микрокапсулы и способ их полученияПатент на изобретение №: 2159037 Автор: Герберт Бенсон ШЕР (US), Джин Линг ЧЕН (CN) Патентообладатель: ЗЕНЕКА ЛИМИТЕД (GB) Дата публикации: 20 Ноября, 2000 Начало действия патента: 7 Ноября, 1994 Адрес для переписки: 129010, Москва, ул. Большая Спасская 25, стр.3, ООО "Городисский и Партнеры", Лебедевой Н.Г. Изображения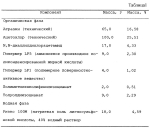   Описываются микрокапсулы, полученные реакцией полимеризации на границе раздела фаз, содержащие твердый агрохимический материал 0,1-55 мас.%, суспендированный в перемешивающейся с водой органической жидкости, 0,01-10 мас. % неионного диспергатора, активного на границе раздела фаз и не действующего как эмульгатор. В качестве агрохимического агента и органической жидкости микрокапсула может содержать гербицид. В качестве полимерной стенки микрокапсулы содержат полимер на основе смеси изоцианатов или этерифицированного мочевиноформальдегидного форполимера. Способ получения микрокапсул состоит в получении суспензии агрохимического агента в органической жидкости, содержащей указанные диспергатор и форполимеры и введении полученной суспензии в водную фазу, содержащую защитный коллоид и поверхностно-активное вещество с последующим перемешиванием смеси при высоком сдвиге и регулировании при необходимости температуры и/или рН эмульсии до образования микрокапсул. Технический результат - упрощение процесса микрокапсулирования. 2 с. и 16 з.п. ф-лы, 2 табл. , , ОПИСАНИЕ ИЗОБРЕТЕНИЯ К ПАТЕНТУИзобретение относится к микрокапсулам, которые содержат твердое биологически активное соединение, суспендированное в жидкости, и способам их получения, а также к применению таких микрокапсул. Технология микрокапсулирования существует в течение ряда лет. Микрокапсулы имеют целый ряд областей применения, особенно для содержания красителей, чернил, химических реагентов, фармацевтических соединений, ароматизирующих веществ и особенно агрохимических материалов, которыми являются фунгициды, бактерициды, инсектициды, гербициды и тому подобное. Разработка и применение микрокапсулирования описывается в работе Gordon Marrs, Herbert B. Scher, "Controlled Delivery of Crop Protection Agents", chapter 4 (London, Taylor and Francis 1990). Как описывается в этой работе, имеется три способа формования микрокапсул: i) физические методы, ii) методы фазового разделения и iii) полимеризации на границе раздела фаз. В третьем из этих способов стенки микрокапсул обычно формуются из полимерного материала, полученного реакцией полимеризации, которая предпочтительно имеет место на границе раздела двух фаз, обычно водной фазы и водонесмешиваемой органической фазы. Таким образом, они могут быть получены из эмульсии воды в масле или более обычно из эмульсии масло в воде. Основным патентом, рассматривающим технологию микрокапсулирования, является патент США N 4285720. В этом патенте стенки микрокапсул получаются из полимеров, образованных реакциями изоцианатных мономеров. Второй способ формования микрокапсул полимеризацией на границе раздела фаз описывается в патенте США 4956129. В этом патенте стенки полимерной микрокапсулы получаются из этерифицированных мочевина-формальдегидных форполимеров, которые претерпевают самополиконденсацию в кислотных условиях. Предлагаются различные улучшения этих способов. Например, патент США 4140516 описывает применение фазообменных катализаторов, тогда как патент США 4448929 описывает применение улучшенного защитного коллоида. Однако во всех этих патентах способ применим только к жидкостям, т.е. к материалам, которые являются жидкостью при окружающей температуре, или к растворам. К сожалению, многие биологически активные соединения являются твердыми веществами с высокими точками плавления и являются труднорастворимыми в наиболее широко используемых растворителях. Выгоды микрокапсулирования, например регулируемое высвобождение и повышенная сохраняемость эффективности, не являются легко достижимыми при использовании известных способов. Также известно заключение твердых веществ в полимерную матрицу. Так в патенте США 4428983 описывается способ получения кристаллов кварца в полимерной матрице. Патент использует термин "суспензия" для описания пасты кристаллов кварца в форполимере, но эта публикация не описывает получение микрокапсул, содержащих твердое вещество, суспендированное в жидкости. Имеется большое число публикаций, относящихся к получению и применению микрокапсулированных рецептур галогенацетанилидных гербицидов. Они включают патенты США 4280833, 4417916, 4534783, 4563212 и 4640709. Дополнительно патент США 4936901 описывает гербицидные композиции, которые являются сухими сыпучими диспергируемыми в воде гранулированными рецептурами, содержащими смесь микрокапсул из водонерастворимого пестицида (включая галогенацетанилидный гербицид), капсулированного в полимерную оболочку, и по крайней мере одного другого пестицида, который является некапсулированным. Такие композиции являются необходимыми, так как нет известных удовлетворительных способов получения микрокапсулы, содержащей твердый биологически активный гербицид, суспендированный в жидкости. Патент GB-A-2011341 описывает способ капсулирования, использующий полимеризацию на границе раздела фаз, который может быть применен к твердым веществам, суспендированным в жидкостях. Неудивительно, что капсулы, содержащие биологически активное твердое вещество, суспендированное в жидкости, не получены до настоящего времени, так как проблемы, с которыми сталкиваются в производстве такой капсулы, являются труднопреодолимыми. Например, при формовании таких капсул из эмульсии масло в воде могут встретиться следующие трудности. Во-первых, должна быть получена стабильная суспензия твердого вещества в водонесмешивающейся жидкости. Если используются диспергаторы или поверхностно-активные вещества, они не должны мешать другим процессам диспергирования, используемым при получении микрокапсул. Во-вторых, суспензия должна быть диспергирована в воде с получением стабильных, хорошо диспергированных капелек. Для биологически активных веществ предпочтительно иметь очень мелкие капельки жидкости, диспергированной в воде, для обеспечения высокой удельной поверхности в получаемых микрокапсулах. Для получения очень мелких капелек требуются высокие усилия сдвига, что обуславливает тенденцию к разрушению капелек и/или высвобождению твердого вещества из суспензии. Для достижения хорошего диспергирования и получения стабильных капелек обычно требуются поверхностно-активные вещества. В-третьих, присутствие одного или более поверхностно-активных веществ может сделать нестабильной систему диспергированных капелек, и может иметь место явление фазовой инверсии, т.е. вода образует мелкие капельки в жидкости, эмульсия вода в масле. В-четвертых, твердое вещество, суспендированное в водонесмешивающейся жидкости, подвержено миграции в водную фазу, особенно когда используются эмульгирующие поверхностно-активные вещества. Теперь установлено, что указанные выше проблемы могут быть преодолены и что можно получить микрокапсулированные композиции, содержащие твердое биологически активное соединение, суспендированное в жидкости. В соответствии с изобретением микрокапсулирования рецептура твердого биологически активного соединения, суспендированного в жидкости, получается способами фазового разделения или полимеризации на границе раздела фаз. Предпочтительным способом является полимеризация на границе раздела фаз, в частности, получение капсул из эмульсии масло в воде способами, такими как описанные в патентах США 4285720 и 4956129, модифицированными, как описано здесь. Твердым биологически активным соединением предпочтительно является агрохимическое вещество, в частности гербицид. Предпочтительными гербицидами являются S-триазины, например атразин, симазин, пропазин, ципрозин; сульфонилмочевины, например хлорсульфурон, хлоримуронэтил, метсульфуронметил, тиаметуронметил; и трикетоны, например сулкотрион. Особенно предпочтительным гербицидом является атразин. Другим пригодным соединением является фунгицид (E)-метил-2-[2-(6-(2-цианофенокси)пиримидин-4-илокси)фенил]-3- метоксипропеноат. Жидкостью, в которой суспендируется твердое вещество, может, соответственно, быть второй гербицид, особенно тиокарбамат или галогенацетанилид и предпочтительно ацетохлор. Галогенацетанилиды, особенно подкласс, обычно называемый d-хлорацетанилидами, являются общеизвестным классом гербицидных агентов и используются и предлагаются для использования в ряде сельскохозяйственных и несельскохозяйственных применений. Некоторые из более известных представителей этого класса включают в себя a-хлор-6"-этил-N-(2-метокси-1-метилэтил)-ацетанилид (метолахлор), N-бутоксиметил-d-хлор-2",6"-диэтилацетанилид (бутахлор), d-хлор-2",6"-диэтил-N-метоксиметилацетанилид (алахлор), 2-хлор-N-(этоксиметил)-6"-этил-o-ацетотолуидид (ацетохлор) и d-хлор-N-изопропилацетанилид (пропахлор). Многие другие соединения этого типа рассматриваются в многочисленных патентах. Тиокарбаматы являются хорошо известным классом гербицида, который включает: Молинат - S-этил-гексагидро-1H-азепин-1-карботиоат, Бутилат - S-этил-диизобутилтиокарбамат, ЭПТК - этилдипропилтиолкарбамат, Триаллат - 2,3,3-трихлораллил-диизопропилтиолкарбамат, Диаллат - цис-1-транс-2,3-дихлораллил-диизопропилтиолкарбамат, Вернолат - S-пропилдипропилтиолкарбамат. Микрокапсулы изобретения, соответственно, содержат 0,1-55 мас.% биологически активных соединений. Альтернативно, жидкостью может быть любой органический растворитель, который не смешивается с водой, не растворяет биологически активное твердое вещество в значительной степени и является достаточно полярным для растворения форполимеров, используемых для формования стенок микрокапсул. Соответствующими примерами таких растворителей являются ароматические соединения, такие как ксилолы или нафталины, особенно Солвессо 200; алифатическое соединение, такое как алкилэфиры, особенно алкилацетаты, например Эксксат 700 - Эксксэт 1000; алкилфталаты, такие как диэтилфталат, дибутилфталат; спирты, такие как изопропиловый спирт; кетоны, такие как ацетофенон, циклогексанон. Растворителем может быть смесь более одного соединений. Может присутствовать противодействующее средство для любого гербицида, и многие такие противодействующие средства или антидоты хорошо известны в технике. Предпочтительные типы для использования с галогенацетанилидными гербицидами включают в себя дихлорацетамиды, такие как дихлорамид (N,N-диаллилдихлорацетамид); 2,2,5-триметил-3-дихлорацетилоксазолидин (R-29148), N-дихлорацетил-1-окса-4-азепино[4,5] декан (AD-67); 4-дихлорацетил-2,3-дигидро-3-метил-1,4-бензоксазин (CGA-154281); 1-(дихлорацетил)гексагидро-3,3,8a-триметилпиррол-[1,2-a] -пиримидин-6(2H)-он и N-(1,3-диоксолан-2-ил-метил)-N-(2-пропенил)-2,2-дихлорацетамид (PPG-1292). Эти и другие дихлорацетамиды описаны, например, в патентах США 4124372, 4256481, 4294764, 4448960, 4601745, 4618361, 4708735 и 4900350. Дополнительные известные типы противодействующих средств или антидотов включают в себя некоторые оксим-производные (например, патенты США 4070389 и 4269775), тиазол-карбоновые кислоты и производные (например, патент США 4199506), галогенацилтетрагидроизохинолины (например, патент США 4755218), арилциклопропанкарбонитриды (например, патент США 4859232) и 1,8-нафталиновая кислота, ее ангидрид и производные. При включении противодействующих средств или антидотов они обычно содержатся в органической или водонесмешивающейся фазе. Предпочтительными материалами для микрокапсулы являются полимочевина, полученная, как описано в патенте США 4285720, или мочевина-формальдегидный полимер, как описано в патенте США 4956129. Полимочевина является особенно предпочтительной. Вкратце способ содержит следующие стадии: Стадия 1. Получение твердого биологически активного материала с требуемым размером частиц соответствующим способом измельчения. Предпочтительный средний размер частиц твердого вещества составляет 0,01-50,0 мкм, предпочтительно 1-10 мкм, еще более предпочтительно 1-5 мкм. Стадия 2. Суспендирование твердого биологически активного материала в органической жидкости. Жидкость является предпочтительно плохим растворителем для твердого материала, т.е. она не растворяет больших количеств твердого материала. Жидкость также должна не смешиваться с водой, но быть достаточно полярной для растворения форполимеров, используемых в процессе микрокапсулирования. Жидкость предпочтительно содержит диспергатор, способный удерживать твердое вещество в жидкости, но который не дает твердому веществу экстрагироваться в воду, когда суспензия диспергируется в воде. Кроме того, когда суспензия добавляется к воде, диспергатор не должен позволять, чтобы имела место фазовая инверсия, т.е. вода не должна образовывать эмульсию с органической жидкостью. Точный выбор диспергаторов зависит от выбора твердого вещества и жидкости, но предпочтительными диспергаторами являются неионные поверхностно-активные вещества, которые действуют при пространственном затруднении и являются активными только на границе раздела твердое вещество/органическая жидкость и не действуют как эмульгирующие агенты. Такие диспергаторы, соответственно, получаются из i) полимерной цепи, имеющей сильное сродство к жидкости, и ii) группы, которая сильно абсорбируется твердым материалом. Примеры таких диспергаторов включают фталоцианин производные, полиоксиалкиленамин производные, полиаминовые полимеры, полимеры сложных полиэфиров, различные производные поликонденсированных жирных кислот, включая производные металлов, производные амина и производные аммония, которые доступны под торговыми марками Hypermer и Atlox от фирмы ICI Americas Inc., Wilmington, Delaware, т.е. Atlox LP1, Atlox LP2, Atlox LP3, Atlox LP4, Atlox LP5, Atlox LP6, Atlox PS2, Atlox PS3, Hypermer PS1, Hypermer PS2, Hypermer PS3 и Hypermer LP2; и винилпирролидоновые полимеры, доступные под торговыми марками Agrimer AL от фирмы GAF, такие как Agrimer AL-220 и Agrimer AL-216. Торговые марки, указанные выше, соответствуют следующим соединениям. Atlox и Hypermer LP1 - полимерное поверхностно-активное вещество, Atlox и Hypermer LP2 - производное фталоцианина; Atlox LP3 - производное металла поликонденсированной жирной кислоты; Atlox LP4 - аминовое производное поликонденсированной жирной кислоты; Atlox и Hypermer LP5 - аммониевое производное поликонденсированной жирной кислоты; Atlox LP6 - раствор конденсата полиамин/жирная кислота; Hypermer PS1 - фталоцианиновое производное; Atlox и Hypermer PS2 - производное полиоксалкиленамина; Atlox и Hypermer PS3 - полимер полиамина и сложного полиэфира; Agrimer AL-220 - алкилированные винилпирролидоновые сополимеры (алкилированные на 80%); Agrimer AL-216 - алкилированные винилпирролидоновые сополимеры (алкилированные на 50%). Вообще, используемый интервал концентрации диспергатора составляет от примерно 0,01 до примерно 10 мас.% по отношению к органической фазе, но может также использоваться более высокая концентрация. Альтернативно, операция Стадий 1 и 2 могут отличаться проведением предварительного процесса измельчения для снижения размера частиц твердого вещества, после чего твердый биологически активный материал суспендируется в органической жидкости (измельчение в среде). Стадия 3. Получается физическое диспергирование водонесмешиваемой фазы в водной фазе. Для получения соответствующей дисперсии органическая фаза добавляется к водной фазе при перемешивании. Для диспергирования органической фазы в жидкой фазе используется соответствующее диспергирующее средство. Средством может быть любое высокосдвиговое устройство, обеспечивающее получение требуемого размера капелек (и соответствующего размера частиц микрокапсул) в интервале от примерно 1 до примерно 200 мкм. Предпочтительно размер капелек составляет от примерно 1 до примерно 30 мкм, наиболее предпочтительно от примерно 3 до примерно 20 мкм, в среднем. Как только получается надлежащий размер капелек, диспергирующее средство отключается. Для остальной части процесса требуется только слабое перемешивание. Водонесмешиваемая фаза содержит твердое биологически активное соединение, суспендированное в капсулируемой жидкости, полученной, как описано выше на Стадиях 1 и 2. Водная фаза состоит из воды и материала, называемого "защитным коллоидом". Предпочтительно она дополнительно содержит поверхностно-активное вещество. Вообще, поверхностно-активным веществом или поверхностно-активными веществами в этой фазе могут быть анионные или неионные поверхностно-активные вещества с интервалом значений ГЛБ (HLB) от примерно 12 до примерно 16, что является достаточно высоким для образования стабильной эмульсии масло в воде. Если используется более одного поверхностно-активного вещества, отдельные поверхностно-активные вещества могут иметь значения более низкие чем 12 или более высокие чем 16. Однако в комбинации суммарное значение ГЛБ поверхностно-активных веществ находится в пределах 12-16. Соответствующие поверхностно-активные вещества включают в себя полиэтиленгликольные эфиры линейных спиртов, этоксилированные нонилфенолы, нафталинсульфонаты и т.п. Другие соответствующие поверхностно-активные вещества включают блок-сополимеры пропиленоксида и этиленоксида и анионные/неионные смеси. Предпочтительно гидрофобная часть поверхностно-активного вещества имеет химические характеристики, подобные органической жидкости. Так, когда органической жидкостью является ароматический растворитель, поверхностно-активным веществом будет этоксилированный нонилфенол. Особенно предпочтительными поверхностно-активными веществами являются Терджитол NP7, Терджитол NP40 и Терджитол 15-S-20. Вообще, интервал концентраций поверхностно-активного вещества в способе составляет от примерно 0,01 до примерно 10,0 мас.% по отношению к водной фазе, но могут также использоваться более высокие концентрации поверхностно-активного вещества. Защитный коллоид, присутствующий в водной (или непрерывной) фазе, должен сильно абсорбироваться на поверхности капелек масла. Соответствующие коллоидообразующие материалы включают в себя один или более представителей из группы: полиалкилаты, метилцеллюлоза, поливиниловый спирт, полиакриламид, полиметилвиниловый эфир/малеиновый ангидрид), привитые сополимеры поливинилового спирта и метилвиниловый эфир/малеиновая кислота (гидролизованный метилвиниловый эфир/малеиновый ангидрид; см. патент США 4448929, который поэтому приводится здесь в качестве ссылки) и лигносульфонаты щелочных или щелочноземельных металлов. Предпочтительно, однако, защитный коллоид выбирается из лигносульфонатов щелочных и щелочноземельных металлов, причем наиболее предпочтительны лигносульфонаты натрия. Особенно предпочтительные коллоиды также содержат поливиниловый спирт. Должно присутствовать достаточное количество коллоида, чтобы он мог покрыть всю поверхность всех капелек органической жидкости. Используемое количество защитного коллоида зависит от различных факторов, таких как молекулярная масса, совместимость и т.д. Защитный коллоид может добавляться к водной фазе перед добавлением органической фазы, или он может добавляться к вышеуказанной системе после добавления органической фазы или ее дисперсии. Защитный коллоид обычно присутствует в водной фазе в количестве от примерно 0,1 до примерно 10,0 мас.%. Любое поверхностно-активное вещество, используемое в водной фазе, не должно вытеснять защитный коллоид с поверхности капелек органической жидкости. Если водонесмешивающийся жидкостью является тиокарбамат или галогенацетанилидный гербицид, то в зависимости от назначения или применения этого микрокапсулированного продукта композиции данного изобретения могут также включать противодействующее гербициду вещество или антидот. В случае включения противодействующих веществ или антидотов, они обычно содержатся в органической или водонесмешивающейся фазе. Предпочтительный средний размер частиц капелек водонесмешивающейся жидкости, содержащей биологически активное твердое вещество, составляет 1-200 мкм, предпочтительно 1-30 мкм, более предпочтительно 3-20 мкм. Размер частиц может регулироваться в соответствии с конечным использованием микрокапсул путем регулирования скорости и времени перемешивания и путем выбора поверхностно-активных веществ и используемого количества поверхностно-активных веществ. Для того, чтобы получить микрокапсулы, органическая жидкость и/или вода должны содержать один или более материалов, которые могут реагировать с образованием полимера на границе раздела между органической жидкостью и водой. В способе, описанном в патенте США 4285720, полиизоцианаты растворяются в органической фазе (т.е., на Стадии 2 вышеуказанного способа), и полимеризация имеет место при гидролизе форполимеров на границе раздела вода/органическая жидкость с образованием аминов, которые, в свою очередь, взаимодействуют с негидролизованными мономерами с образованием полимочевинной стенки микрокапсулы. Могут использоваться отдельное соединение или смесь двух или более полиизоцианатов. Смеси являются предпочтительными. Из полиизоцианатов предпочтительными являются полиметиленполифенилизоцианат (ПАФИ) и изомерные смеси толуолдиизоцианат (ТДИ). Особенно предпочтительными являются смеси полиметиленполифенилизоцианата с изомерными смесями толуолдиизоцианата в массовом соотношении ПАФИ:ТДИ от примерно 1:30 до примерно 4: 1, особенно от 1:10 до 1:1. Количество органического полиизоцианата, используемое в способе, определяет содержание стенки микрокапсул. Вообще, стенка микрокапсулы составляет от примерно 2 до примерно 75 мас. % микрокапсулы. Наиболее предпочтительно стенка составляет от примерно 4 до примерно 15 мас.% микрокапсулы. Дисперсия поддерживается в температурном интервале от примерно 20 до примерно 90oC, предпочтительно при 40-60oC, в течение периода времени, пока имеет место реакция конденсации с образованием полимочевины на поверхности раздела между капельками органической фазы и водной фазой. Тиокарбамат или галогенацетанилидный гербицид может быть использован в качестве растворителя полиизоцианатов. Альтернативно, могут быть использованы такие растворители, как ксилол (см. канадский патент 1094402). Другая соответствующая система для образования микрокапсул описывается в патенте США 4956129, в котором полимер образуется из этерифицированного мочевина-формальдегидного форполимера, в котором 50-98% метилольных групп этерифицируется C4-10-спиртом. Самоконденсация форполимера имеет место под воздействием тепла при низком pH, например при pH 0-4 при 20-100oC. Для образования микрокапсул температура двухфазной смеси повышается до значения от примерно 20 до примерно 90oC, предпочтительно от примерно 40 до примерно 90oC, наиболее предпочтительно от примерно 40 до примерно 60oC. В зависимости от системы значение pH может регулироваться до соответствующего уровня. Далее приводятся примеры получения композиций данного изобретения. Общая методика Органическую фазу сначала получают суспендированием твердого биологического активного материала в органической жидкости. К жидкости также добавляют диспергаторы и полимеры и, необязательно, предохраняющий агент в зависимости от используемого гербицида. Твердое вещество или измельчают перед добавлением его к жидкости или измельчают после добавления к жидкости до среднего размера частиц от 0,01 до 50,0 мкм. В последующих первых двух примерах композиции получаются по следующей общей методике. Органическая фаза добавляется к водной фазе, и эмульсия масло в воде образуется с помощью высокосдвигового смесителя. Средний размер частиц находится в пределах (11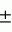 2) мкм. При поддержании слабого перемешивания температура загрузки повышается до 50oC в течение 30 мин и поддерживается при 50oC в течение 3 ч. Полученная суспензия микрокапсулы охлаждается до комнатной температуры. Затем добавляются дополнительные ингредиенты и pH регулируется до 11 с помощью 50% каустиком. В третьем примере pH водной фазы корректируется до 2. Затем органическая фаза добавляется к водной фазе, и с помощью высокосдвигового смесителя образуется эмульсия масло в воде. Средний размер частиц находится в пределах 28 2) мкм. При поддержании слабого перемешивания температура загрузки повышается до 50oC в течение 30 мин и поддерживается при 50oC в течение 3 ч. Полученная суспензия микрокапсулы охлаждается до комнатной температуры. Затем добавляются дополнительные ингредиенты и pH регулируется до 11 с помощью 50% каустиком. В третьем примере pH водной фазы корректируется до 2. Затем органическая фаза добавляется к водной фазе, и с помощью высокосдвигового смесителя образуется эмульсия масло в воде. Средний размер частиц находится в пределах 28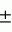 3 мкм. При поддержании слабого перемешивания температура загрузки повышается до 50oC в течение 30 мин и выдерживается при 50oC в течение 3 ч. Полученная суспензия микрокапсулы затем охлаждается до комнатной температуры. Затем вводятся дополнительные ингредиенты и pH корректируется до 7 с помощью 50% каустика. Пример I. 14473-27-1 Композиция получается с использованием описанной выше общей методики с ингредиентами, представленными в табл. 1. Пример II. 14585-26. Композиция получается с использованием описанной выше общей методики с ингредиентами, представленными в табл. 2. Готовый микрокапсулированный продукт имел средний диаметр частиц 12,5 мкм ( см. табл. 2). В каждом примере конечный продукт способа был исследован с помощью микроскопии и полярографии. Результаты показали, что суспензия биологически активного твердого вещества была успешно микрокапсулирована, и водная фаза была фактически свободна от твердого вещества. 3 мкм. При поддержании слабого перемешивания температура загрузки повышается до 50oC в течение 30 мин и выдерживается при 50oC в течение 3 ч. Полученная суспензия микрокапсулы затем охлаждается до комнатной температуры. Затем вводятся дополнительные ингредиенты и pH корректируется до 7 с помощью 50% каустика. Пример I. 14473-27-1 Композиция получается с использованием описанной выше общей методики с ингредиентами, представленными в табл. 1. Пример II. 14585-26. Композиция получается с использованием описанной выше общей методики с ингредиентами, представленными в табл. 2. Готовый микрокапсулированный продукт имел средний диаметр частиц 12,5 мкм ( см. табл. 2). В каждом примере конечный продукт способа был исследован с помощью микроскопии и полярографии. Результаты показали, что суспензия биологически активного твердого вещества была успешно микрокапсулирована, и водная фаза была фактически свободна от твердого вещества.
ФОРМУЛА ИЗОБРЕТЕНИЯ1. Микрокапсула, полученная реакцией полимеризации на границе раздела фаз, включающая твердый агрохимический материал, суспендированный в водонесмешивающейся органической жидкости и от 0,01 до около 10 мас.% в расчете на вес микрокапсулы и ее содержимого неионного диспергатора, активного только на границе раздела твердое вещество/органическая жидкость, не действующего как эмульгатор, включающего полимерную цепь, имеющую сильное сродство с органической жидкостью, и группу, сильно абсорбируемую твердым агрохимическим агентом. 2. Микрокапсула по п.1, отличающаяся тем, что содержит гербицид. 3. Микрокапсула по п.2, отличающаяся тем, что в качестве гербицида содержит атразин. 4. Микрокапсула по п.1, отличающаяся тем, что в качестве органической жидкости содержит жидкий гербицид. 5. Микрокапсула по п.4, отличающаяся тем, что в качестве жидкого гербицида содержит галогенацетанилидный или тиокарбаматный гербицид. 6. Микрокапсула по п.5, отличающаяся тем, что в качестве жидкого гербицида содержит ацетохлор. 7. Микрокапсула по п. 6, отличающаяся тем, что дополнительно содержит антидот. 8. Микрокапсула по п.1, отличающаяся тем, что содержит от примерно 0,1 до примерно 55,0 мас.% агрохимического материала. 9. Микрокапсула по пп.1-7, отличающаяся тем, что получена полимеризацией смеси полиметиленполифенилизоцианата и изомерной смеси толуолдиизоцианатов. 10. Микрокапсула по п.1, отличающаяся тем, что получена из этерифицированного мочевиноформальдегидного форполимера, 50-98% метилольных групп которого этерифицировано C4-C10 - спиртом. 11. Микрокапсула по пп.8-10, отличающаяся тем, что содержание стенки составляет от примерно 4 до примерно 15 мас.% капсулы. 12. Способ получения микрокапсул, содержащих твердое агрохимическое вещество, суспендированное в водонесмешивающейся органической жидкости, включающий а) получение суспензии твердого агрохимического вещества в не смешивающейся с водой органической жидкости, которая содержит один или более форполимеров, которые могут реагировать с образованием полимера на границе раздела органической жидкости и воды, неионный диспергатор, активный только на границе раздела твердое вещество/органическая жидкость и не действующий как эмульгатор, состоящий из полимерной цепи, обладающей сильным сродством к органической жидкости, и группы, сильно абсорбируемой твердым агрохимическим веществом, и, возможно, антидот, i) получением порошка агрохимического вещества с размером частиц 0,01-50,0 мкм и суспендированием порошка в указанной органической жидкости, либо ii) суспендированием указанного агрохимического вещества в указанной органической жидкости и затем измельчением указанного вещества до частиц размером 0,01-50,0 мкм, в) введение полученной суспензии в водную фазу воды, содержащую защитный коллоид и поверхностно-активное вещество, способное поддерживать органическую жидкость в виде капелек в воде, без экстрагирования твердого вещества из органической жидкости в воду, с) перемешивание суспензии органической жидкости в водной фазе при высоком сдвиге с образованием эмульсии масло в воде и d) регулирование при необходимости температуры и/или pH эмульсии до образования микрокапсул. 13. Способ по п.12, отличающийся тем, что агрохимический агент измельчают до частиц размером 1-10 мкм. 14. Способ по п.12 или 13, отличающийся тем, что органическую жидкость диспергируют в воде до капелек размером 1-30 мкм. 15. Способ по пп.12 - 14, отличающийся тем, что в качестве защитного коллоида используют лигносульфонат щелочного или щелочноземельного металла и поливиниловый спирт. 16. Способ по пп.12 - 15, отличающийся тем, что в качестве ПАВ водной фазы используют ПАВ с ГЛБ 12-16. 17. Способ по пп.12 - 16, отличающийся тем, что в качестве форполимера используют смесь полиметиленполифенилизоцианата и изомерной смеси толуолдиизоцианатов. 18. Способ по пп.12 - 16, отличающийся тем, что в качестве форполимера используют мочевиноформальдегидный форполимер, в котором 50-90% метилольных групп этерифицировано C4-C10 - спиртом, образующий твердый полимер при pH 0-4 при 20-100oC.Популярные патенты: 2403703 Способ интенсификации роста растений ... от 3-х до 5-ти, распыляют активированную воду и поливают активированной водой. Способ позволяет упростить процесс активации воды, используемой для интенсификации роста растений с повышением урожайности, всхожести посевного материала и ускоренным выращиванием продукции. 3 табл. Изобретение относится к области биосинтеза и, прежде всего, к культивированию растений в сельском хозяйстве, цветоводстве, растениеводстве, точнее к водным обработкам растений активированной водой, приводящим к ускорению биосинтеза, в результате чего можно достигнуть повышения урожайности, увеличения всхожести посевов, сокращения сроков выращивания растений и других эффектов. Подобные обработки также ... 2056743 Установка для выращивания пушных зверей ... и зверосовхозах. В летний период времени, а в южных широтах почти круглый год, высокая температура окружающего воздуха является серьезным препятствием для выращивания в неволе ценных пушных зверей, таких как норка, соболь, куница и т. п. Это связано с тем, что от жары пушные звери болеют, страдают от насекомых-паразитов, теряют подшерсток, плохо едят, что приводит к невосполнимым потерям качества пушнины. Для повышения качества пушнины целесообразно круглогодично содержать зверей при низких температурах, используя для этого искусственный холод. Известна система охлаждения помещений для содержания животных. Система имеет несколько расставленных с промежутками синхронно вращающихся ... 2181542 Способ хранения эритроцитов в условиях охлаждения при отсутствии кислорода (варианты) ... промывания эритроцитов солевым раствором, содержащим глюкозу, перед их использованием для того, чтобы снизить в них концентрацию фосфата аммония. 8. Способ хранения эритроцитов, который включает стадии: а. получения массы уплотненных эритроцитов; б. смешивания уплотненных эритроцитов с консервирующим раствором, который включает глюкозу, аденин и соли, с формированием таким образом суспензии эритроцитов; в. снижения уровня кислорода эритроцитов в суспензии эритроцитов до примерно 8% от их уровня насыщения или ниже путем промывания эритроцитов инертным газом и г. охлаждения суспензии эритроцитов до 4oС. 9. Способ хранения эритроцитов по п. 8, где указанная стадия снижения уровня ... 2267924 Способ стимулирования роста растений ... задача снижения количества используемого стимулятора роста при сохранении его эффективности приобретает особую актуальность. В качестве стимуляторов роста в сельском хозяйстве используют как индивидуальные соединения, так и композиции, содержащие в своем составе ростостимулирующие вещества.Из уровня техники известно применение в качестве стимуляторов роста некоторых предельных дикарбоновых кислот в виде водных растворов или в составе водо-растворимых композиций.Известна композиция для повышения устойчивости растений к болезням путем обработки семян и вегетирующих растений на основе водных растворов хитозана, в которой в качестве регуляторов роста растений содержатся ... 2106082 Устройство для укладки подстилочного навоза в бурт ... скреперным полотном с приводом от спаренных силовых винтов, установленных по бортам наклонной плоскости и имеющих одновременно правую и левую прямоугольную резьбу, при этом передняя стенка камеры выполнена виде плиты, установленной с возможностью перемещения посредством отталкивающего устройства, состоящего из четырех параллельно работающих винтов с приводом от мотор-редуктора или ручной рукояти, а передние колеса устройства выполнены самоустанавливающимися. Навозный двор имеет твердое покрытие и предпочтительно должен иметь навес или кровлю. На фиг. 1 изображен буртоукладчик и присоединенная к нему транспортная тележка со скрепежным разгрузчиком. На фиг. 2 изображена укладка бурта ... |
Еще из этого раздела: 2399200 Устройство для обработки роговых образований животных, например крупного рогатого скота 2095957 Устройство для транспортирования подстилочного навоза 2015654 Теплица для подземной выработки 2040900 Фунгицидное средство 2060650 Дозатор концентрированных кормов 2403708 Устройство для полива сельхозрастений 2280351 Установка для скашивания сорной растительной массы с берм и откосов канала 2247490 Способ освоения закустаренных земель и устройство для его осуществления 2477044 Искусственная рыболовная приманка (варианты) 2048752 Дождевальная машина |
Изобретения в сельском хозяйстве
Обработка почвы в сельском и лесном хозяйствах
Посадка, посев, удобрение
Уборка урожая, жатва
Обработка и хранение продуктов полеводства и садоводства
Садоводство, разведение овощей, цветов, риса, фруктов, винограда, лесное хозяйство
Новые виды растений или способы их выращивания
Производство молочных продуктов
Животноводство, разведение и содержание птицы, рыбы, насекомых, рыбоводство, рыболовство
Поимка, отлов или отпугивание животных
Консервирование туш животных, или растений или их частей
Биоцидная, репеллентная, аттрактантная или регулирующая рост растений активность химических соединений или препаратов
Хлебопекарные печи, машины и прочее оборудование для хлебопечения
Машины или оборудование для приготовления или обработки теста
Обработка муки или теста для выпечки, способы выпечки, мучные изделия
|
|
||