Способ защиты растений от грибковой инфекции (варианты)Патент на изобретение №: 2141760 Автор: Кохен Йигал (IL) Патентообладатель: Агроджин, Лтд. (IL) Дата публикации: 27 Ноября, 1999 Начало действия патента: 9 Декабря, 1994 Адрес для переписки: 113054, Россия, Москва, Большой Строченовский пер., 22/25, Фирма "Бейкер и Макензи", Ариевичу Е.А. Изображения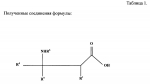    Описывается способ защиты растений от грибковых болезней, вызванных патогенными грибами путем индуцирования системной устойчивости указанной культуры, отличающийся тем, что на указанную культуру или место ее произрастания наносят состав, содержащий эффективное количество соединения формулы I 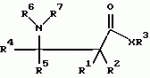 где а) R1 и R2 каждый независимо означает водород; (b) R3 означает водород, С1-С23-алкил; (с) R4 означает С1-C8-алкил, a R5 означает водород; (d) R6 и R7 каждый независимо означает водород, бензоил, фенил-С1-С4-алкил, где фенильный остаток означает незамещенный фенил; (е) Х означает O, и его соли, и культуру выбирают из группы зерновых, огурцов, арбуза, спаржевой капусты, цветной капусты, капусты кольраби, подсолнечника, картофеля, табака, винограда, кукурузы, риса, в количестве, достаточном для индуцирования механизма локального и системного иммунитета указанного культурного растения для подавления грибковой болезни. Технический результат - повышение эффективности способа защиты растений от грибковой инфекции. 4 с. и 33 з.п.ф-лы, 24 табл.
, , , , , , , , , , , , , , , , , , , , , , , где а) R1 и R2 каждый независимо означает водород; (b) R3 означает водород, С1-С23-алкил; (с) R4 означает С1-C8-алкил, a R5 означает водород; (d) R6 и R7 каждый независимо означает водород, бензоил, фенил-С1-С4-алкил, где фенильный остаток означает незамещенный фенил; (е) Х означает O, и его соли, и культуру выбирают из группы зерновых, огурцов, арбуза, спаржевой капусты, цветной капусты, капусты кольраби, подсолнечника, картофеля, табака, винограда, кукурузы, риса, в количестве, достаточном для индуцирования механизма локального и системного иммунитета указанного культурного растения для подавления грибковой болезни. Технический результат - повышение эффективности способа защиты растений от грибковой инфекции. 4 с. и 33 з.п.ф-лы, 24 табл.
, , , , , , , , , , , , , , , , , , , , , , , ОПИСАНИЕ ИЗОБРЕТЕНИЯ К ПАТЕНТУИзобретение относится к новому способу защиты растений от поражения патогенными микроорганизмами. Более конкретно, настоящее изобретение относится к способу нанесения выбранных соединений и составов на сельскохозяйственную культуру или место ее произрастания для индуцирования местной и системной устойчивости культурного растения к грибковым болезням, где этот эффект в настоящей заявке упоминается как "индуцированная фитозащита" (упоминаемая далее в описании ИФЗ). ИФЗ у культурного растения проявляется через различные защитные механизмы, включая накопление в указанной культуре растворимых белков, называемых патогенными белками (PR-белки). Установлено, что некоторые из таких патогенных белков относятся к гидролазам, например как хитиназы и В-1, 3-глюконазы, в то время как другие относятся к пероксидазам. Кроме того, в культурном растении происходит накопление группы из указанных белков с молекулярной массой от примерно 10 до 20 кДа, называемых Р14-белками, у которых отсутствует известная биологическая функция. Каждый из указанных белков, как полагают, участвует в системе защиты культуры. Из патентной литературы известно использование различных изоникотиноил-пиридинилгидразиновых производных и бензотиадиазолов в качестве иммунизирующих агентов здоровых растений против грибковых болезней (заявки на Европатент N0268775, 0288976 и 0313512). Известно также использование DL-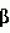 -аминомасляной кислоты для борьбы с корневой гнилью гороха, вызванной Aphanomyces euteiches Drechs. (Papavizas, Plant Disease Reporter, Vol. 48, N. 7, pp. 537-541 (1964), Papavizas, Plant Disease Reporter, Vol. 51, N. 2, pp. 125-129 (1967)). Известно использование 0,03 М раствора DL- -аминомасляной кислоты для борьбы с корневой гнилью гороха, вызванной Aphanomyces euteiches Drechs. (Papavizas, Plant Disease Reporter, Vol. 48, N. 7, pp. 537-541 (1964), Papavizas, Plant Disease Reporter, Vol. 51, N. 2, pp. 125-129 (1967)). Известно использование 0,03 М раствора DL-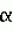 -aминoмacлянoй кислоты для борьбы с паршой яблок, вызванной Venturia inaequalis (Кис и др., 1959, Phytopathology, 49, с.313- 315). Известно использование of DL- -aминoмacлянoй кислоты для борьбы с паршой яблок, вызванной Venturia inaequalis (Кис и др., 1959, Phytopathology, 49, с.313- 315). Известно использование of DL-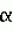 -аминомасляной кислоты и DL- -аминомасляной кислоты и DL-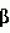 -аминомасляной кислоты в качестве химических лечебных средств против антракноза плодов огурцов, вызванных Colletotrium cucumerium и Colletotrium lagenarium и фитофторозной гнили плодов томата, вызванных Phytophthora (Oort, A.J.P и Van Andel, O.M., 1960, Mededel, Landbouwhogeschool Opzoekingssta, Staat Gent, 25:981-992). В патентной литературе описано использование различных производных DL- -аминомасляной кислоты в качестве химических лечебных средств против антракноза плодов огурцов, вызванных Colletotrium cucumerium и Colletotrium lagenarium и фитофторозной гнили плодов томата, вызванных Phytophthora (Oort, A.J.P и Van Andel, O.M., 1960, Mededel, Landbouwhogeschool Opzoekingssta, Staat Gent, 25:981-992). В патентной литературе описано использование различных производных DL-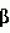 -аминомасляной кислоты и - -аминомасляной кислоты и -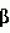 -аминокротоновой кислоты в качестве фунгицидов против фитофторозной гнили плодов томата, вызванных Phytophthora и гнили плодов винограда, вызванных Plasmopara viticola (DE-PS 1120802). Cohen, Niderman, Mosinger и Fluhr недавно сообщили в печати (Plant physiol. (1994), вып.104, стр.58-66) о том, что связанные с патогенезом белки участвуют в механизме ИФЗ томатов. Целью настоящего изобретения является создание нового метода, обеспечивающего ИФЗ. Другой целью предлагаемого изобретения является создание нового метода, обеспечивающего ИФЗ выбранных растений. Предлагается новый метод защиты сельскохозяйственной культуры против грибковых болезней, вызванных болезнетворными грибами, который, согласно изобретению, заключается в том, что на культуру или место его произрастания наносят состав, содержащий эффективное количество соединения формулы I -аминокротоновой кислоты в качестве фунгицидов против фитофторозной гнили плодов томата, вызванных Phytophthora и гнили плодов винограда, вызванных Plasmopara viticola (DE-PS 1120802). Cohen, Niderman, Mosinger и Fluhr недавно сообщили в печати (Plant physiol. (1994), вып.104, стр.58-66) о том, что связанные с патогенезом белки участвуют в механизме ИФЗ томатов. Целью настоящего изобретения является создание нового метода, обеспечивающего ИФЗ. Другой целью предлагаемого изобретения является создание нового метода, обеспечивающего ИФЗ выбранных растений. Предлагается новый метод защиты сельскохозяйственной культуры против грибковых болезней, вызванных болезнетворными грибами, который, согласно изобретению, заключается в том, что на культуру или место его произрастания наносят состав, содержащий эффективное количество соединения формулы I 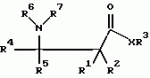 где (a) R1 и R2 каждый независимо означает водород; (b) R3 означает водород, C1-C23-алкил; (с) R4 означает C1-C8-алкил, a R5 означает водород; (d) R6 и R7 каждый независимо означает водород, бензоил, фенил-C1-C4-алкил, где фенильный остаток означает незамещенный фенил; (e) X означает O и его соли, и культуру выбирают из группы зерновых, огурцов, арбуза, спаржевой капусты, цветной капусты, капусты кольраби, подсолнечника, картофеля, табака, винограда, кукурузы, риса, в количестве, достаточном для индуцирования механизма локального и системного иммунитета указанного культурного растения для подавления грибковой болезни. Алкил, используемый в данном описании, означает алкил с неразветвленной или разветвленной углеродной цепью или циклические его формы, содержащий предпочтительно от 1 до 4 атомов углерода. R1 и R2 каждый независимо означает водород, предпочтительно R3 означает водород, R4 означает C1-C3-алкил, R5 означает водород, R6 и R7 каждый независимо означает водород, и X означает кислород или предпочтительно, R1 и R2 означают водород, R4 означает метил, R5 означает водород, R6 означает водород или метил и R7 означает водород. К предпочтительным соединениям предлагаемого изобретения относятся аминомасляные, и наиболее предпочтительны аминомасляные кислоты (Схема I) и, особенно предпочтительна R- где (a) R1 и R2 каждый независимо означает водород; (b) R3 означает водород, C1-C23-алкил; (с) R4 означает C1-C8-алкил, a R5 означает водород; (d) R6 и R7 каждый независимо означает водород, бензоил, фенил-C1-C4-алкил, где фенильный остаток означает незамещенный фенил; (e) X означает O и его соли, и культуру выбирают из группы зерновых, огурцов, арбуза, спаржевой капусты, цветной капусты, капусты кольраби, подсолнечника, картофеля, табака, винограда, кукурузы, риса, в количестве, достаточном для индуцирования механизма локального и системного иммунитета указанного культурного растения для подавления грибковой болезни. Алкил, используемый в данном описании, означает алкил с неразветвленной или разветвленной углеродной цепью или циклические его формы, содержащий предпочтительно от 1 до 4 атомов углерода. R1 и R2 каждый независимо означает водород, предпочтительно R3 означает водород, R4 означает C1-C3-алкил, R5 означает водород, R6 и R7 каждый независимо означает водород, и X означает кислород или предпочтительно, R1 и R2 означают водород, R4 означает метил, R5 означает водород, R6 означает водород или метил и R7 означает водород. К предпочтительным соединениям предлагаемого изобретения относятся аминомасляные, и наиболее предпочтительны аминомасляные кислоты (Схема I) и, особенно предпочтительна R-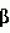 -аминомасляная кислота. Схема 1 -аминомасляная кислота. Схема 1   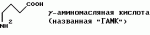 Согласно изобретению, предпочтительными соединениями также являются: N-бензоил-3-аминомасляной кислоты 1-метил-1-бутиловый эфир; N-бензоил-3-аминомасляной кислоты 1-метил-5-пентиловый эфир; N-бензоил-3-аминомасляной кислоты н-гептиловый эфир; N-бензоил-3-аминомасляной кислоты н-гексиловый эфир; N-бензоил-3-аминомасляной кислоты 1-метил-1-гептиловый эфир; N-бензоил-3-аминомасляной кислоты 1-метил-1-гексиловый эфир; N-бензоил-3-аминомасляной кислоты 1-метил-1-октиловый эфир; N-бензоил-3-аминомасляной кислоты 1-метил-1-пентиловый эфир; N-2-фенилэтил-3-аминомасляной кислоты н-октиловый эфир; N-2-фенилэтил-3-аминомасляной кислоты 1-метил-1-пентиловый эфир; и натриевая соль 3-аминомасляной кислоты. В объем солей любого соединения формулы (I), предлагаемых в данной заявке входят соли присоединения кислот, например полученные реакцией присоединения HCl, CF3, CO2H, толуолсульфокислоты, метансульфокислоты и (CO2H)2, Согласно изобретению, предпочтительными соединениями также являются: N-бензоил-3-аминомасляной кислоты 1-метил-1-бутиловый эфир; N-бензоил-3-аминомасляной кислоты 1-метил-5-пентиловый эфир; N-бензоил-3-аминомасляной кислоты н-гептиловый эфир; N-бензоил-3-аминомасляной кислоты н-гексиловый эфир; N-бензоил-3-аминомасляной кислоты 1-метил-1-гептиловый эфир; N-бензоил-3-аминомасляной кислоты 1-метил-1-гексиловый эфир; N-бензоил-3-аминомасляной кислоты 1-метил-1-октиловый эфир; N-бензоил-3-аминомасляной кислоты 1-метил-1-пентиловый эфир; N-2-фенилэтил-3-аминомасляной кислоты н-октиловый эфир; N-2-фенилэтил-3-аминомасляной кислоты 1-метил-1-пентиловый эфир; и натриевая соль 3-аминомасляной кислоты. В объем солей любого соединения формулы (I), предлагаемых в данной заявке входят соли присоединения кислот, например полученные реакцией присоединения HCl, CF3, CO2H, толуолсульфокислоты, метансульфокислоты и (CO2H)2, 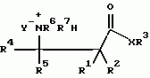 где Y означает остаток кислоты; а соли щелочных металлов, например, полученные путем обработки NaOH, КОН или LiOH, где Y означает остаток кислоты; а соли щелочных металлов, например, полученные путем обработки NaOH, КОН или LiOH, 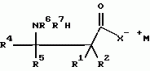 где M означает щелочной металл, например Na, K или Li; и соли амина/присоединения кислоты, например, которые получены путем обработки HCl и амином, например диэтиламин, пропиламин, бензиламин. где M означает щелочной металл, например Na, K или Li; и соли амина/присоединения кислоты, например, которые получены путем обработки HCl и амином, например диэтиламин, пропиламин, бензиламин. 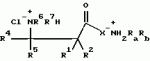 где Ra и Rb означают заместители. К предпочтительным сельскохозяйственным культурам, где может найти применение метод предлагаемого изобретения, относятся такие культурные растения как огурцы, арбуз, спаржевая капуста, цветная капуста, кольраби, картофель, подсолнечник, табак, виноград, кукуруза, рис. К наиболее предпочтительным культурам относятся подсолнечник, виноград, огурцы, арбуз, спаржевая капуста, кольраби, цветная капуста, картофель, табак и кукуруза. Метод предлагаемого изобретения отличается от прототипа, особенно в части механизма действия на томаты. Причина заключается в том, что механизм индуцированной фитозащиты у томатов, о котором сообщалось, осуществляется через образование связанных с патогенезом белков (PR-белков). Установлено (Y.Cohen, неопубликованные результаты), что механизм их индуцированной фитозащиты иной, чем у других растений. Так, например, было установлено, что указанный механизм, например, у огурцов и арбуза осуществляется через накопление калозы и лигнина в инфицированных клетках без участия в процессе каких-либо PR-белков. Кроме того, подтверждено документально [Y. Cohen, Physiological и Molecular Plant Pathology (1994), 44:273-288], что механизм защиты против грибковых инфекций у табака не связан с накоплением ни PR-белка, калозы или лигнина. Более того, предлагаемый метод эффективен против патогенных грибов с уже приобретенной устойчивостью к большинству имеющихся в продаже химических фунгицидов. И наконец, предлагаемый метод, как установлено, эффективен даже после инфицирования растений и, таким образом, он обеспечивает индуцированную защиту растений с лечебным эффектом. Новые соединения, предлагаемые в объеме настоящей заявки, относятся с точки зрения их структуры к известным соединениям и их можно легко получить либо из известных соединений, либо необходимой модификацией способов получения известного соединения. Эти способы получения будут ясны специалистам в данной области техники. Ниже приводятся примеры, иллюстрирующие способы получения соединений предлагаемого изобретения. Соединения формулы Ia, где Ra и Rb означают заместители. К предпочтительным сельскохозяйственным культурам, где может найти применение метод предлагаемого изобретения, относятся такие культурные растения как огурцы, арбуз, спаржевая капуста, цветная капуста, кольраби, картофель, подсолнечник, табак, виноград, кукуруза, рис. К наиболее предпочтительным культурам относятся подсолнечник, виноград, огурцы, арбуз, спаржевая капуста, кольраби, цветная капуста, картофель, табак и кукуруза. Метод предлагаемого изобретения отличается от прототипа, особенно в части механизма действия на томаты. Причина заключается в том, что механизм индуцированной фитозащиты у томатов, о котором сообщалось, осуществляется через образование связанных с патогенезом белков (PR-белков). Установлено (Y.Cohen, неопубликованные результаты), что механизм их индуцированной фитозащиты иной, чем у других растений. Так, например, было установлено, что указанный механизм, например, у огурцов и арбуза осуществляется через накопление калозы и лигнина в инфицированных клетках без участия в процессе каких-либо PR-белков. Кроме того, подтверждено документально [Y. Cohen, Physiological и Molecular Plant Pathology (1994), 44:273-288], что механизм защиты против грибковых инфекций у табака не связан с накоплением ни PR-белка, калозы или лигнина. Более того, предлагаемый метод эффективен против патогенных грибов с уже приобретенной устойчивостью к большинству имеющихся в продаже химических фунгицидов. И наконец, предлагаемый метод, как установлено, эффективен даже после инфицирования растений и, таким образом, он обеспечивает индуцированную защиту растений с лечебным эффектом. Новые соединения, предлагаемые в объеме настоящей заявки, относятся с точки зрения их структуры к известным соединениям и их можно легко получить либо из известных соединений, либо необходимой модификацией способов получения известного соединения. Эти способы получения будут ясны специалистам в данной области техники. Ниже приводятся примеры, иллюстрирующие способы получения соединений предлагаемого изобретения. Соединения формулы Ia, 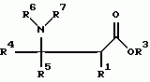 где R1 и R4-R7 имеют вышеуказанные значения, a R3 означает водород или C1-C8 алкил, можно получить из соединения IIa где R1 и R4-R7 имеют вышеуказанные значения, a R3 означает водород или C1-C8 алкил, можно получить из соединения IIa 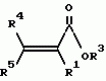 Для получения соединений формулы (Ia), где R6 означает H, a R7 имеет вышеуказанные значения, осуществляют взаимодействие соединения формулы (IIa) с NR7H2, где R7 имеет вышеуказанные значения. Реакции такого типа описаны в литературе, см., например, A.Zilkha и J.Rivlin, Joс 1957, 23, 94. Для получения соединений формулы (Ia), где R6 и R7 имеют вышеуказанные значения, кроме водорода, осуществляют взаимодействие соединения формулы (IIa) с NH6R7Li, где R6 и R7 имеют вышеуказанные значения, кроме водорода. Реакции такого типа описаны в литературе, см.например, Davies и др. Tetrahedron: Asymmetry, том. 2, N.3, стр. 183-186 (1991). Соединения формулы (IIa) либо относятся к известным соединениям, либо их можно получить из известных соединений в соответствии с традиционными методами. Как можно легко понять, в том случае, где R4 и R5 не означают один и тот же заместитель, атом углерода, с которым они связаны является хиральным. Способы получения каждой энантиомерной формы как описаны в литературе, см., например, заявку на ЕР 0144980 или Davies, выше, можно получить аналогичными методами. Предлагаемый метод защиты растений, как установлено, эффективен против множества различных болезней. В качестве примера можно привести фитофтороз пасленовых, ложную мучнистую росу, пероноспороз табака, пятнистость листьев, фузариозный вилт, рак ствола, бурую гниль плодов, "черную ножку", белую ржавчину, черную гниль корневой шейки и фитофторозную гниль корней. Соединения настоящего изобретения наносят обычно на сельскохозяйственные культуры или место их произрастания до или после их заболевания, или соединения можно наносить на поверхность листвы защищаемой культуры после проявления первоначальных признаков грибкового поражения. Количество активного вещества, используемого в составе, должно быть достаточным для индуцирования устойчивости культуры к патогенным грибам и обычно меняется в зависимости от таких факторов как вид грибов, типа обработки (например, распыление, опудривание, протравливание семян, орошение почвы), состояния культуры, и индивидуальных особенностей используемого активного вещества. Что касается обработки культуры или место его произрастания, то соединения предлагаемого изобретения обычно наносят на посев культур при норме расхода от 0,1 до 5 кг/га, предпочтительно от 0,2 до 2 кг/га, причем при необходимости обработку повторяют, обычно с промежутком от одной до трех недель. В зависимости от обстоятельств, соединения настоящего изобретения можно использовать в комбинации с другими пестицидами, например фунгицидами, инсектицидами, акарицидами, гербицидами, или регуляторами роста растений для усиления их активности или расширения спектра их действия. Соединения настоящего изобретения подходят для нанесения в виде фунгицидных составов в комбинации с сельскохозяйственно пригодными носителями или наполнителями. Указанные составы также входят в объем настоящего изобретения. Они могут содержать, помимо любого соединения формулы (I) в качестве активного ингредиента, другие активные вещества, например фунгициды. Указанные составы можно использовать как в твердых, так и жидких формах, например, в виде смачивающегося порошка, концентрата эмульсии, концентрата диспергируемой в воде суспензии ("текучей"), присыпки, гранулята, препарата с замедленным высвобождением активного вещества, содержащего традиционные носители, наполнители, и/или адъюванты. Такие составы можно приготовить традиционным способом, например путем смешивания активного вещества с носителем и другими ингредиентами композиции. Типичные составы, наносимые путем распыления, например диспергируемые в воде концентраты или смачивающиеся порошки, могут содержать поверхностно-активные вещества, например смачивающие агенты и диспергаторы, например продукт реакции конденсации формальдегида с нафталинсульфонатом, алкиларилсульфонатом, лигнинсульфонатом, алкилсульфатом жирных кислот, этоксилированным алкилфенолом и этоксилированным спиртом жирного ряда. Обычно составы содержат от 0,01 до 90 мас.% активного ингредиента, при этом указанный активный ингредиент состоит из либо по меньшей мере одного соединения формулы (I), либо из смеси его с другими активными веществами, например фунгицидами. Составы в форме концентратов обычно содержат от примерно 2 до 80%, предпочтительно от примерно 5 до 70 мас.% активного ингредиента. Составы, используемые для нанесения, могут, например, содержать от 0,01 до 20 мас.%, предпочтительно от 0,01 до 5 мас.% активного ингредиента. Пример состава I. Смачивающийся порошок. 50 мас. частей соединения формулы (I) размалывают с 2 частями лаурилсульфата, 3 частями лигнинсульфоната натрия и 45 частями тонкодисперсного каолинита до получения среднего размера частиц менее 5 микрон. Полученный смачивающийся порошок разбавляют водой перед его использованием до концентрации активного ингредиента от 0,01 до 5%. Полученную жидкость для распыления можно наносить путем опрыскивания листвы, а также пропитыванием жидкого препарата зоны расположения корней. Пример состава II. Концентрат эмульсии. 25 мас. частей соединения формулы I, 65 частей ксилола, 10 частей продукта взаимодействия смеси из алкилфенола с окисью ксилола и додецилбензолсульфонатом кальция тщательно перемешивают до получения гомогенного раствора. Полученный концентрат эмульсии разводят водой перед использованием. Пример состава III. Гранулированный препарат (для почвенной обработки). На 94,5 мас.частей кварцевого песка, помещенного в барабанный смеситель, распыляют 0,5 мас.частей связующего (неионогенного) и полученную смесь тщательно перемешивают. После этого к полученной смеси прибавляют в порошкообразном виде 5 мас.частей соединения формулы (I) и после тщательного перемешивания получают гранулированный препарат, имеющий размер частиц от примерно 0,3 до примерно 0,7 мм. Полученный гранулят можно наносить путем внесения его в почву вблизи зоны испытуемых растений. Пример состава IV. Протравливание семян или клубней. 25 мас. частей соединения формулы (I), 15 частей диалкил-феноксиполиэтиленоксиэтанола, 15 частей мелкозернистого кремнезема, 44 части каолина, 0,5 части, например, кристаллического фиолетового и 0,5 части ксантамовой смолы смешивают и размельчают в струйной мельнице при скорости примерно 10000 об/мин до получения среднего размера частиц менее 20 микрон. Полученный состав в виде водной суспензии распыляют на семена или клубни с использованием любого аппарата, пригодного для этой цели. В случае, когда соединение формулы (I) получают в жидкой форме, то его сначала адсорбируют на носители, используя, при желании, небольшое количество летучего растворителя, например ацетона. В случае, когда используют растворитель, то полученный порошок вначале сушат, затем к нему прибавляют другие ингредиенты и выполняют оставшиеся операции указанного метода. Пример состава V. Капельное орошение почвы. 2 мас.части соединения формулы (I) растворяют в 1000 частях воды. Полученный состав наносят на растения методом капельного орошения. Как указывалось ранее, соединения формулы (I) обладают способностью активизировать или усиливать систему защиты культурного растения против грибковых болезней, вызванных патогенными грибами. Такую активность предлагаемых соединений можно продемонстрировать нижеследующими испытаниями при использовании общей методики их проведения. Испытание A. Индуцированная фитозащита растений картофеля против Phytophthora. Посадочный материал картофеля (сорт Bintje) выращивают из клубней в горшках, заполненных почвенной смесью из легкого суглинка, торфа и перлита, взятых в равных объемах, в теплице (20-22oC). Растения готовы для проведения испытания при наличии у них 6 или 7 сложных листьев. Испытания проводят при использовании металаксил-устойчивых изолированных штаммов MR1 грибов Phytophtora, а также изолятов MS2, MS3, MR2 и MR3 (Kadish и Cohen, Phytopathology, 78: 912-9155 (1988). Спорангий указанного гриба выращивают на пластинах картофельного клубня при температуре 15oC в темноте. Спорангиевый урожай собирают на 6 день после инокуляции пластинок в двукратнодистиллированную воду (4oC), и их концентрацию доводят до 104 спорангиоспор/мл перед использованием их для контрольного заражения. Соединения предлагаемого изобретения растворяют в воде и полученный раствор разбрызгивают как на наружную, так и внутренную поверхности листьев картофеля методом мелкокапельного опрыскивания (примерно 10 мл на растение). Растения оставляют на тепличном стеллаже до полного высыхания капелек распыленного раствора и затем помещают в ростовую камеру, установленную на режим температуры 20oC и 14 световых часов на 10 дней. Контрольное заражение патогенами Phytophthora infestans проводят с интервалом от 30 минут до 12 дней после обработки предлагаемыми соединениями путем опрыскивания спорангиевой суспензией наружных поверхностей листьев (примерно 15 мл на растение). В одном эксперименте капли инокулята (10 капель, содержащих примерно 100 спорангиоспор) помешают на поверхность листьев, по две капли на листочек, и по одной на каждую сторону главной жилки. В другом эксперименте соединения наносят с лечебной целью через 24 часа после инокуляции P.infestans. Инокулированные растения выдерживают в условиях 100% относительной влажности в темноте в течение 24 часов при 20-18oC, и затем возвращают в ростовую камеру, где поддерживается температура 20oC и 12-часовой световой день. Степень тяжести болезни определяют через 4-8 дней после инокуляции растений визуальной оценкой доли или площади листа, пораженного фитофторозом. Испытание B. Индуцированная фитозащита рассады табака против Peronospora tabacina. Рассаду табака (сорт Ку-14 или Ку-16) выращивают из семян в горшках в теплице. Когда у проростков появятся 10 листочков или более, раствор предлагаемых соединений впрыскивают в стебель растения. В 1-3 день перед впрыскиванием или в 1-10 день после впрыскивания соединений осуществляют контрольное заражение растений конидиями грибов Peronospora tabacina Adam, которые являются возбудителями пероноспороза табака. Урожай конидии собирают с ранее инфицированных растений табака. Инокуляцию осуществляют раствором, содержащим 104-105 конидий/мл, используя примерно 50 мл на растение. В данном испытании можно также использовать вышеописанную методику инокуляции, поддержания культуры, оценки степени поражения растения. Хотя настоящее изобретение будет описано на некоторых предпочтительных примерах его осуществления, ясно, что изобретение не ограничивается этими конкретными вариантами его осуществления. Наоборот, изобретение подразумевает внесение всех возможных вариантов, изменений и эквивалентных решений в пределах существа и объема изобретения, определенных в нижеследующей формуле изобретения. Таким образом, нижеследующие примеры, включающие предпочтительные варианты осуществления изобретения, служат для его иллюстрации. Следует понимать, что детали показаны через пример и только для иллюстративных целей предпочтительных вариантов осуществления изобретения и представлены для того, чтобы дать представление о том, что, как полагают, является наиболее полезным и легко понятным в описании методов, а также принципов и концептуальных аспектов изобретения. Пример 1. N-(2-гидроксиэтил)-аминомасляная кислота. Раствор, содержащий 86 г кротоновой кислоты (1 моль) и этаноламина (1 моль) в пиридине (200 мл) кипятят с обратным холодильником в течение 2-3 часов и затем охлаждают. Полученный продукт фильтруют и после перекристаллизации получают названное соединение с т.пл. 178-180oC (соединение 1.1, табл. 1). По аналогичной методике получают соединения 1.2-1.7, 1.10, 1.11 и 1.13-1.15, приведенные в табл. 1. Пример 2. 3-Аминокапроновая кислота. Смесь 2-гексиновой кислоты (7,0 г, 0,06 моль) и концентрированного водного раствора гидроокиси аммония (70 мл) кипятят в течение 24 часов в автоклаве при температуре 150oC. Охлажденную смесь обрабатывают углеродной сажей и фильтруют. После упаривания растворителя неочищенный продукт перекристаллизовывают из этанола, и получают названное соединение, т.пл. 203oC (соединение 1.21, табл. 1). По аналогичной методике получают соединения 1.8, 1.9, 1.12-1.20, приведенные в табл. 1. Пример 3. N-бензоил-3-аминомасляная кислота. К охлажденному раствору 3-аминомасляной кислоты (13 г) в 2М NaOH (130 мл) прибавляют хлористый бензоил (19,7 г) в течение 2 часов. Смеси дают нагреться до комнатной температуры. После промывания диэтиловым эфиром, подкисления водной фазы 20% HCl, экстрагирования диэтиловым эфиром, сушки на MgSO4, отгонки растворителя и перекристаллизации остатка в смеси диэтиловый эфир/гексан получают названное соединение, т.пл. 150-152oC (соединение 1.16, табл. 1). По аналогичной методике получают соединение 1.17, приведенное в табл. 1. Пример 4. N-бензилоксикарбонил-3-аминомасляной кислоты (4-хлорфенил)-1-этиламид. Z-защищенную Для получения соединений формулы (Ia), где R6 означает H, a R7 имеет вышеуказанные значения, осуществляют взаимодействие соединения формулы (IIa) с NR7H2, где R7 имеет вышеуказанные значения. Реакции такого типа описаны в литературе, см., например, A.Zilkha и J.Rivlin, Joс 1957, 23, 94. Для получения соединений формулы (Ia), где R6 и R7 имеют вышеуказанные значения, кроме водорода, осуществляют взаимодействие соединения формулы (IIa) с NH6R7Li, где R6 и R7 имеют вышеуказанные значения, кроме водорода. Реакции такого типа описаны в литературе, см.например, Davies и др. Tetrahedron: Asymmetry, том. 2, N.3, стр. 183-186 (1991). Соединения формулы (IIa) либо относятся к известным соединениям, либо их можно получить из известных соединений в соответствии с традиционными методами. Как можно легко понять, в том случае, где R4 и R5 не означают один и тот же заместитель, атом углерода, с которым они связаны является хиральным. Способы получения каждой энантиомерной формы как описаны в литературе, см., например, заявку на ЕР 0144980 или Davies, выше, можно получить аналогичными методами. Предлагаемый метод защиты растений, как установлено, эффективен против множества различных болезней. В качестве примера можно привести фитофтороз пасленовых, ложную мучнистую росу, пероноспороз табака, пятнистость листьев, фузариозный вилт, рак ствола, бурую гниль плодов, "черную ножку", белую ржавчину, черную гниль корневой шейки и фитофторозную гниль корней. Соединения настоящего изобретения наносят обычно на сельскохозяйственные культуры или место их произрастания до или после их заболевания, или соединения можно наносить на поверхность листвы защищаемой культуры после проявления первоначальных признаков грибкового поражения. Количество активного вещества, используемого в составе, должно быть достаточным для индуцирования устойчивости культуры к патогенным грибам и обычно меняется в зависимости от таких факторов как вид грибов, типа обработки (например, распыление, опудривание, протравливание семян, орошение почвы), состояния культуры, и индивидуальных особенностей используемого активного вещества. Что касается обработки культуры или место его произрастания, то соединения предлагаемого изобретения обычно наносят на посев культур при норме расхода от 0,1 до 5 кг/га, предпочтительно от 0,2 до 2 кг/га, причем при необходимости обработку повторяют, обычно с промежутком от одной до трех недель. В зависимости от обстоятельств, соединения настоящего изобретения можно использовать в комбинации с другими пестицидами, например фунгицидами, инсектицидами, акарицидами, гербицидами, или регуляторами роста растений для усиления их активности или расширения спектра их действия. Соединения настоящего изобретения подходят для нанесения в виде фунгицидных составов в комбинации с сельскохозяйственно пригодными носителями или наполнителями. Указанные составы также входят в объем настоящего изобретения. Они могут содержать, помимо любого соединения формулы (I) в качестве активного ингредиента, другие активные вещества, например фунгициды. Указанные составы можно использовать как в твердых, так и жидких формах, например, в виде смачивающегося порошка, концентрата эмульсии, концентрата диспергируемой в воде суспензии ("текучей"), присыпки, гранулята, препарата с замедленным высвобождением активного вещества, содержащего традиционные носители, наполнители, и/или адъюванты. Такие составы можно приготовить традиционным способом, например путем смешивания активного вещества с носителем и другими ингредиентами композиции. Типичные составы, наносимые путем распыления, например диспергируемые в воде концентраты или смачивающиеся порошки, могут содержать поверхностно-активные вещества, например смачивающие агенты и диспергаторы, например продукт реакции конденсации формальдегида с нафталинсульфонатом, алкиларилсульфонатом, лигнинсульфонатом, алкилсульфатом жирных кислот, этоксилированным алкилфенолом и этоксилированным спиртом жирного ряда. Обычно составы содержат от 0,01 до 90 мас.% активного ингредиента, при этом указанный активный ингредиент состоит из либо по меньшей мере одного соединения формулы (I), либо из смеси его с другими активными веществами, например фунгицидами. Составы в форме концентратов обычно содержат от примерно 2 до 80%, предпочтительно от примерно 5 до 70 мас.% активного ингредиента. Составы, используемые для нанесения, могут, например, содержать от 0,01 до 20 мас.%, предпочтительно от 0,01 до 5 мас.% активного ингредиента. Пример состава I. Смачивающийся порошок. 50 мас. частей соединения формулы (I) размалывают с 2 частями лаурилсульфата, 3 частями лигнинсульфоната натрия и 45 частями тонкодисперсного каолинита до получения среднего размера частиц менее 5 микрон. Полученный смачивающийся порошок разбавляют водой перед его использованием до концентрации активного ингредиента от 0,01 до 5%. Полученную жидкость для распыления можно наносить путем опрыскивания листвы, а также пропитыванием жидкого препарата зоны расположения корней. Пример состава II. Концентрат эмульсии. 25 мас. частей соединения формулы I, 65 частей ксилола, 10 частей продукта взаимодействия смеси из алкилфенола с окисью ксилола и додецилбензолсульфонатом кальция тщательно перемешивают до получения гомогенного раствора. Полученный концентрат эмульсии разводят водой перед использованием. Пример состава III. Гранулированный препарат (для почвенной обработки). На 94,5 мас.частей кварцевого песка, помещенного в барабанный смеситель, распыляют 0,5 мас.частей связующего (неионогенного) и полученную смесь тщательно перемешивают. После этого к полученной смеси прибавляют в порошкообразном виде 5 мас.частей соединения формулы (I) и после тщательного перемешивания получают гранулированный препарат, имеющий размер частиц от примерно 0,3 до примерно 0,7 мм. Полученный гранулят можно наносить путем внесения его в почву вблизи зоны испытуемых растений. Пример состава IV. Протравливание семян или клубней. 25 мас. частей соединения формулы (I), 15 частей диалкил-феноксиполиэтиленоксиэтанола, 15 частей мелкозернистого кремнезема, 44 части каолина, 0,5 части, например, кристаллического фиолетового и 0,5 части ксантамовой смолы смешивают и размельчают в струйной мельнице при скорости примерно 10000 об/мин до получения среднего размера частиц менее 20 микрон. Полученный состав в виде водной суспензии распыляют на семена или клубни с использованием любого аппарата, пригодного для этой цели. В случае, когда соединение формулы (I) получают в жидкой форме, то его сначала адсорбируют на носители, используя, при желании, небольшое количество летучего растворителя, например ацетона. В случае, когда используют растворитель, то полученный порошок вначале сушат, затем к нему прибавляют другие ингредиенты и выполняют оставшиеся операции указанного метода. Пример состава V. Капельное орошение почвы. 2 мас.части соединения формулы (I) растворяют в 1000 частях воды. Полученный состав наносят на растения методом капельного орошения. Как указывалось ранее, соединения формулы (I) обладают способностью активизировать или усиливать систему защиты культурного растения против грибковых болезней, вызванных патогенными грибами. Такую активность предлагаемых соединений можно продемонстрировать нижеследующими испытаниями при использовании общей методики их проведения. Испытание A. Индуцированная фитозащита растений картофеля против Phytophthora. Посадочный материал картофеля (сорт Bintje) выращивают из клубней в горшках, заполненных почвенной смесью из легкого суглинка, торфа и перлита, взятых в равных объемах, в теплице (20-22oC). Растения готовы для проведения испытания при наличии у них 6 или 7 сложных листьев. Испытания проводят при использовании металаксил-устойчивых изолированных штаммов MR1 грибов Phytophtora, а также изолятов MS2, MS3, MR2 и MR3 (Kadish и Cohen, Phytopathology, 78: 912-9155 (1988). Спорангий указанного гриба выращивают на пластинах картофельного клубня при температуре 15oC в темноте. Спорангиевый урожай собирают на 6 день после инокуляции пластинок в двукратнодистиллированную воду (4oC), и их концентрацию доводят до 104 спорангиоспор/мл перед использованием их для контрольного заражения. Соединения предлагаемого изобретения растворяют в воде и полученный раствор разбрызгивают как на наружную, так и внутренную поверхности листьев картофеля методом мелкокапельного опрыскивания (примерно 10 мл на растение). Растения оставляют на тепличном стеллаже до полного высыхания капелек распыленного раствора и затем помещают в ростовую камеру, установленную на режим температуры 20oC и 14 световых часов на 10 дней. Контрольное заражение патогенами Phytophthora infestans проводят с интервалом от 30 минут до 12 дней после обработки предлагаемыми соединениями путем опрыскивания спорангиевой суспензией наружных поверхностей листьев (примерно 15 мл на растение). В одном эксперименте капли инокулята (10 капель, содержащих примерно 100 спорангиоспор) помешают на поверхность листьев, по две капли на листочек, и по одной на каждую сторону главной жилки. В другом эксперименте соединения наносят с лечебной целью через 24 часа после инокуляции P.infestans. Инокулированные растения выдерживают в условиях 100% относительной влажности в темноте в течение 24 часов при 20-18oC, и затем возвращают в ростовую камеру, где поддерживается температура 20oC и 12-часовой световой день. Степень тяжести болезни определяют через 4-8 дней после инокуляции растений визуальной оценкой доли или площади листа, пораженного фитофторозом. Испытание B. Индуцированная фитозащита рассады табака против Peronospora tabacina. Рассаду табака (сорт Ку-14 или Ку-16) выращивают из семян в горшках в теплице. Когда у проростков появятся 10 листочков или более, раствор предлагаемых соединений впрыскивают в стебель растения. В 1-3 день перед впрыскиванием или в 1-10 день после впрыскивания соединений осуществляют контрольное заражение растений конидиями грибов Peronospora tabacina Adam, которые являются возбудителями пероноспороза табака. Урожай конидии собирают с ранее инфицированных растений табака. Инокуляцию осуществляют раствором, содержащим 104-105 конидий/мл, используя примерно 50 мл на растение. В данном испытании можно также использовать вышеописанную методику инокуляции, поддержания культуры, оценки степени поражения растения. Хотя настоящее изобретение будет описано на некоторых предпочтительных примерах его осуществления, ясно, что изобретение не ограничивается этими конкретными вариантами его осуществления. Наоборот, изобретение подразумевает внесение всех возможных вариантов, изменений и эквивалентных решений в пределах существа и объема изобретения, определенных в нижеследующей формуле изобретения. Таким образом, нижеследующие примеры, включающие предпочтительные варианты осуществления изобретения, служат для его иллюстрации. Следует понимать, что детали показаны через пример и только для иллюстративных целей предпочтительных вариантов осуществления изобретения и представлены для того, чтобы дать представление о том, что, как полагают, является наиболее полезным и легко понятным в описании методов, а также принципов и концептуальных аспектов изобретения. Пример 1. N-(2-гидроксиэтил)-аминомасляная кислота. Раствор, содержащий 86 г кротоновой кислоты (1 моль) и этаноламина (1 моль) в пиридине (200 мл) кипятят с обратным холодильником в течение 2-3 часов и затем охлаждают. Полученный продукт фильтруют и после перекристаллизации получают названное соединение с т.пл. 178-180oC (соединение 1.1, табл. 1). По аналогичной методике получают соединения 1.2-1.7, 1.10, 1.11 и 1.13-1.15, приведенные в табл. 1. Пример 2. 3-Аминокапроновая кислота. Смесь 2-гексиновой кислоты (7,0 г, 0,06 моль) и концентрированного водного раствора гидроокиси аммония (70 мл) кипятят в течение 24 часов в автоклаве при температуре 150oC. Охлажденную смесь обрабатывают углеродной сажей и фильтруют. После упаривания растворителя неочищенный продукт перекристаллизовывают из этанола, и получают названное соединение, т.пл. 203oC (соединение 1.21, табл. 1). По аналогичной методике получают соединения 1.8, 1.9, 1.12-1.20, приведенные в табл. 1. Пример 3. N-бензоил-3-аминомасляная кислота. К охлажденному раствору 3-аминомасляной кислоты (13 г) в 2М NaOH (130 мл) прибавляют хлористый бензоил (19,7 г) в течение 2 часов. Смеси дают нагреться до комнатной температуры. После промывания диэтиловым эфиром, подкисления водной фазы 20% HCl, экстрагирования диэтиловым эфиром, сушки на MgSO4, отгонки растворителя и перекристаллизации остатка в смеси диэтиловый эфир/гексан получают названное соединение, т.пл. 150-152oC (соединение 1.16, табл. 1). По аналогичной методике получают соединение 1.17, приведенное в табл. 1. Пример 4. N-бензилоксикарбонил-3-аминомасляной кислоты (4-хлорфенил)-1-этиламид. Z-защищенную 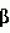 -аминомасляную кислоту (0,02 мл), (4-хлорфенил)-1-этиламина и 1,1 эквивалента ДЦК (дициклогексилкарбоимид) перемешивают в этилацетате при комнатной температуре в течение 16 часов. Выпавшую фазу отфильтровывают, фильтрат упаривают и очищают хроматографией на силикагеле (смесь гексан/этилацетат, 1:1 в качестве элюента) с получением названного соединения в виде смеси диастереоизомеров, т.пл.168-178oC. Пример 5. Хлоргидрат -аминомасляную кислоту (0,02 мл), (4-хлорфенил)-1-этиламина и 1,1 эквивалента ДЦК (дициклогексилкарбоимид) перемешивают в этилацетате при комнатной температуре в течение 16 часов. Выпавшую фазу отфильтровывают, фильтрат упаривают и очищают хроматографией на силикагеле (смесь гексан/этилацетат, 1:1 в качестве элюента) с получением названного соединения в виде смеси диастереоизомеров, т.пл.168-178oC. Пример 5. Хлоргидрат 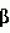 -аминомасляной кислоты. 5,15 г -аминомасляной кислоты. 5,15 г 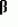 -аминомасляной кислоты (50 моль) растворяют в 650 мл метанола. После прибавления 5,5 мл концентрированной HCl, полученный раствор упаривают. Осадок порошкуют в диэтиловом эфире, декантируют и сушат. После разделения получают бесцветное масло. Данные микроанализа: C, 34,4; H, 7,2; N, 10,0; Cl, 25,4. Пример 6. Натриевая соль -аминомасляной кислоты (50 моль) растворяют в 650 мл метанола. После прибавления 5,5 мл концентрированной HCl, полученный раствор упаривают. Осадок порошкуют в диэтиловом эфире, декантируют и сушат. После разделения получают бесцветное масло. Данные микроанализа: C, 34,4; H, 7,2; N, 10,0; Cl, 25,4. Пример 6. Натриевая соль 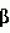 -аминомасляной кислоты. 2,06 г -аминомасляной кислоты. 2,06 г 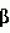 -аминомасляной кислоты (20 моль) растворяют в 100 мл смеси вода/метанол, (1:1). К полученному раствору прибавляют 1 эквивалент NaOH в 10 мл воды. Раствор упаривают, и полученный аморфный твердый продукт сушат. Данные микроанализа: C, 37,4; H, 6,7; N, 10,9. Пример 7. -аминомасляной кислоты (20 моль) растворяют в 100 мл смеси вода/метанол, (1:1). К полученному раствору прибавляют 1 эквивалент NaOH в 10 мл воды. Раствор упаривают, и полученный аморфный твердый продукт сушат. Данные микроанализа: C, 37,4; H, 6,7; N, 10,9. Пример 7. 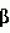 -Аминомасляной кислоты диэтиламмония хлорид. 1,4 г -Аминомасляной кислоты диэтиламмония хлорид. 1,4 г 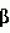 -аминомасляной кислоты (10 моль) растворяют в 100 мл метанола. К полученному раствору прибавляют диэтиламин (0,9 г, 12,3 моль), и остаток упаривают. Маслянистый остаток промывают диэтиловым эфиром, сливают и после сушки получают аморфное вещество. Н-ЯМР (CD3OD, 200 MHz) 1,29 (м, 9H, 3CH3; 2,25-2,45 (м, 2H,CH2);3.14(п, 4H, CH2CH3); 3,34-3,58(м,1H,CH) Пример 8. Зашита томатов от фузариозного вилта. Рассаду томата выращивали в стерильной почве в теплице. Когда растения достигали 4-листовой стадии их обрабатывали раствором, содержащим соединение формулы (I) путем пропитывания почвы в зоне расположения корней. Через 4 дня растения выдергивали из почвы, промывали водой и погружали их корневую систему на две минуты в суспензию конидий (107 конидий/мл) Fusarium oxysporum f.sp. lycopersici. Растения затем высаживали (без промывания) в горшки, заполненные стерильной почвой. Через 12 дней все инфицированные растения в контроле увяли, в то время как ни у одного обработанного растения после их инфицирования не отмечено увядания. Условия выращивания последних были такие же как и у неинокулированных контрольных растений без проверочного заражения. Полученные результаты приведены в табл. 2. Пример 9. По методике Примера 8, проводили аналогичный эксперимент с использованием более низкой концентрации БАМК. Полученные результаты приведены в табл. 3. Растения обрабатывали методом пропитывания почвы раствором, содержащим 2000 ч/млн (0,2 кг/га) соединения настоящего изобретения и инокулировали через 4 дня; оценку степени поражения проводили через 2 дня после инокуляции. Пример 10. В соответствии с вышеописанными методами изучали эффект аминомасляных кислот на ложную мучнистую росу подсолнечника. Результаты, приведенные в табл. 4, свидетельствуют о выраженной активности "БАМК" при оценке защитного эффекта растений. Пример 11. В соответствии с вышеописанными методами изучали эффект аминомасляных кислот на ложную мучнистую росу виноградной лозы, вызванную инокулятом Plasimopara viticola. Результаты, приведенные в табл. 5, свидетельствуют о хорошем защитном эффекте "БАМК". Пример 12. В соответствии с вышеописанными методами изучали эффект аминомасляных кислот на ложную мучнистую росу на рассаду огурцов и арбуза. Результаты, приведенные в табл. 6, свидетельствуют о хорошем защитном эффекте "БАМК"". Пример 13-15. В соответствии с вышеописанными методами изучали активность S-БАМК и R-БАМК против P. parasitica и A.bassicola у спаржевой капусты, кольраби и цветной капусты. Результаты, приведенные в табл. 7-9, соответственно, свидетельствуют о хорошем защитном эффекте R-БАМК. Во всех экспериментах инокуляцию грибного патогенна осуществляли либо за день до проведения обработки с лечебной целью, либо через 2 дня после обработки. Степень развития болезни оценивали через 9 дней после инокуляции. У БАМК отмечен также следующий лечебный эффект: при нанесении на инокулированные листовые пластинки на 0, 1, 2 и 3 день после инокуляции % защитного эффекта составлял 100, 86, 50 и 30, соответственно. Пример 16. В соответствии с вышеописанными методами изучали воздействие 25% DL-БАМК в виде смачивающегося порошка на клубни картофеля. Полученные результаты приведены в табл. 10. Пример 17. В соответствии с вышеописанными методами установлен четко выраженный ингибирующий эффект DL-БАМК против фитофторозной гнили клубней картофеля (сорт Bintje), выращиваемого в ростовой камере. Полученные результаты приведены в табл. 11. Пример 18. Испытание проводили в соответствии с методикой Примера 16, за исключением того, что их осуществляли в полевых условиях на посадках картофеля как сорта Alpha, так и Bintje. Полученные результаты приведены в табл. 12. Примеры 19-20. Исследовали устойчивость к возбудителю Peronospora tabacina, индуцированную у растений табака по методике, описанной Y.Cohen (Physiological и Molecular Plant Pathology (1994), 44:273-88), где активные вещества вводили впрыскиванием в стебли испытуемых растений. Полученные результаты обработки впрыскиванием в стебли приведены в табл. 13. Пример 21. В соответствии с методикой Примеров 19 - 20, эффект орошения почвы раствором DL-БАМК (3 мг на растение) на развитие голубой плесени у растений табака сорта Ку 16 показал 80% ингибирование болезни через 20 дней после контрольного заражения. Пример 22. Защиту культуры подсолнечника от ложной мучнистой росы, вызванной Plasmopora halstedii обеспечивали путем протравливания семян раствором БАМК. Так например, семечки подсолнечника протравливали в течение 24 часов в растворе, содержащем 10 мг БАМК на мл растворителя, и затем их сажали в горшки в теплице. Через 2 недели проростки подсолнечника инокулировали Plasmopora halstedii. Степень развития болезни оценивали через интервалы времени более 7 дней с получением следующих результатов. В то время как 100% растений в контроле оставались инфицированными, то только 2% обработанных растений были поражены инфекцией. Пример 23. Кукурузные зерна (линия 3376) выдерживали в воде для прорастания в течение 5 дней. Затем их погружали в раствор БАМК на одни сутки. Проросшее зерно затем промывали и выдерживали в контакте с Fusarium moniliforme в течение 1 дня, а затем засевали в горшки. Через две недели оценивали % развития болезни с получением результатов, указанных в табл. 14. Пример 24. Активность DL- -аминомасляной кислоты (10 моль) растворяют в 100 мл метанола. К полученному раствору прибавляют диэтиламин (0,9 г, 12,3 моль), и остаток упаривают. Маслянистый остаток промывают диэтиловым эфиром, сливают и после сушки получают аморфное вещество. Н-ЯМР (CD3OD, 200 MHz) 1,29 (м, 9H, 3CH3; 2,25-2,45 (м, 2H,CH2);3.14(п, 4H, CH2CH3); 3,34-3,58(м,1H,CH) Пример 8. Зашита томатов от фузариозного вилта. Рассаду томата выращивали в стерильной почве в теплице. Когда растения достигали 4-листовой стадии их обрабатывали раствором, содержащим соединение формулы (I) путем пропитывания почвы в зоне расположения корней. Через 4 дня растения выдергивали из почвы, промывали водой и погружали их корневую систему на две минуты в суспензию конидий (107 конидий/мл) Fusarium oxysporum f.sp. lycopersici. Растения затем высаживали (без промывания) в горшки, заполненные стерильной почвой. Через 12 дней все инфицированные растения в контроле увяли, в то время как ни у одного обработанного растения после их инфицирования не отмечено увядания. Условия выращивания последних были такие же как и у неинокулированных контрольных растений без проверочного заражения. Полученные результаты приведены в табл. 2. Пример 9. По методике Примера 8, проводили аналогичный эксперимент с использованием более низкой концентрации БАМК. Полученные результаты приведены в табл. 3. Растения обрабатывали методом пропитывания почвы раствором, содержащим 2000 ч/млн (0,2 кг/га) соединения настоящего изобретения и инокулировали через 4 дня; оценку степени поражения проводили через 2 дня после инокуляции. Пример 10. В соответствии с вышеописанными методами изучали эффект аминомасляных кислот на ложную мучнистую росу подсолнечника. Результаты, приведенные в табл. 4, свидетельствуют о выраженной активности "БАМК" при оценке защитного эффекта растений. Пример 11. В соответствии с вышеописанными методами изучали эффект аминомасляных кислот на ложную мучнистую росу виноградной лозы, вызванную инокулятом Plasimopara viticola. Результаты, приведенные в табл. 5, свидетельствуют о хорошем защитном эффекте "БАМК". Пример 12. В соответствии с вышеописанными методами изучали эффект аминомасляных кислот на ложную мучнистую росу на рассаду огурцов и арбуза. Результаты, приведенные в табл. 6, свидетельствуют о хорошем защитном эффекте "БАМК"". Пример 13-15. В соответствии с вышеописанными методами изучали активность S-БАМК и R-БАМК против P. parasitica и A.bassicola у спаржевой капусты, кольраби и цветной капусты. Результаты, приведенные в табл. 7-9, соответственно, свидетельствуют о хорошем защитном эффекте R-БАМК. Во всех экспериментах инокуляцию грибного патогенна осуществляли либо за день до проведения обработки с лечебной целью, либо через 2 дня после обработки. Степень развития болезни оценивали через 9 дней после инокуляции. У БАМК отмечен также следующий лечебный эффект: при нанесении на инокулированные листовые пластинки на 0, 1, 2 и 3 день после инокуляции % защитного эффекта составлял 100, 86, 50 и 30, соответственно. Пример 16. В соответствии с вышеописанными методами изучали воздействие 25% DL-БАМК в виде смачивающегося порошка на клубни картофеля. Полученные результаты приведены в табл. 10. Пример 17. В соответствии с вышеописанными методами установлен четко выраженный ингибирующий эффект DL-БАМК против фитофторозной гнили клубней картофеля (сорт Bintje), выращиваемого в ростовой камере. Полученные результаты приведены в табл. 11. Пример 18. Испытание проводили в соответствии с методикой Примера 16, за исключением того, что их осуществляли в полевых условиях на посадках картофеля как сорта Alpha, так и Bintje. Полученные результаты приведены в табл. 12. Примеры 19-20. Исследовали устойчивость к возбудителю Peronospora tabacina, индуцированную у растений табака по методике, описанной Y.Cohen (Physiological и Molecular Plant Pathology (1994), 44:273-88), где активные вещества вводили впрыскиванием в стебли испытуемых растений. Полученные результаты обработки впрыскиванием в стебли приведены в табл. 13. Пример 21. В соответствии с методикой Примеров 19 - 20, эффект орошения почвы раствором DL-БАМК (3 мг на растение) на развитие голубой плесени у растений табака сорта Ку 16 показал 80% ингибирование болезни через 20 дней после контрольного заражения. Пример 22. Защиту культуры подсолнечника от ложной мучнистой росы, вызванной Plasmopora halstedii обеспечивали путем протравливания семян раствором БАМК. Так например, семечки подсолнечника протравливали в течение 24 часов в растворе, содержащем 10 мг БАМК на мл растворителя, и затем их сажали в горшки в теплице. Через 2 недели проростки подсолнечника инокулировали Plasmopora halstedii. Степень развития болезни оценивали через интервалы времени более 7 дней с получением следующих результатов. В то время как 100% растений в контроле оставались инфицированными, то только 2% обработанных растений были поражены инфекцией. Пример 23. Кукурузные зерна (линия 3376) выдерживали в воде для прорастания в течение 5 дней. Затем их погружали в раствор БАМК на одни сутки. Проросшее зерно затем промывали и выдерживали в контакте с Fusarium moniliforme в течение 1 дня, а затем засевали в горшки. Через две недели оценивали % развития болезни с получением результатов, указанных в табл. 14. Пример 24. Активность DL-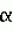 -аминомасляной и DL- -аминомасляной и DL-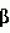 -аминомасляной кислот против фитофторозной гнили (возбудитель Phytophthora infestans) различных сортов культуры картофеля исследовали в ростовых камерах. Растения, после шести недель выращивания в горшках, опрыскивали указанным соединением и инокулировали через два дня. Данные развития болезни, снимаемые через 7 дней после инокуляции приведены в табл. 15. Пример 25. Активность БАМК была изучена против серой гнили огурцов и томатов. Молодые растения томатов (сорт Baby) 4-листовой стадии и молодые растения огурцов (сорт Dlila) 1 - листовой стадии были опрысканы раствором БАМК и после двух дней инокулированы суспензией спор Botrytis cinera. Растения культивировали в течение 4-х дней под пленочным покрытием Perspex и затем регистрировали заражение. Результаты показаны в табл. 16. Пример 26. a) Цель испытания - Для оценки эффективности БАМК против пирикуляриоза листьев риса, вызванного (Pyricularia oryzae). - Для оценки фитотоксичности испытуемого соединения на рисовой культуре (если имеется). b) Материал и Методика испытания. - Место проведения: Центр Защиты культурных растений. Южный Вьетнам. Long Dinh village, регион Chau Thanh, провинция Tien Giang. -Культура: рис. Сорт: ОМ 296. - Схема опыта: CRD. - Обработка: проводили 6 обработок следующим образом: Обработка - Норма расхода (100 ч/млн соответствует 0,1 кг/га) 1 - БАМК - 100 ч/млн 2 - БАМК - 500 ч/млн 3 - БАМК - 1000 ч/млн 4 - БАМК - 2000 ч/млн 5 - Пропиконазол 25 ЕС - 625 ч/млн 6 -10 обработку не проводили - - с) Методика проведения испытаний. + Для каждой обработки использовали по 5 глиняных горшков (30 см в диаметре и 28 см по высоте). + В каждый глиняный горшок высаживали 14-дневные рисовые проростки. + В глиняных горшках во время выращивания растений риса всегда поддерживали достаточное количество воды. + В каждый горшок на 3 день после пересадки растений прибавляли по 3 г мочевины. + Инокуляцию выполняли через 30 дней выращивания растений. Листья риса, пораженные пирикуляриозом собирали с делянок, измельчали и выдерживали во влажных условиях (при температуре 25oC и влажности 90%) в течение трех дней для развития грибницы и последующего образования из нее спор, переносимых на выращиваемые растения риса. + После инокуляции глиняные горшки помешали в условия затенения для инфицирования. Время проведения обработки. Проводили однократное опрыскивание на 7 сутки после инокуляции возбудителя пирикуляриоза листьев во время обработки 1-8 (23 - дневные растения), и однократное опрыскивание при появлении признаков болезни во время обработки 9 (37-дневное растение). Метод оценки. Для оценки количества случаев болезни и степени ее тяжести собирали все листья на лунку до и каждую неделю после появления признаков заболевания. Количество случаев и тяжесть поражения рисовой культуры вычисляли по следующей формуле Количество инфицированных листьев (%) заболеваемости = ------- -аминомасляной кислот против фитофторозной гнили (возбудитель Phytophthora infestans) различных сортов культуры картофеля исследовали в ростовых камерах. Растения, после шести недель выращивания в горшках, опрыскивали указанным соединением и инокулировали через два дня. Данные развития болезни, снимаемые через 7 дней после инокуляции приведены в табл. 15. Пример 25. Активность БАМК была изучена против серой гнили огурцов и томатов. Молодые растения томатов (сорт Baby) 4-листовой стадии и молодые растения огурцов (сорт Dlila) 1 - листовой стадии были опрысканы раствором БАМК и после двух дней инокулированы суспензией спор Botrytis cinera. Растения культивировали в течение 4-х дней под пленочным покрытием Perspex и затем регистрировали заражение. Результаты показаны в табл. 16. Пример 26. a) Цель испытания - Для оценки эффективности БАМК против пирикуляриоза листьев риса, вызванного (Pyricularia oryzae). - Для оценки фитотоксичности испытуемого соединения на рисовой культуре (если имеется). b) Материал и Методика испытания. - Место проведения: Центр Защиты культурных растений. Южный Вьетнам. Long Dinh village, регион Chau Thanh, провинция Tien Giang. -Культура: рис. Сорт: ОМ 296. - Схема опыта: CRD. - Обработка: проводили 6 обработок следующим образом: Обработка - Норма расхода (100 ч/млн соответствует 0,1 кг/га) 1 - БАМК - 100 ч/млн 2 - БАМК - 500 ч/млн 3 - БАМК - 1000 ч/млн 4 - БАМК - 2000 ч/млн 5 - Пропиконазол 25 ЕС - 625 ч/млн 6 -10 обработку не проводили - - с) Методика проведения испытаний. + Для каждой обработки использовали по 5 глиняных горшков (30 см в диаметре и 28 см по высоте). + В каждый глиняный горшок высаживали 14-дневные рисовые проростки. + В глиняных горшках во время выращивания растений риса всегда поддерживали достаточное количество воды. + В каждый горшок на 3 день после пересадки растений прибавляли по 3 г мочевины. + Инокуляцию выполняли через 30 дней выращивания растений. Листья риса, пораженные пирикуляриозом собирали с делянок, измельчали и выдерживали во влажных условиях (при температуре 25oC и влажности 90%) в течение трех дней для развития грибницы и последующего образования из нее спор, переносимых на выращиваемые растения риса. + После инокуляции глиняные горшки помешали в условия затенения для инфицирования. Время проведения обработки. Проводили однократное опрыскивание на 7 сутки после инокуляции возбудителя пирикуляриоза листьев во время обработки 1-8 (23 - дневные растения), и однократное опрыскивание при появлении признаков болезни во время обработки 9 (37-дневное растение). Метод оценки. Для оценки количества случаев болезни и степени ее тяжести собирали все листья на лунку до и каждую неделю после появления признаков заболевания. Количество случаев и тяжесть поражения рисовой культуры вычисляли по следующей формуле Количество инфицированных листьев (%) заболеваемости = -------  100 Общее количество наблюдаемых случаев поражения 9n9+8n8+7n7+6n6+5n5+4n4+3n3+2n2+n1 (%) заболеваемости = -------- 100 Общее количество наблюдаемых случаев поражения 9n9+8n8+7n7+6n6+5n5+4n4+3n3+2n2+n1 (%) заболеваемости = --------  100 (d) - Результаты и обсуждение. Через 7 дней после инокуляции листья риса были инфицированы Pyricularia orvzea. Количество инфицированных растений и степень их поражения были относительно одинаковыми во всех случаях обработки. После обработки эти показатели возрастали, но в меньшей степени по сравнению с необработанными растениями (отмечалось достоверное различие между тяжестью заболевания у обработанных и необработанных растений в испытании по методу Duncant). Это означает, что БАМК и пропиконазол в испытуемых дозах, приведенных выше, могут препятствовать распространению пирикуляриоза риса. В то же время не отмечено достоверного различия показателя эффективности против пирикуляриоза риса во всех случаях, где проводили обработку. Отмечена разница растений по высоте, однако никаких различий не наблюдали по количеству всходов на лунку между обработанными и необработанными растениями. Не зафиксировано никакой фитотоксичности после нанесения БАМК. (e) - Вывод. БАМК при использовании ее во время испытания в 4 дозах, то есть 100 ч/млн, 500 ч/млн, 1000 ч/млн, 2000 ч/млн, а пропиконазол 25 ЕС в дозе 625 обладают эффективностью для предупреждения развития пирикуляриоза риса. Более эффективно использование БАМК в небольших дозах. БАМК не приводит к повреждению растений риса. В заключение следует сказать, что БАМК обладает превосходным фунгицидным эффектом и даже превосходит пропиконазол против Pyriculana oruzae риса, при этом она оказывает свое действие путем индуцирования механизма местной и системной устойчивости (иммунитета). n1. Количество листьев по балльной оценке 1; n2. Количество листьев по балльной оценке 2; n3. Количество листьев по балльной оценке 3; n4. Количество листьев по балльной оценке 4; n5. Количество листьев по балльной оценке 5; n6. по балльной оценке 6; n7. по балльной оценке 7; n8. по балльной оценке 8; n9. по балльной оценке 9. N. Количество наблюдаемых случаев поражения листьев. Балльная оценка пирикуляриоза риса: использовали стандартную систему, приведенную в табл. 21, оценки рисовой культуры (IRIR - 2-издание. Июль 1980) Фитотоксичность оценивали визуально по 1 - 9-балльной системе оценки EWRS (где 1 означает отсутствие эффекта, 9 - полная гибель растения) на 1, 3, 7 и 14 день после проведения обработки. Еженедельно подсчитывали количество побегов риса и замеряли высоту растения. Пример 27. Получение н-бензоил-3-аминомасляной кислоты 1-метил-1-бутилового эфира. Смесь, содержащую 2,0 г н-бензоил-3-аминомасляной кислоты, 1,5 г 2-пентанола, 30 мл толуола и 0,004 г концентрированной H2SO4 кипятят с обратным холодильником в течение 6,5 часов. Образующуюся в результате воду удаляют азеотропной отгонкой. Охлажденный раствор промывают водой (3 х 15 мл), а затем 2% раствором бикарбоната натрия (3 х 15 мл). После упаривания растворителя и последующей отгонки избытка спирта при температуре 30oC (при давлении 0,4 мм ртутного столба) получают 2,5 г маслянистого продукта. Структуру полученного продукта подтверждают методами масс-спектроскопии и ЯМР. В соответствии с вышеописанной методикой и используя подходящий метод масс-спектроскопии и исходные реагенты получают соединения 2-8. Пример 28. Получение N-бензил-3-аминомасляной кислоты 1-метил-1-пентилового эфира. К 30 г кротоновой кислоты, растворенной в 120 г этилового спирта прибавляют 37,2 г бензиламина при температуре 10-15oC в течение 25 мин. Смесь затем нагревают до 75-77oC в течение 5 часа. Реакционную смесь охлаждают до комнатной температуры и после фильтрования получают 43,8 г н-бензил-3-аминомасляной кислоты. К 4,0 г бензилового продукта, растворенного в 50 мл толуола, прибавляют тионилхлорид (2,4) г при комнатной температуре в течение 15 минут. Полученную смесь нагревают при 80oC в течение 1 часа. После охлаждения к реакционной смеси прибавляют 7,2 г 2-гексанола при комнатной температуре в течение 15 мин. Затем реакционную смесь нагревают при 80oC в течение 4 часов. После этого смесь промывают последовательно водой (2х50 мл) и затем 2% раствором бикарбоната натрия (3 х 50 мл). После упаривания смеси и последующей отгонки избытка спирта получают 4,4 г названного соединения. В результате последующей очистки указанного соединения на колонке с силикагелем при использовании в качестве элюента смесь дихлорэтан:этилацетат (90: 10) получают 3,2 г названного сложного эфира. Структуру полученного продукта подтверждают методами масс-спектроскопии и ЯМР. В соответствии с вышеописанной методикой и используя подходящий метод масс-спектроскопии и исходные реагенты получают соединения 10 и 11. Пример 29. Получение хлоргидрата 100 (d) - Результаты и обсуждение. Через 7 дней после инокуляции листья риса были инфицированы Pyricularia orvzea. Количество инфицированных растений и степень их поражения были относительно одинаковыми во всех случаях обработки. После обработки эти показатели возрастали, но в меньшей степени по сравнению с необработанными растениями (отмечалось достоверное различие между тяжестью заболевания у обработанных и необработанных растений в испытании по методу Duncant). Это означает, что БАМК и пропиконазол в испытуемых дозах, приведенных выше, могут препятствовать распространению пирикуляриоза риса. В то же время не отмечено достоверного различия показателя эффективности против пирикуляриоза риса во всех случаях, где проводили обработку. Отмечена разница растений по высоте, однако никаких различий не наблюдали по количеству всходов на лунку между обработанными и необработанными растениями. Не зафиксировано никакой фитотоксичности после нанесения БАМК. (e) - Вывод. БАМК при использовании ее во время испытания в 4 дозах, то есть 100 ч/млн, 500 ч/млн, 1000 ч/млн, 2000 ч/млн, а пропиконазол 25 ЕС в дозе 625 обладают эффективностью для предупреждения развития пирикуляриоза риса. Более эффективно использование БАМК в небольших дозах. БАМК не приводит к повреждению растений риса. В заключение следует сказать, что БАМК обладает превосходным фунгицидным эффектом и даже превосходит пропиконазол против Pyriculana oruzae риса, при этом она оказывает свое действие путем индуцирования механизма местной и системной устойчивости (иммунитета). n1. Количество листьев по балльной оценке 1; n2. Количество листьев по балльной оценке 2; n3. Количество листьев по балльной оценке 3; n4. Количество листьев по балльной оценке 4; n5. Количество листьев по балльной оценке 5; n6. по балльной оценке 6; n7. по балльной оценке 7; n8. по балльной оценке 8; n9. по балльной оценке 9. N. Количество наблюдаемых случаев поражения листьев. Балльная оценка пирикуляриоза риса: использовали стандартную систему, приведенную в табл. 21, оценки рисовой культуры (IRIR - 2-издание. Июль 1980) Фитотоксичность оценивали визуально по 1 - 9-балльной системе оценки EWRS (где 1 означает отсутствие эффекта, 9 - полная гибель растения) на 1, 3, 7 и 14 день после проведения обработки. Еженедельно подсчитывали количество побегов риса и замеряли высоту растения. Пример 27. Получение н-бензоил-3-аминомасляной кислоты 1-метил-1-бутилового эфира. Смесь, содержащую 2,0 г н-бензоил-3-аминомасляной кислоты, 1,5 г 2-пентанола, 30 мл толуола и 0,004 г концентрированной H2SO4 кипятят с обратным холодильником в течение 6,5 часов. Образующуюся в результате воду удаляют азеотропной отгонкой. Охлажденный раствор промывают водой (3 х 15 мл), а затем 2% раствором бикарбоната натрия (3 х 15 мл). После упаривания растворителя и последующей отгонки избытка спирта при температуре 30oC (при давлении 0,4 мм ртутного столба) получают 2,5 г маслянистого продукта. Структуру полученного продукта подтверждают методами масс-спектроскопии и ЯМР. В соответствии с вышеописанной методикой и используя подходящий метод масс-спектроскопии и исходные реагенты получают соединения 2-8. Пример 28. Получение N-бензил-3-аминомасляной кислоты 1-метил-1-пентилового эфира. К 30 г кротоновой кислоты, растворенной в 120 г этилового спирта прибавляют 37,2 г бензиламина при температуре 10-15oC в течение 25 мин. Смесь затем нагревают до 75-77oC в течение 5 часа. Реакционную смесь охлаждают до комнатной температуры и после фильтрования получают 43,8 г н-бензил-3-аминомасляной кислоты. К 4,0 г бензилового продукта, растворенного в 50 мл толуола, прибавляют тионилхлорид (2,4) г при комнатной температуре в течение 15 минут. Полученную смесь нагревают при 80oC в течение 1 часа. После охлаждения к реакционной смеси прибавляют 7,2 г 2-гексанола при комнатной температуре в течение 15 мин. Затем реакционную смесь нагревают при 80oC в течение 4 часов. После этого смесь промывают последовательно водой (2х50 мл) и затем 2% раствором бикарбоната натрия (3 х 50 мл). После упаривания смеси и последующей отгонки избытка спирта получают 4,4 г названного соединения. В результате последующей очистки указанного соединения на колонке с силикагелем при использовании в качестве элюента смесь дихлорэтан:этилацетат (90: 10) получают 3,2 г названного сложного эфира. Структуру полученного продукта подтверждают методами масс-спектроскопии и ЯМР. В соответствии с вышеописанной методикой и используя подходящий метод масс-спектроскопии и исходные реагенты получают соединения 10 и 11. Пример 29. Получение хлоргидрата 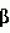 -аминомасляной кислоты. 6,0 г -аминомасляной кислоты. 6,0 г 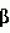 -аминомасляной кислоты растворяют в 20 мл воды. После прибавления 8,0 г HCl (32%), полученный раствор упаривают и полученное соединение сушат. Пример 30. Получение натриевой соли -аминомасляной кислоты растворяют в 20 мл воды. После прибавления 8,0 г HCl (32%), полученный раствор упаривают и полученное соединение сушат. Пример 30. Получение натриевой соли 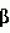 -аминомасляной кислоты. 6,0 г -аминомасляной кислоты. 6,0 г 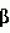 -аминомасляной кислоты растворяют в 20 мл воды. Затем к полученному раствору прибавляют 2,3 г NaOH, растворенный в 12 мл воды. Полученный раствор упаривают и твердый продукт сушат. Пример 31. Через 8 дней после инокуляции проводили испытание некоторых производных БАМК на их активность против настоящей мучнистой росы пшеницы, вызываемой Erysiphe Graminis. Результаты испытания приведены в табл. 22, которые сопоставимы с данными, полученными в случае без какой-либо обработки, которая показала только 12% эффективность защиты культуры. Пример 32. В соответствии с методами, описанными выше в Примерах 16 и 24, изучали активность некоторых производных БАМК против фитофтороза клубней картофеля, вызванного Ptytophotra Infestans. Результаты приведены в табл. 23, которые сопоставимы с данными, полученными в случае без какой-либо обработки, которая показала только 12% эффективность защиты культуры. Пример 33. В соответствии с методами, описанными выше, изучали активность некоторых производных БАМК против фитофтороза плодов помидоров, вызванного Ptytophotra Infestans. Результаты приведены в табл. 24, которые сопоставимы с данными, полученными в случае без какой-либо обработки, которая показала только 5 % эффективность защиты культуры. -аминомасляной кислоты растворяют в 20 мл воды. Затем к полученному раствору прибавляют 2,3 г NaOH, растворенный в 12 мл воды. Полученный раствор упаривают и твердый продукт сушат. Пример 31. Через 8 дней после инокуляции проводили испытание некоторых производных БАМК на их активность против настоящей мучнистой росы пшеницы, вызываемой Erysiphe Graminis. Результаты испытания приведены в табл. 22, которые сопоставимы с данными, полученными в случае без какой-либо обработки, которая показала только 12% эффективность защиты культуры. Пример 32. В соответствии с методами, описанными выше в Примерах 16 и 24, изучали активность некоторых производных БАМК против фитофтороза клубней картофеля, вызванного Ptytophotra Infestans. Результаты приведены в табл. 23, которые сопоставимы с данными, полученными в случае без какой-либо обработки, которая показала только 12% эффективность защиты культуры. Пример 33. В соответствии с методами, описанными выше, изучали активность некоторых производных БАМК против фитофтороза плодов помидоров, вызванного Ptytophotra Infestans. Результаты приведены в табл. 24, которые сопоставимы с данными, полученными в случае без какой-либо обработки, которая показала только 5 % эффективность защиты культуры.
ФОРМУЛА ИЗОБРЕТЕНИЯ1. Способ защиты сельскохозяйственной культуры от грибковых болезней, вызванных патогенными грибами, путем индуцирования системной устойчивости указанной культуры, отличающийся тем, что на указанную культуру или место ее произрастания наносят состав, содержащий эффективное количество соединения формулы I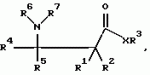 где (а) R1 и R2 каждый независимо означает водород; (b) R3 означает водород, C1 - C23 алкил; (c) R4 означает C1 - C8-алкил, а R5 означает водород; (d) R6 и R7 каждый независимо означает водород, бензоил, фенил-C1 - C4 алкил, где фенильный остаток означает незамещенный фенил; (e) X означает О и его соли, и культуру выбирают из группы зерновых, огурцов, арбуза, спаржевой капусты, цветной капусты, капусты кольраби, подсолнечника, картофеля, табака, винограда, кукурузы, риса, в количестве, достаточном для индуцирования механизма локального и системного иммунитета указанного культурного растения для подавления грибковой болезни. 2. Способ по п.1, отличающийся тем, что R1 и R2 каждый независимо означает водород, R3 означает водород, R4 означает C1 - C3-алкил, R5 означает водород, R6 и R7 каждый независимо означает водород и X означает кислород. 3. Способ по п.2, отличающийся тем, что R1 и R2 означают водород, R4 означает метил, R5 означает водород, R6 означает водород или метил и R7 означает водород. 4. Способ по п.1, отличающийся тем, что в качестве соединения формулы (I) используют R- где (а) R1 и R2 каждый независимо означает водород; (b) R3 означает водород, C1 - C23 алкил; (c) R4 означает C1 - C8-алкил, а R5 означает водород; (d) R6 и R7 каждый независимо означает водород, бензоил, фенил-C1 - C4 алкил, где фенильный остаток означает незамещенный фенил; (e) X означает О и его соли, и культуру выбирают из группы зерновых, огурцов, арбуза, спаржевой капусты, цветной капусты, капусты кольраби, подсолнечника, картофеля, табака, винограда, кукурузы, риса, в количестве, достаточном для индуцирования механизма локального и системного иммунитета указанного культурного растения для подавления грибковой болезни. 2. Способ по п.1, отличающийся тем, что R1 и R2 каждый независимо означает водород, R3 означает водород, R4 означает C1 - C3-алкил, R5 означает водород, R6 и R7 каждый независимо означает водород и X означает кислород. 3. Способ по п.2, отличающийся тем, что R1 и R2 означают водород, R4 означает метил, R5 означает водород, R6 означает водород или метил и R7 означает водород. 4. Способ по п.1, отличающийся тем, что в качестве соединения формулы (I) используют R-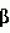 -аминомасляную кислоту. 5. Способ по п.1, отличающийся тем, что в качестве соединения формулы (I) используют N-бензоил-3-аминомасляной кислоты 1-метил-1-бутиловый эфир. 6. Способ по п.1, отличающийся тем, что в качестве соединения формулы (I) используют N-бензоил-3-аминомасляной кислоты 1-метил-5-пентиловый эфир. 7. Способ по п.1, отличающийся тем, что в качестве соединения формулы (I) используют N-бензоил-3-аминомасляной кислоты н-гептиловый эфир. 8. Способ по п.1, отличающийся тем, что в качестве соединения формулы (I) используют N-бензоил-3-аминомасляной кислоты н-гексиловый эфир. 9. Способ по п.1, отличающийся тем, что в качестве соединения формулы (I) используют N-бензоил-3-аминомасляной кислоты 1-метил-1-гептиловый эфир. 10. Способ по п.1, отличающийся тем, что в качестве соединения формулы (I) используют N-бензоил-3-аминомасляной кислоты 1-метил-1-гексиловый эфир. 11. Способ по п.1, отличающийся тем, что в качестве соединения формулы (I) используют N-бензоил-3-аминомасляной кислоты 1-метил-1-октиловый эфир. 12. Способ по п.1, отличающийся тем, что в качестве соединения формулы (I) используют N-бензоил-3-аминомасляной кислоты 1-метил-1-пентиловый эфир. 13. Способ по п.1, отличающийся тем, что в качестве соединения формулы (I) используют N-2-фенилэтил-3-аминомасляной кислоты н-октиловый эфир. 14. Способ по п.1, отличающийся тем, что в качестве соединения формулы (I) используют N-2-фенилэтил-3-аминомасляной кислоты 1-метил-1-пентиловый эфир. 15. Способ по п.1, отличающийся тем, что в качестве соединения формулы (I) используют натриевую соль 3-аминомасляной кислоты. 16. Способ по любому из пп.1 - 15, отличающийся тем, что культуру выбирают из группы огурцов, арбуза, спаржевой капусты, цветной капусты, капусты кольраби, картофеля, подсолнечника, табака, винограда, кукурузы, риса. 17. Способ по любому из пп.1 - 16, отличающийся тем, что культуру выбирают из группы подсолнечника, винограда, огурцов, арбуза, спаржевой капусты, капусты кольраби, цветной капусты, картофеля, табака и кукурузы. 18. Способ по любому из пп.1 - 16, отличающийся тем, что соединение наносят на листья или стебли растения. 19. Способ по любому из пп.1 - 16, отличающийся тем, что соединение наносят на корни растения. 20. Способ по любому из пп.1 - 16, отличающийся тем, что соединение вносят в почву. 21. Способ по любому из пп.1 - 16, отличающийся тем, что соединение наносят на семена, клубни растения. 22. Способ по любому из пп.1 - 16, отличающийся тем, что соединение наносят в предвсходовый период. 23. Способ по любому из пп.1 - 16, отличающийся тем, что соединение наносят в послевсходовый период. 24. Способ по любому из пп.1 - 16, отличающийся тем, что соединение наносят на культуру при норме расхода от 0,1 до 5 кг/га. 25. Способ по любому из пп.1 - 16, отличающийся тем, что соединение наносят на культуру при норме расхода от 0,2 до 2 кг/га. 26. Способ защиты риса от пирикуляриоза листьев по п.1 путем индуцирования местной и системной устойчивости указанной культуры, отличающийся тем, что на указанную культуру или место ее произрастания наносят эффективное количество соединения формулы I -аминомасляную кислоту. 5. Способ по п.1, отличающийся тем, что в качестве соединения формулы (I) используют N-бензоил-3-аминомасляной кислоты 1-метил-1-бутиловый эфир. 6. Способ по п.1, отличающийся тем, что в качестве соединения формулы (I) используют N-бензоил-3-аминомасляной кислоты 1-метил-5-пентиловый эфир. 7. Способ по п.1, отличающийся тем, что в качестве соединения формулы (I) используют N-бензоил-3-аминомасляной кислоты н-гептиловый эфир. 8. Способ по п.1, отличающийся тем, что в качестве соединения формулы (I) используют N-бензоил-3-аминомасляной кислоты н-гексиловый эфир. 9. Способ по п.1, отличающийся тем, что в качестве соединения формулы (I) используют N-бензоил-3-аминомасляной кислоты 1-метил-1-гептиловый эфир. 10. Способ по п.1, отличающийся тем, что в качестве соединения формулы (I) используют N-бензоил-3-аминомасляной кислоты 1-метил-1-гексиловый эфир. 11. Способ по п.1, отличающийся тем, что в качестве соединения формулы (I) используют N-бензоил-3-аминомасляной кислоты 1-метил-1-октиловый эфир. 12. Способ по п.1, отличающийся тем, что в качестве соединения формулы (I) используют N-бензоил-3-аминомасляной кислоты 1-метил-1-пентиловый эфир. 13. Способ по п.1, отличающийся тем, что в качестве соединения формулы (I) используют N-2-фенилэтил-3-аминомасляной кислоты н-октиловый эфир. 14. Способ по п.1, отличающийся тем, что в качестве соединения формулы (I) используют N-2-фенилэтил-3-аминомасляной кислоты 1-метил-1-пентиловый эфир. 15. Способ по п.1, отличающийся тем, что в качестве соединения формулы (I) используют натриевую соль 3-аминомасляной кислоты. 16. Способ по любому из пп.1 - 15, отличающийся тем, что культуру выбирают из группы огурцов, арбуза, спаржевой капусты, цветной капусты, капусты кольраби, картофеля, подсолнечника, табака, винограда, кукурузы, риса. 17. Способ по любому из пп.1 - 16, отличающийся тем, что культуру выбирают из группы подсолнечника, винограда, огурцов, арбуза, спаржевой капусты, капусты кольраби, цветной капусты, картофеля, табака и кукурузы. 18. Способ по любому из пп.1 - 16, отличающийся тем, что соединение наносят на листья или стебли растения. 19. Способ по любому из пп.1 - 16, отличающийся тем, что соединение наносят на корни растения. 20. Способ по любому из пп.1 - 16, отличающийся тем, что соединение вносят в почву. 21. Способ по любому из пп.1 - 16, отличающийся тем, что соединение наносят на семена, клубни растения. 22. Способ по любому из пп.1 - 16, отличающийся тем, что соединение наносят в предвсходовый период. 23. Способ по любому из пп.1 - 16, отличающийся тем, что соединение наносят в послевсходовый период. 24. Способ по любому из пп.1 - 16, отличающийся тем, что соединение наносят на культуру при норме расхода от 0,1 до 5 кг/га. 25. Способ по любому из пп.1 - 16, отличающийся тем, что соединение наносят на культуру при норме расхода от 0,2 до 2 кг/га. 26. Способ защиты риса от пирикуляриоза листьев по п.1 путем индуцирования местной и системной устойчивости указанной культуры, отличающийся тем, что на указанную культуру или место ее произрастания наносят эффективное количество соединения формулы I 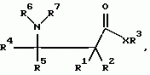 где (а) R1 и R2 каждый независимо означает водород; (b) R3 означает водород, C1 - C23-алкил; (c) R4 означает C1 - C8-алкил, а R5 означает водород; (d) R6 и R7 каждый независимо означает водород, бензоил, фенил-C1 - C4 алкил, где фенильный остаток означает незамещенный фенил; (e) X означает О и его соли. 27. Способ защиты томатов от Fusarium oxysporum of sp. Lycopersici путем индуцирования системной устойчивости указанной культуры, отличающийся тем, что на указанную культуру или место ее произрастания наносят эффективное количество соединения формулы I где (а) R1 и R2 каждый независимо означает водород; (b) R3 означает водород, C1 - C23-алкил; (c) R4 означает C1 - C8-алкил, а R5 означает водород; (d) R6 и R7 каждый независимо означает водород, бензоил, фенил-C1 - C4 алкил, где фенильный остаток означает незамещенный фенил; (e) X означает О и его соли. 27. Способ защиты томатов от Fusarium oxysporum of sp. Lycopersici путем индуцирования системной устойчивости указанной культуры, отличающийся тем, что на указанную культуру или место ее произрастания наносят эффективное количество соединения формулы I 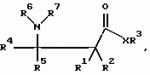 где (а) R1 и R2 каждый независимо означает водород; (b) R3 означает водород; (c) R4 означает C1 - C8-алкил, а R5 означает водород; (d) R6 и R7 каждый независимо означает водород; (e) X означает О и его соли. 28. Способ по п.27, отличающийся тем, что в качестве соединения формулы (I) используют R- где (а) R1 и R2 каждый независимо означает водород; (b) R3 означает водород; (c) R4 означает C1 - C8-алкил, а R5 означает водород; (d) R6 и R7 каждый независимо означает водород; (e) X означает О и его соли. 28. Способ по п.27, отличающийся тем, что в качестве соединения формулы (I) используют R-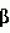 -аминомасляную кислоту. 29. Способ по любому из пп.27 и 28, отличающийся тем, что соединение наносят на листья или стебли растения. 30. Способ по любому из пп.27 и 28, отличающийся тем, что соединение вносят в почву. 31. Способ по любому из пп.27 и 28, отличающийся тем, что соединение наносят в послевсходовый период. 32. Способ защиты картофеля от фитофторозной гнили пасленовых путем индуцирования системной устойчивости указанной картофельной культуры, отличающийся тем, что на растения картофеля или место их произрастания наносят состав, содержащий эффективное количество DL - -аминомасляную кислоту. 29. Способ по любому из пп.27 и 28, отличающийся тем, что соединение наносят на листья или стебли растения. 30. Способ по любому из пп.27 и 28, отличающийся тем, что соединение вносят в почву. 31. Способ по любому из пп.27 и 28, отличающийся тем, что соединение наносят в послевсходовый период. 32. Способ защиты картофеля от фитофторозной гнили пасленовых путем индуцирования системной устойчивости указанной картофельной культуры, отличающийся тем, что на растения картофеля или место их произрастания наносят состав, содержащий эффективное количество DL - 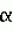 -аминомасляной кислоты, D - -аминомасляной кислоты, D - 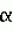 -аминомасляной кислоты, L - -аминомасляной кислоты, L - 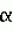 -аминомасляной кислоты, или их смеси. 33. Способ по п.32, отличающийся тем, что соединение наносят на листья или стебли растения. 34. Способ защиты культурного растения от серой гнили путем индуцирования системной устойчивости указанной культуры, отличающийся тем, что на указанную культуру наносят состав, содержащий эффективное количество соединения формулы I -аминомасляной кислоты, или их смеси. 33. Способ по п.32, отличающийся тем, что соединение наносят на листья или стебли растения. 34. Способ защиты культурного растения от серой гнили путем индуцирования системной устойчивости указанной культуры, отличающийся тем, что на указанную культуру наносят состав, содержащий эффективное количество соединения формулы I 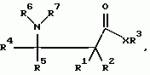 где (а) R1 и R2 каждый независимо означает водород; (b) R3 означает водород; (c) R4 означает C1 - C8-алкил, а R5 означает водород; (d) R6 и R7 каждый независимо означает водород; (e) X означает О и его соли. 35. Способ по п. 34, отличающийся тем, что в качестве соединения используют где (а) R1 и R2 каждый независимо означает водород; (b) R3 означает водород; (c) R4 означает C1 - C8-алкил, а R5 означает водород; (d) R6 и R7 каждый независимо означает водород; (e) X означает О и его соли. 35. Способ по п. 34, отличающийся тем, что в качестве соединения используют 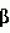 -аминомасляную кислоту. 36. Способ по п.34, отличающийся тем, что указанное культурное растение выбирают из группы культуры томатов и огурцов. 37. Способ по п.34, отличающийся тем, что указанный состав наносят на листья или стебли растения. Приоритет по пунктам: 12.12.93, 30.11.94 по пп.1 - 4, 16 - 25, 27; 30.11.94 по пп.1 - 4, 16 - 25, 27 - 37. -аминомасляную кислоту. 36. Способ по п.34, отличающийся тем, что указанное культурное растение выбирают из группы культуры томатов и огурцов. 37. Способ по п.34, отличающийся тем, что указанный состав наносят на листья или стебли растения. Приоритет по пунктам: 12.12.93, 30.11.94 по пп.1 - 4, 16 - 25, 27; 30.11.94 по пп.1 - 4, 16 - 25, 27 - 37.Популярные патенты: 2144756 Селекционная сеялка для посева семян в кассеты ... где ячейки 16 для забора семян из разгрузочной камеры 11 семенной банки 3 расположены рядами по 2-3 штуки, только в корпусе 14 высевающего барабана 12 они выполнены в виде полусферических лунок, а на экране 15 им придана форма самого крупного семени одного или группы видов со сходными семенами, причем сам экран 15 выполнен съемным с возможностью крепления на поверхности корпуса 14 с помощью хомутов 17. В качестве транспортера для перемещения засеваемых кассет 18 применен ящик 19, который установлен в направляющих 20 корпуса 1 с возможностью совершать возвратно-поступательные движения. На верхнем ребре одной из его боковых стенок натянута роликовая цепь 21, взаимодействующая со ... 2462864 Устройство составления экономичного кормового рациона и экономичного кормления животных и птиц ... дозы расхода корма вычисляют в зависимости от дозы расхода каждого ингредиента корма, при этом формируют сигнал величины дозы расхода корма, периодически изменяют сигнал сформированной величины дозы расхода корма в диапазоне между технологически допустимыми наименьшим и наибольшим ее заданными значениями, причем в зависимости от значения изменяемого сигнала сформированной величины дозы расхода корма вычисляют стоимость продукции данной партии животных или птицы, причем стоимость расхода корма вычисляют в зависимости от сформированной величины дозы расхода корма, затем вычисляют первую разность между стоимостью продукции и стоимостью расхода корма в качестве показателя прибыли в ... 2479988 Способ формирования линейно ориентированного виноградника с капельным орошением (версия 3) ... сосуд 10 с герметичной верхней его частью, в котором выполняют вертикальный паз 11 для верхней части патрубка 8, где его и располагают. При этом верхнюю часть чашеобразного сосуда 10 выполняют в виде вертикальной опоры 12 с цилиндрической верхней частью 13 и с резьбой для последующего свинчивания с вертикальной опорой 1, которую выполняют также с резьбой и со сквозными ортогональными отверстиями 3, которые выполняют не меньше диаметра направляющей проволоки 4 и позиционно располагают на соответствующем уровне расположения их, после чего выполняют функциональное соединение вертикальной опоры 12 чашеобразного сосуда 10 и вертикальной опоры 1 со сквозными отверстиями 3, в которых на ... 2197817 Поплавок для рыболовных удочек и снастей ... Насадка 5 может быть выполнена сплошной из плотного пенопласта с осевым отверстием для тугой посадки на шток 4 или в виде пустотелого герметичного пластикового цилиндра с осевым отверстием или других материалов с равным или меньшим удельным весом, чем у твердого пенопласта. Верхний свободный от насадки конец штока 4 выполняет роль "мачты" либо сам непосредственно за счет увеличения длины, либо за счет надетой на него цветной тонкостенной пластиковой трубки 6. В нижней части трубки 6 выполнены отверстия 7 для вытекания попадающей в нее воды. В дне 8 цилиндра корпуса 1 с наружной его стороны расположен конусообразный патрубок 9 для соединения с надеваемым на него наконечником 10, ... 2059368 Способ борьбы с насекомыми-листогрызущими вредителями растений ... расхода бакуловирусных препаратов и сократить латентный период их действия. Снижение нормы расхода вирусных препаратов, кроме сокращения затрат, создает дополнительные преимущества, а именно повышает безопасность труда для персонала, контактирующего с биопрепаратами в процессе производственной деятельности. Известно, что энтомопатогенные бакуловирусы экологически безвредны. Однако вирусы, как и любые другие препараты, содержащие белок, обладают аллергенными свойствами. Поэтому уменьшение концентрации вирусных частиц в биопрепаратах снижает риск возникновения иммунологических сдвигов в организме людей или животных. Хитиназа, выделяемая из микробиологических источников, также ... |
Еще из этого раздела: 2474105 Плодосъемник шолина 2234219 Композиция для отпугивания паразитов 2261597 Способ борьбы с нематодами - возбудителями болезней сельскохозяйственных растений 2169462 Улей (варианты), способ его сборки и способ круглогодичного содержания в нем пчел 2114555 Способ электродиагностики вымени крупного рогатого скота и устройство для его осуществления 2261592 Ферма двухконсольного дождевального агрегата 2476277 Способ защиты почв от остатков пестицидов 2075933 Композиция для иммунизации растений от различных фитопатогенов 2110911 Способ выращивания птицы 2479996 Экологический комплекс для аквакультуры и рекультивации морских вод |
Изобретения в сельском хозяйстве
Обработка почвы в сельском и лесном хозяйствах
Посадка, посев, удобрение
Уборка урожая, жатва
Обработка и хранение продуктов полеводства и садоводства
Садоводство, разведение овощей, цветов, риса, фруктов, винограда, лесное хозяйство
Новые виды растений или способы их выращивания
Производство молочных продуктов
Животноводство, разведение и содержание птицы, рыбы, насекомых, рыбоводство, рыболовство
Поимка, отлов или отпугивание животных
Консервирование туш животных, или растений или их частей
Биоцидная, репеллентная, аттрактантная или регулирующая рост растений активность химических соединений или препаратов
Хлебопекарные печи, машины и прочее оборудование для хлебопечения
Машины или оборудование для приготовления или обработки теста
Обработка муки или теста для выпечки, способы выпечки, мучные изделия
|
|
||