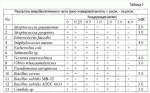
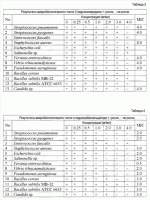
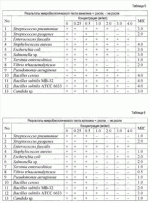
Бактерицидный агент и бактерицидная композицияПатент на изобретение №: 2414818 Автор: ЦУТИДА Юудзоу (JP), ЦУТИДА Котароу (JP), ВАТАНАБЕ Кунитомо (JP), САКУРАИ Дайсуке (JP), КОКЕЦУ Мамору (JP), КАВАБЕ Мицуо (JP), УЦУМИ Теруо (JP) Патентообладатель: ЦУТИДА Юудзоу (JP) Дата публикации: 20 Марта, 2010 Начало действия патента: 8 Марта, 2007 Адрес для переписки: 129090, Москва, ул.Б.Спасская, 25, стр.3, ООО "Юридическая фирма Городисский и Партнеры", Е.Е.Назиной, рег. 517 Изобретение относится к области бактерицидных средств. Бактерицидный агент содержит 5,7,4 Область техники, к которой относится изобретение Данное изобретение относится к бактерицидному агенту и бактерицидной композиции. Уровень техники В течение продолжительного времени известно, что экстракт бамбука (Sasa) имеет бактерицидную активность. Например, сообщалось, что этот экстракт имеет бактерицидное действие против Staphylococcus aureus, Pseudomonas aeruginosa и Escherichia coli, которые являются этиологическими факторами раневой инфекции (Патентные документы 1 и 2), а также против Helicobacter pilori, который считается этиологическим фактором язвы желудка. Кумазаса является растением, принадлежащим к семейству Gramineae, роду Sasa. Обычно Sasa, растущий в горах, называют Кумазаса, причем этот термин является общим для растений Sasa, край листьев которых становится заболевающим и этиолированным зимой. Имеются различные Sasa, называемые Кумазаса, некоторые из которых имеют научное название В течение продолжительного времени известно, что Кумазаса (Sasa albo marginata) обнаруживает чрезвычайно большое разнообразие эффектов, сравнимое с Gymnema sylvestre из Индии, гуайявой (гуавой) из Китая и Lycium chinense из Южной Кореи, которые известны в качестве травяного лекарственного средства, используемого в восточной медицине. В Японии также использовали Кумазаса в качестве традиционного этнофармакологического лекарственного средства при гастропатии, сахарном диабете, гипертензии и т.д. (Непатентные документы 1-3), а также использовали в качестве упаковочного материала для пищевых продуктов, например Sasa-dango или Chimaki, а также аналептического средства. Эксперименты на животных, выполненные в послевоенные годы, выявили, что Кумазаса имел ингибирующую активность против гепатомы в мышах, и некоторые фармакологические исследования проводились с точки зрения канцеростатического действия (Непатентный документ 4). Кроме того, проводились исследования превосходной консервирующей активности (Непатентный документ 5) и микробиологической активности (Непатентный документ 6), которые имеет Кумазаса. Однако в большинстве этих исследований не сообщалось ничего кроме анализа органических кислот с использованием газовой хроматографии. Имеется несколько сообщений, которые раскрывают выделение и очистку основных компонентов, которые обеспечивают бактерицидное действие. Было также известно, что кумаровая кислота и ее производные имеют бактерицидную активность против E. coli, Staphylococcus aureus и Pseudomonas aeruginosa (Патентный документ 3). Кроме того, было также известно, что экстракт Кумазаса содержит фенилпропаноиды, такие как кумаровая кислота, феруловая кислота, кофейная кислота, и ванилин, 3-гидроксипиридин и т.п., и смесь этих соединений обнаруживает бактерицидную активность против Escherichia coli, Staphylococcus aureus и Pseudomonas aeruginosa (Патентный документ 4). Патентный документ 1: WO 00/067707 Патентный документ 2: JP 2003-201247 А Патентный документ 3: JP 2004-359626 А Патентный документ 4: JP 2006-36731 А Непатентный документ 1: M. Shibata, K. Kubo, M. Onoda, Journal of the Pharmaceutical Society of Japan, 98, 1436 (1978). Непатентный документ 2: S. Okabe, K. Takeuchi, K. Takagi, M. Shibata, Jpn. J. Pharmacol., 25, 608 (1975). Непатентный документ 3: M. Shibata, F. Sato, K. Takeshita, K. Otani, Natural Medicines (Shoyaku-gaku zasshi), 34, 274 (1980). Непатентный документ 4: M. Shibata, K. Kubo, M. Onoda, Folia Pharmacol. Jpn, 72, 531-541 (1976). Непатентный документ 5: N.V. Chuyen, T. Kurata, H. Kabo, J. Antibact. Antifung. Agents, 11, 69-75 (1983). Непатентный документ 6: N. V. Chuyen, H. Kato, Agric. Biol. Chem., 46, 2795-2801 (1982) 3-1128 (2004). Описание изобретения Проблемы, подлежащие решению посредством данного изобретения Задачей данного изобретения является предоставление бактерицидного агента. Другой задачей данного изобретения является предоставление бактерицидной композиции, содержащей этот бактерицидный агент. Средства для решения проблемы Данное изобретение предоставляет бактерицидный агент и бактерицидную композицию, содержащую его, следующим образом. 1. Бактерицидный агент, содержащий в качестве эффективного ингредиента по меньшей мере один ингредиент, выбранный из группы, состоящей из п-гидроксибензальдегида, 5,7,4'-тригидрокси-3',5'-диметоксифлавона, 3-гидроксипиридина и ванилина. 2. Бактерицидный агент согласно абзацу 1, приведенному выше, где указанный микроорганизм выбран из группы, состоящей из Streptococcus, Enterococcus, Staphylococcus, Escherichia, Salmonella, Yersinia, Vibrio, Pseudomonas, Bacillus и Candida. 3. Бактерицидный агент, содержащий в качестве эффективного ингредиента по меньшей мере один ингредиент, выбранный из группы, состоящей из п-гидроксибензальдегида и 5,7,4'-тригидрокси-3',5'-диметоксифлавона. 4. Бактерицидный агент согласно абзацу 3, приведенному выше, где указанный микроорганизм выбран из группы, состоящей из Streptococcus, Enterococcus, Staphylococcus, Escherichia, Salmonella, Yersinia, Vibrio, Pseudomonas, Bacillus и Candida. 5. Бактерицидный агент согласно абзацу 1, приведенному выше, где указанный агент содержит 3-гидроксипиридин в качестве эффективного ингредиента, а указанный микроорганизм выбран из группы, состоящей из Streptococcus pneumoniae, Streptococcus pyogenes, Staphylococcus aureus, Yersinia enterocolitica, Pseudomonas aeruginosa и Candida sp. 6. Бактерицидный агент согласно абзацу 1, приведенному выше, где указанный агент содержит п-гидроксибензальдегид в качестве эффективного ингредиента, а указанный микроорганизм выбран из группы, состоящей из Streptococcus pneumoniae, Streptococcus pyogenes, Staphylococcus aureus, Escherichia coli, Salmonella sp., Yersinia enterocolitica, Vibrio parahaemolyticus, Pseudomonas aeruginosa, Bacillus cereus, Bacillus subtilis и Candida sp. 7. Бактерицидный агент согласно абзацу 1, приведенному выше, где указанный агент содержит ванилин в качестве эффективного ингредиента, а указанный микроорганизм выбран из группы, состоящей из Streptococcus pneumoniae, Streptococcus pyogenes, Staphylococcus aureus, Escherichia coli, Salmonella sp., Yersinia enterocolitica, Vibrio parahaemolyticus, Bacillus cereus, Bacillus subtilis и Candida sp. 8. Бактерицидный агент согласно абзацу 1, приведенному выше, где указанный агент содержит 5,7,4'-тригидрокси-3',5'-диметоксифлавон в качестве эффективного ингредиента, а указанный микроорганизм выбран из группы, состоящей из Salmonella sp. и Pseudomonas aeruginosa. 9. Бактерицидная композиция, содержащая бактерицидный агент по любому из абзацев 1-8, приведенных выше. Термин «микроорганизм» в данном контексте включает в себя бактерии, микобактерии, цианобактерии, архебактерии, грибы, дрожжи, водоросли, вирусы и тому подобное, и, в частности, этот термин обозначает микроорганизмы, которые оказывают нежелательное действие на животных и растения, в том числе на человека. Эффекты изобретения Бактерицидный агент в соответствии с данным изобретением имеет высокую микробиологическую активность против различных микроорганизмов, в частности Streptococcus, Enterococcus, Staphylococcus, Escherichia, Salmonella, Yersinia, Vibrio, Pseudomonas, Bacillus, Candida и т.д.; более конкретно, Streptococcus pneumoniae, Streptococcus pyogenes, Staphylococcus aureus, Escherichia coli, Salmonella sp., Yersinia enterocolitica, Vibrio parahaemolyticus, Pseudomonas aeruginosa, Bacillus cereus, Bacillus subtilis и Candida sp. Наилучший способ осуществления изобретения Для выяснения природы бактерицидного действия Кумазаса (Sasa albo marginata) и описания компонентов, эффективных для супрессии бактерий, авторы данного изобретения фракционировали экстракт, полученный с использованием горячей воды, листа Кумазаса при помощи различных растворителей. После фракционирования его хроматографией на силикагеле авторы выполняли разделение с использованием ТСХ, а также с использованием препаративной колонки ODS для высокоэффективной жидкостной хроматографии для достижения выделения и очистки. Кроме того, они определяли структуру выделенных соединений с использованием различных спектров и проводили микробиологические тесты с использованием 13 типов бактерий. В результате они обнаружили, что вышеописанные п-гидроксибензальдегид, 5,7,4'-тригидрокси-3',5'-диметоксифлавон (здесь также называемый далее «трицином»), 3-гидроксипиридин, транс-п-кумаровая кислота (транс-п-гидроксикоричная кислота) и ванилин проявляют специфические виды бактерицидной активности против различных микроорганизмов, завершив тем самым данное изобретение. Данное изобретение будет далее описано в деталях. В качестве экспериментального материала использовали экстракт Кумазаса (Sasa albo marginata), полученный с использованием горячей воды, из Hououdou Co., Ltd. (товарное название: TWEBS). Растворитель в 10 г экстракта, полученного с использованием горячей воды (далее называемого Этот горячий водный экстракт подвергали фракционированию с использованием различных растворителей. То есть горячий водный экстракт (Sa) жизнеспособных клеток экстрагировали этилацетатом и растворитель в полученном этилацетатном слое выпаривали с получением посредством этого растворимой в этилацетате фракции (далее называемой Согласно этому бактерицидному тесту, растворимая в этилацетате фракция имела бактерицидную активность, почти эквивалентную активности горячего водного экстракта Кумазаса. С другой стороны, бактерицидная активность растворимой в н-бутаноле фракции и фракции водного слоя была слабой. Вышеописанный бактерицидный тест выявил, что бактерицидная активность была распределена в растворимой в этилацетате фракции. Таким образом, 2,3 кг горячего водного экстракта листа Кумазаса (Sa) экстрагировали этилацетатом. Растворитель в полученном этилацетатном слое выпаривали с получением 78 г растворимой в этилацетате фракции (Sa-1). Бактерицидную активность полученной фракции Sa-1 оценивали против Staphylococcus aureus. В результате эта фракция показала бактерицидную активность. Бактерицидная активность против Staphylococcus aureus Фракционирование и очистка компонентов, имеющих бактерицидную активность Фракционирование растворимой в этилацетате фракции (Sa-1) С использованием хроматографии на нейтральном силикагеле фракционировали 52 г растворимой в этилацетате фракции (Sa-1), которая обнаруживала бактерицидную активность. Для элюции колонки использовали ступенчатый способ, в котором соотношения смешивания растворителей ступенчато изменяли. Используемыми растворителями были: н-гексан/этилацетат = 5:5 в количестве 2,5 л и 4:6, 3:7, 2:8, в каждом случае в количестве 1 л, и метанол отдельно в количестве 2,5 л. Разделение элюированных соединений выполняли на основании результата ТХА и детектирование пятен на хроматограмме выполняли с использованием УФ 254 нм. В результате растворимую в этилацетате фракцию фракционировали на 7 фракций. Эти 7 фракций были названы, соответственно, Sa-1-A (90 мг), Sa-1-B (250 мг), Sa-1-C (3,36 г), Sa-1-D (3,00 г) Sa-1-Е (110 мг), Sa-1-F (1,56 г), Sa-1G (30,0 г). Сначала Sa-1-С (3,36 г) растворяли в 5 мл хлороформа и к раствору добавляли н-гексан в равном количестве с последующим оставлением этой смеси стоять в течение ночи. В результате эта смесь разделялась на два слоя. Верхний слой (далее называемый Анализ Sa-1-(C) К 2,22 г Sa-1-С(1) добавляли 3,50 г силикагеля и эти компоненты адсорбировали в нем с последующим фракционированием с использованием колоночной хроматографии на силикагеле. Для элюции колонки использовали ступенчатый способ. Использовали следующий состав растворителей, хлороформ:ацетон = 20:1 в количестве 2 л, и 7:3, 6:4, в каждом случае в количестве 100 мл, и только ацетон в количестве 500 мл. Для извлечения использовали флаконы объемом 50 мл. Среди 110 флаконов объемом 50 мл флаконы ВЖХ-разделение концентрата (Sa-1-С(1)-а) из флаконов Условия элюции: колонка: Wakosil-II 5C18HG prep, 20,0 мм × 250 мм, подвижная фаза: 20% водный раствор ацетонитрила, скорость тока: 5 мл/мин, температура колонки: 30°С, детектирование: УФ 260 нм. Основной пик при 34,5 мин разделяли с получением 60 мг белого твердого вещества (далее называемого 1Н- и 13С-ЯМР-спектры белого твердого вещества (Sa-1-С(1)-аа) 1 Н-ЯМР (500 МГц, CD3OD): 13 С-ЯМР (125 МГц, CD3OD): ИК (Kbr): 3179, 1668 см-1 Т. пл.: 114-115°С Сигнал водорода при Затем, среди 110 флаконов с объемом 50 мл флаконы Среди 42 флаконов с объемом 50 мл, флаконы 1Н- и 13С-ЯМР-спектры светло-желтого твердого вещества (Sa-1-С(1)-baa) 1Н-ЯМР (500 МГц, CD3OD): 13С-ЯМР (125 МГц, CD3 OD): ИК (KBr): 3168, 1670 см-1 Т. пл.: 118-119°С Сигнал водорода в Анализ Sa-1-(С(2) Перекристаллизацию (ацетон/гексан) 1,14 г Sa-1-С(2) проводили два раза с получением 478 мг светло-желто-зеленого твердого вещества (далее называемого 1Н- и 13С-ЯМР-спектры светло-желто-зеленого твердого вещества (Sa-1-С(2)-а) 1Н-ЯМР (500 МГц, CD 3OD): 13С-ЯМР (125 МГц, CD3OD): ИК (KBr): 3168, 2830, 975 см-1 Т. пл.: 213-214°С Два дублетных сигнала, соответствующих четырем атомам водорода, в Анализ Sa-1-F К Sa-1-F (1,56 г), который был одной из фракций, полученных фракционированием растворимой в этилацетате фракции колоночной хроматографией на силикагеле, добавляли хлороформ и полученную смесь тщательно перемешивали с последующим удалением жидкого слоя, содержащего компоненты, которые растворяются в хлороформе. После этого к остатку добавляли ацетон, который не растворяется в хлороформе, и полученную смесь разделяли на растворимый в ацетоне жидкий слой (далее называемый Анализ Sa-1-F(1) К 162 мг Sa-1-F(1) добавляли опять ацетон для его растворения и полученную смесь оставляли стоять. После этого извлекали прозрачную светлую часть жидкого слоя. Растворитель ацетон выпаривали с получением 10 мг желтого твердого вещества (далее называемого С использованием дейтерированного ацетона измеряли 1Н- и 13С-ЯМР-спектры этого желтого твердого вещества (Sa-1-F(1)-а). 1Н- и 13С-ЯМР-спектры желтого твердого вещества (Sa-1-F(1)-а) 1Н-ЯМР (500 МГц, (CD3) 2CO): 13С-ЯМР (125 МГц, (CD3)2CO): ИК (KBr): 3357, 1615 см-1 Т. пл.: 276-277°С 13С-ЯМР-спектр выявил, что имелись 17 атомов углерода, и DEPT выявил, что имелись 2 первичных атома углерода, 5 третичных атомов углерода и 10 четвертичных атомов углерода. Синглетный сигнал, соответствующий 6 атомам водорода в Анализ Sa-1-F(2) К 1,40 г Sa-1-F(2) добавляли 3,00 г силикагеля, и эти компоненты адсорбировались в нем, после чего проводили фракционирование с использованием колоночной хроматографии на силикагеле. Для элюции колонки использовали ступенчатый способ. Использованными растворителями были смесь хлороформ/ацетон = 10:1, 8:2 в количестве 200 мл, 5:5, 3:7 и только ацетон, в каждом случае в количестве 300 мл, и только метанол в количестве 200 мл. Для извлечения использовали 53 флакона объемом 50 мл. Среди 53 флаконов объемом 50 мл флаконы 1Н- и 13С-ЯМР-спектры светло-желтого твердого вещества (Sa-1-F(2)-а) 1Н-ЯМР (500 МГц, CD 3OD): 13С-ЯМР (125 МГц, CD3OD): ИК (KBr): 3449 см-1 Т. пл.: 127-128°С Сигналы, соответствующие четырем атомам водорода, в Бактерицидный тест Способ разведения с использованием агара В качестве бактерицидного тест-способа для транс-кумаровой кислоты, 3-гидроксипиридина, п-гидроксибензальдегида и ванилина использовали способ разведений с применением агара. В способе разведений с использованием агара раствор, в котором растворена проба, серийно разводят несколько раз и каждый из растворов разведенных проб смешивают с агаровой средой для получения агаров для чашек, имеющих различную концентрацию проб. Затем бактерии инокулируют на эти агары для проб. В случаях, когда проба имеет бактерицидную активность, рост бактерий на этих чашках может быть ингибирован. Самую низкую концентрацию, которая может ингибировать рост этих бактерий, называют минимальной ингибирующей концентрацией (MIC), оценивая посредством этого степень бактерицидной активности пробы. Сначала 400 мг пробы растворяли в 1 мл ДМСО с получением раствора пробы 400 мг/мл. Затем 0,5 мл этого раствора пробы 400 мг/мл разводили в 2 раза с получением раствора пробы 200 мг/мл. Таким же образом готовили раствор пробы 300 мг/мл. После этого 0,2 мл каждого из этих растворов пробы смешивали с 19,8 мл среды BHI (агара для инфузии головного мозга и сердца, (Becton Dickinson, MD) и готовили чашки с агаровой средой, имеющие концентрацию пробы 4,0 мг/мл, 3,0 мг/мл, 2,0 мг/мл, 1,0 мг/мл, 0,5 мг/мл и 0,25 мг/мл в чашках. В качестве контроля для сравнения бактерицидной активности проб готовили чашки с агаровой средой, содержащие катехин, имеющий вышеуказанные концентрации. Для растворения катехина использовали стерилизованную воду, так как катехин был нерастворимым в ДМСО. В качестве тестируемых бактерий использовали 13 типов бактерий, т.е. Streptococcus pneumoniae, Streptococcus pyogenes, Enterococcus faecalis, Staphylococcus aureus, Escherichia coli, Salmonella sp., Yersinia enterocolitica, Vibrio parahaemoliticus, Pseudomonas aeruginosa, Bacillus cereus Bacillus subtilis MB-32, Bacillus subtilis ATCC6633 и Candida sp. Каждую из этих бактерий смешивали с 2 мл стерилизованной жидкой среды MBHR (Muller Hinton BrothR (Becton Dickinson, MD) для получения бактериальной суспензии, имеющей мутность 1 (концентрация бактерий 108/мл). Предварительно небольшие пробирки устанавливали в каждую ячейку решетки и стерилизовали, и 1 мл из 13 бактериальных суспензий добавляли в каждую из этих небольших пробирок, установленных в решетке, соответственно. С использованием микроплантера (SAKUMA, model: MIT-P), аликвоту 10 мкл брали из каждой тест-пробирки в этой решетке и переносили в другую тест-пробирку, и перенесенные бактериальные суспензии разводили в 100 раз (бактериальная концентрация 106/мл). С использованием микроплантера 10 мкл ( Описанные выше результаты показали, что транс-п-кумаровая кислота имела активность против Streptococcus pneumoniae, Streptococcus pyogenes, Staphylococcus aureus, Yersinia enterocolitica, Vibrio parahaemoliticus, Bacillus cereus, Bacillus subtilis АТСС6633, Candida sp.. Ее MIC были 2,0 мг/мл против Streptococcus pneumoniae, 3,0 мг/мл против Streptococcus pyogenes, Vibrio parahaemoliticus, Bacillus cereus, Bacillus subtilis АТСС6633 и Candida sp. и 4,0 мг/мл против Staphylococcus aureus и Yersinia enterocolitica. Было показано, что 3-гидроксипиридин имел активность против Streptococcus pneumoniae, Streptococcus pyogenes, Staphylococcus aureus, Yersinia enterocolitica, Pseudomonas aeruginosa и Candida sp. Его MIC были 4,0 мг/мл против Streptococcus pneumoniae, Streptococcus pyogenes, Staphylococcus aureus, Yersinia enterocolitica, Pseudomonas aeruginosa и Candida sp. Было показано, что п-гидроксибензальдегид имел активность против многих типов бактерий, т.е. Streptococcus pneumoniae, Streptococcus pyogenes, Staphylococcus aureus, Escherichia coli, Salmonella sp., Yersinia enterocolitica, Vibrio parahaemolyticus, Pseudomonas aeruginosa, Bacillus cereus, Bacillus subtilis МВ-32, Bacillus subtilis АТСС6633 и Candida sp. В частности, п-гидроксибензальдегид показал сильную активность против Yersinia enterocolitica и его MIC против Yersinia была равна 0,5 мг/мл. Было показано, что ванилин имел активность против Streptococcus pneumoniae, Streptococcus pyogenes, Staphylococcus aureus, Escherichia coli, Salmonella sp., Yersinia enterocolitica, Vibrio parahaemolyticus, Bacillus cereus, Bacillus subtilis МВ-32, Bacillus subtilis АТСС6633 и Candida sp. Ванилин имел также активность против многих типов бактерий. В частности, среди них, ванилин показал сильную активность против Yersinia enterocolitica, и его MIC против Yersinia была равна 0,5 мг/мл. Способ бумажных дисков В качестве бактерицидного тест-способа для 5,7,4'-тригидрокси-3',5'-диметоксифлавона использовали способ бумажных дисков, при помощи которого бактерицидная активность могла оцениваться даже в случаях, когда растворитель имел некоторые действия. В способе бумажных дисков готовят растворы пробы, имеющие различную концентрацию пробы, и раствор пробы абсорбировался в специальный бумажный диск с последующим высушиванием этого бумажного диска. На чашку, которую готовят смешиванием приготовленной бактериальной суспензии с агаровой средой, помещают бумажные диски. Если проба имеет бактерицидную активность, кольцо ингибирования, которое показывает ингибирование бактериального роста, образуется таким образом, что центр этого кольца совпадает с этим бумажным диском. Степень бактерицидной активности оценивают на основе размера кольца ингибирования. Сначала 4 мг пробы 5,7,4'-тригидрокси-3',5'-диметоксифлавона растворяли в 200 мкл для приготовления раствора пробы 20 мг/мл. К 100 мкл этого раствора пробы 20 мг/мл добавляли 100 мкл стерилизованной воды для приготовления 200 мкл раствора пробы 10 мг/мл. К этому раствору добавляли 60 мкл ДМСО и 140 мкл стерилизованной воды для приготовления 400 мкл раствора пробы 5,0 мг/мл. ДМСО использовали в концентрации 40%, так как эта проба осаждалась из 30% ДМСО. К 350 мкл раствора пробы 5,0 мг/мл добавляли 140 мкл ДМСО и 210 мкл стерилизованной воды для приготовления 700 мкл раствора пробы 2,5 мг/мл. Таким же образом готовили растворы проб 1,25 мг/мл и 0,625 мг/мл. В качестве контроля готовили раствор, содержащий 40% ДМСО и 60% стерилизованной воды. В качестве контроля для сравнения готовили водные растворы катехина, имеющие вышеописанные концентрации. В бумажном диске (с диаметром 8,12 мм) абсорбировали каждый из этих растворов, и эти бумажные диски сушили в течение одного дня. В качестве тестируемых бактерий использовали Staphylococcus aureus, Salmonella sp., Yersinia enterocolitica, Pseudomonas aeruginosa и Candida sp. Эти бактерии смешивали с 2 мл стерилизованной воды для приготовления бактериальных суспензий, имеющих мутность 1 (108/мл). Агар чашек готовили смешиванием 0,2 мл бактериальной суспензии с 19,8 мл среды BHI. Высушенный бумажный диск помещали на агар чашки и эту чашку инкубировали в термостате при 37°С с последующей оценкой активности. Эти результаты показаны в таблице 7. В этой таблице (-) обозначает, что не наблюдалась бактерицидная активность. Эти результаты показывают, что 5,7,4'-тригидрокси-3',5'-диметоксифлавон имел бактерицидную активность против Salmonella sp. и Pseudomonas aeruginosa. Его бактерицидная активность была очень сильной даже в сравнении с катехином. Горячий водный экстракт листа Кумазаса (Sa, 2,3 кг) экстрагировали этилацетатом с получением растворимой в этилацетате фракции (Sa-1, 78 г). Бактерицидный тест против Staphylococcus aureus выявил, что бактерицидная активность распределялась в растворимой в этилацетате фракции (Sa-1). Растворимую в этилацетате фракцию (Sa-1) фракционировали на 7 фракций с использованием колоночной хроматографии на нейтральном силикагеле. Эти 7 фракций были названы Sa-1-А (90 мг), Sa-1-В (250 мг), Sa-1-С (3,36 г), Sa-1-D (3,00 г), Sa-1-Е (110 мг), Sa-1-F (1,56 г) и Sa-1-G (30,0 г), соответственно. Фракцию Sa-1-С (3,36 г) разделяли на два слоя добавлением к ней хлороформа и н-гексана с получением Sa-1-С(1) (2,22 г) и Sa-1-С(2) (1,14 г). Sa-1-С(1) (2,22 г) фракционировали с использованием колоночной хроматографии на нейтральном силикагеле с получением Sa-1-С(1)-а и Sa-1-С(1)-b. Sa-1-С(1)-а фракционировали с использованием препаративной колонки ODS для высокоэффективной жидкостной хроматографии (ВЖХ) с получением 60 мг белого твердого вещества (Sa-1-С(1)-аа). Данные спектров и анализ при помощи ВЖХ выявил, что это белое твердое вещество Sa-1-С(1)-аа было ванилином. Sa-1-С-(1)-b фракционировали опять с использованием колоночной хроматографии на нейтральном силикагеле с получением Sa-1-С(1)-ba, и этот Sa-1-С(1)-ba подвергали препаративной ТСХ с получением 86 мг светло-желтого твердого вещества (Sa-1-С(1)-baa). Данные спектров выявили, что это светло-желтое твердое вещество (Sa-1-С(1)-baa) было п-гидроксибензальдегидом. Далее, Sa-1-С(2) (1,14 г) подвергали перекристаллизации два раза с получением 478 мг светло-желто-зеленого твердого вещества (Sa-1-С(2)-а). Данные спектров выявили, что это светло-желто-зеленое твердое вещество (Sa-1-С(2)-а) было транс-п-кумаровой кислотой. Затем Sa-1-F (1,56 г) разделяли на растворимую в ацетоне фракцию Sa-1-F(1) (162 мг) и не растворимую в ацетоне фракцию Sa-1-F(2) (1,40 г). Опять добавляли ацетон к Sa-1-F(1) (162 мг) и жидкий слой разделяли с получением 10 мг желтого твердого вещества (Sa-1-F(1)-а). Данные спектров выявили, что это желтое твердое вещество Sa-1-F(1)-a) было 5,7,4'-тригидрокси-3',5'-диметоксифлавоном. Далее, Sa-1-F(2) (1,40 г) подвергали колоночной хроматографии на нейтральном силикагеле с получением 46 мг светло-желтого твердого вещества Sa-1-F(2)-a). Данные спектров выявили, что это светло-желтое твердое вещество было 3-гидроксипиридином: Бактерицидную активность ванилина, п-гидроксибензальдегида, транс-кумаровой кислоты и 3-гидроксипиридина испытывали при помощи способа разведения с использованием агара. В результате было подтверждено, что ванилин, п-гидроксибензальдегид, транс-кумаровая кислота и 3-гидроксипиридин имели бактерицидную активность. Среди них ванилин и п-гидроксибензальдегид показывали сильную бактерицидную активность против Yersinia enterocolitica, бактерии-возбудителя пищевого отравления. Для бактерицидного тестирования 5,7,4'-тригидрокси-3',5'-диметоксифлавона использовали способ бумажных дисков. В результате 5,7,4'-тригидрокси-3',5'-диметоксифлавон показал бактерицидную активность против Salmonella sp. и Pseudomonas aeruginosa. Его активность была очень сильной даже в сравнении с катехином. Автор данного изобретения пытался экстрагировать вышеописанные эффективные компоненты из растений, других, чем Кумазаса. В результате было показано, что 5,7,4'-тригидрокси-3',5'-диметоксифлавон (трицин) существовал в изобилии во многих растениях, принадлежащих к семейству Gramineae, например в растении риса (рисе), пшенице, кукурузе, ячмене, ржи, сахарном тростнике, бамбуке (Take), Японской пампасной траве, пампасной траве, тростнике (также называемом Phragmites или Yoshi) и т.д. Конкретными названиями растений являются следующие названия: растение риса, пшеница, ячмень, Avena fatua, рожь, просо, просо итальянское, просо японское, кукуруза, просо пальчатое, сорго, Take, дикий рис (Makomo), сахарный тростник, куикс (слезы Иовы), тростник, Японская пампасная трава, Sasa (бамбук), Arundo donax, Cortaderia argentea и газонная трава. Семейство Gramineae Подсемейство Bambusioideae (Семейство Bambusaceae) Род Bambusa: Houraichiku (Bambusa multiplex (Lour.) Raeusch.), Houraichiku (Bambusa multiplex (Lour.) Raeusch. ex J.A. et J.H. Schult. Род Shibataea: Okamezasa (Shibataea kumasasa (Zoll. ex Steud.) Nakai Род Phyllostachys: Mousouchiku (Phyllostachys heterocycla (Carriere) Matsum.), Madake (Phyllostachys bambusoides Sieb. et Zucc.), Hachiku (Phyllostachys nigra (Lodd. ex Loud.) Munro var. henonis (Bean) Stapf ex Rendle) Род Semiarundinaria: Narihiradake (Semiarundinaria fastuosa (Mitford) Makino ex Nakai), Yashyadake (Semiarundinaria yashadake (Makino) (далее относится к Take) Род Pleioblastus: Nezasa (Pleioblastus argenteostriatus (Regel) Nakai f. glaber (Makino) Murata), Azumanezasa (Pleioblastus chino (Franch. Et Sav.) Makino), Medake (Pleioblastus Simonii (Carr.) Nakai), Ryukyuchiku (Pleioblastus linearis (Hack.) Nakai) Род Pseudosasa: Yadake (Pseudosasa japonica (Siebold et Zucc. ex Steud.) Makino ex Nakai), Yakushimadake (Pseudosasa owatarii (Makino) Makino ex Nakai) Род Sasamorpha: Suzutake (Sasamorpha borealis (Hack.) Nakai) Род Arundrinaria: Azumazasa (Arundrinaria ramose Makino), Suekozasa (Arundrinaria ramose Makino var. suwekoana (Makino) Murata) Род Sasa: (Miyakozasa (Sasa nipponica (Makino) Makino et Shibata), Chimakizasa (Sasa palmate (Lat.-Marl. ex Burb.) E.G. Camus), Kumazasa, Chichimazasa (Sasa kurilensis (Rupr.) Makino et Shibata) (далее упоминаемый в отношении Sasa) Подсемейство Poelideae Род Agropyron: Shibamugi (пырей ползучий, Agropyron repens (L.) P. Beauv.), Kamojigusa (пырей, Agropyron tsukushiense (Honda) Ohwi var. transiens (Hack.) Ohwi, Aokamojigusa (Agropyron ciliare (Trin.) Franch. Var. minus (Miq.) Ohwi) Род Alopecurus: Suzumeno-teppou (Alopecurus aequalis Sobol. var. amurensis (Kom.) Ohwi), Setogaya (Alopecurus japonicus Steud.) Род Arundo: Danchiku (Arundo Donax L.) Род Briza: Kobansou (трясунка средняя, Briza maxima L.), Himekobansou (Briza minor L.) Род Bromus: Suszumeno-chahiki (костер, Bromus japonicus Thunb.), Inumugi (Bromus catharticus Vahl) Род Dactylis: Kamogaya (ежа сборная, Dactylis glomerata L.) Род Eragrostis: Kazekusa (полевичка) (Eragrostis ferruginea (Thunb.) P. Beauv.), Suzumegaya (Eragrostis cilinensis (All.) Link ex Janchen), Shinadare-suzumegaya (Eragrostis curvula (Schrad.) Nees), Niwahokori (Eragrostis multicaulis Steud.) Род Hordeum: ячмень, Mugikusa (ячмень заячий, Hordeum murinum L.) Род Truticum: пшеница Род Lolium: Hosomugi (плевел многолетний (райграсс английский, Lolium perenne L.), Nezumimugi (райнграсс итальянский, Lolium multiflorum Lam.), Dokumugi (плевел опьяняющий, Lolium temulentum L.) Род Poa: Susumeno-katabira (мятлик однолетний, Poa annua L.), Ichigotsunagi (мятлик, Poa ochotensis Trin.) Род Festuca: Naginatagaya (Festuca myuos L.), Ushinokegusa (овсяница, Festuca ovina L.), Toboshigara (Festuca parvigluma Steud.) Род Glyceria: Mutsuoregusa (Glyceria acutiflora Torr. subsp. japonica T.Koyama et Kawano), Dojoutsunagi (Glyceria ischyroneura Steud.) Род Melica: Michischiba (Melica onoei Franch. et Sav., Komegaya )Melica nutans L.) Род Lophatherum: Sasakusa (Lophatherum gracile Brongn.) Род Leptochloa: Azegaya (Leptochloa chinensis (L.) Nees) Род Beckmannia: Kazunokogusa (Beckmannia syzigachne (Steud.) Fernald) Род Sporobolus: Nezumino-o (Sporobolus fertilis (Steud.) Clayton), Higeshiba (Sporobolus japonicus (Steud.) Maxim. Ex Rendle) Род Eleusine: Ohishiba (Eleusine indica (L.) Gaertn.), Shikokubie (просо пальчатое, Eleusine coracana (L.) Gaertn.) Род Cynodon: Gyougishiba (свинорой пальчатый, бермудская трава, Cynodon dactylon (L.) Pers.) Род Phragmites: Urahagusa (Hakonechloa macra (Munro ex S.Moore) Makino ex Honda), тростник, Tsuruyoshi (Phragmites japonica Steud.) Род Phaenosperma Род Leersia Род Oryza: растение риса Род Zizania: Makomo (дикий рис, Zizania latifolia (Griseb.) Turcz. ex Stapf) Род Avena: Karasumugi (Avena fatua L.), овес (Avena sativa L.) Род Deshampsia: Komesusuki (Deshampsia flexuosa (L.) Nees), Hirohano-komesusuki (Deshampsia cespitosa (L.) P.Beauv. var. festucifolia Honda) Род Trisetum: Kanitsurigusa (Trisetum bifidum (Thund.) Ohwi), Rishirikanitsuri (Trisetum spicatum (L.) K.Richt. subsp. alascanum (Nash) Hulten) Род Koeleria: Minoboro (Koeleria cristata (L.) Pers.) Род Hierochloe: Koubou (Hierochloe glabra Trin. subsp. sachalinensis (Printz) Tzvelev), Miyamakoubou (Hierochloe alpina (Sw.) Roem. et Schult) Род Phalaris: Kusayoshi (двукисточник тростниковый, Phalaris arundinacea L.), canary-kusayoshi (канареечник канарский, Phalaris canariensis L.) Род Agrostis: Konukagusa (полевица белая, Agrostis gigantea Roth), Nukabo (Agrostis clavata Trin. subsp. matsumurae (Hack ex Honda) Tateoka) Род Polypogon Род Phleum: Awagaeri (Phleum paniculatum Huds.), Ooawagaeri (тимофеевка луговая, Phleum pretense L.) Род Calamagrostis: Nogariyasu (Calamagrostis brachytricha Steud.), Hossugaya (Calamagrostis pseudophragmites (Hallier f.) Koeler), Yama-awa (Calamagrostis epigeios (L.) Roth) Род Zoysia: Shiba (газонная трава, Zoysia japonica Steud.), Kouraishiba (Zoysia tenuifolia auct. Non Willd. ex Trin.), Onishiba (Zoysia macrostachya Franch. Et Sav.), Nagamionishiba (Zoysia sinica Hance var. nipponica Ohwi) Подсемейство Panicoideae Род Arundinella Род Eulalia: Un-nuke (Eulalia speciosa (Debeaux) Kuntze), Un-nuke-modoki (Eulalia quadrinervis (Hack.) Kuntze) Род Isachne: Chigozasa (Isachne globosa (Thunb.) Kuntze), Haichigozasa (Isachne nipponensis Ohwi) Род Panicum: Kibi (просо культурное, Panicum miliaceum L.) Haikibi (Panicum repens L.), Nukakibi (Panicum bisulcatum Thunb.) Род Echinochloa: Hie (просо японское, Echinochloa esculenta (A. Braun) H. Scholz), Inubie (Echinochloa crus-galli (L.) Beauv. Var. crus-galli) Род Oplismenus: Chijimizasa (Oplismenus undulatifolius (Ard.) Roem. Et Schult.) Род Setaria: Sasakibi (Setaria palmifolia (J.Koenig) Stapf), Enokorogusa (щетинник, просянка, Setaria viridis (L.) P.Beauv.), Awa (щетинник итальянский, просо итальянское, Setaria italica P.Beauv.), Kin-enokoro (Setaria pumila (Poir.) Roem. Et Schult.) Род Paspalum: Suzumenohie (Paspalum thunbergii Kunth ex Steud.), Kisyuusuzumenohie (Paspalum distichum L.), Shima-suzumenohie (паспалум расширенный, Paspalum dilatatum Poir.) Род Digitaria: Mehishiba (Digitaria ciliaris (Retz.) Koeler), Akimehishiba (Digitaria violascens Link) Род Pennisetum: Chikarashiba (Pennisetum alopecuroides (L.) Spreng.), слоновая трава (Pennisetum purpureum Schumach.) Род Spinifex: Tsukiige (Spinifex littoreus (Burm.f.) Merr.) Род Saccharum: сахарный тростник (Saccharum officinarum L.), Waseobana (Saccharum spontaneum L. var. arenicola (Ohwi) Ohwi) Род Imperata: Chigaya (Imperata cylindrical (L.) Raeusch.) Род Eccoilopus: Aburasusuki (Eccoilopus cotulifer (Thund.) A.Camus) Род Miscanthus: Susuki (японская пампасная трава, Miscanthus sinensis Andersson), Ogi (Miscanthus sacchariflorus (Maxim.) Benth.), Tokiwasusuki (Miscanthus floridulus (Labill.) Warb. ex K.Schum. et Lauterb.), Kariyasu (Miscanthus tinctorius (Steud.) Hack.) Род Microstegium: Sasagaya (Microstegium japonicum (Miq.) Koidz.), Ashiboso (Microstegium vimineum (Trin.) A.Camus) Род Pogonatherum: Itachigaya (Pogonatherum crinitum (Thunb.) Kunth) Род Dimeria: Karimatagaya (Dimeria ornithopoda Trin.) Род Hemarthria: Ushinoshippei (Hemarthria sibirica (Gandog.) Ohwi), Kobano-ushinoshippei (Hemarthria compressa (L.f.) R.Br.) Род Phacelurus: Aiashi (Phacelurus latifolius (Steud.) Ohwi) Род Ischaemum: Kamonohashi (Ischaemum aristatum L. var. crassipes (Steud.) Yonek.), Kekamonohashi (Ischaemum anthephoroides (Steud.) Miq.) Род Arthraxon: Kobunagusa (Arthraxon hispidus (Thund.) Makino) Род Cymbopogon: Ogarukaya (Cymbopogon tortilis (J.Presl) Hitchc. var. goeringii (Steud.) Hand.-Mazz.) Род Bothriochloa: Hime-aburasusuki (Capillipedium parviflorum (R.Br.) Stapf) Род Schizoachyrium: Ushikusa Schizoachyrium brevifolium (Sw.) Nees ex Buse) Род Andropogon: Meriken-karukaya (Andropogon virginicus L.) Род Themeda: Megarukaya (Themeda triandra Forssk. var japonica (Willd.) Makino) Род Sorghum: сорго (Sorghum bicolor (L.) Moench), Sato-morokoshi (Sorghum bicolor (L.) Moench 'Dulciusculum', Seiban-morokoshi (Sorghum halepense (L.) Pers.), суданская трава (Sorghum x drummondii (Nees ex Steud.) Millsp. et Chase) Род Coix: Juzudama (Coix lacryma-jobi L.), Hatomugi (коикс, слезы Иовы, Coix lacryma-jobi L. var. ma-yuen (Roman.) Stapf) Род Zea: кукуруза Трицин может быть выделен и очищен подверганием листа, стебля или тому подобного вышеописанных растений экстракции подходящим растворителем и с использованием способов разделения и очистки, таких как ВЖХ. Например, трицин может быть очищен концентрированием водного экстракта, экстракцией сухого остатка спиртом или водным спиртом (например, метанолом, этанолом, водным метанолом или водным этанолом), растворением этого сухого твердого вещества в воде и распределением полученного раствора с использованием этилацетата. В 50 мл различных органических растворителей погружали 5 г высушенных листьев Кумазаса и полученную смесь оставляли стоять с последующим концентрированием этого жидкого экстракта с получением сухого вещества. Отношение (доля) этого сухого вещества в различных жидких экстрактах и отношение (доля) трицина в полученном сухом веществе, при принятии массы листа Кумазаса за 100, показаны в таблице ниже. Растворитель Доля содержания сухого вещества в экстракте (%) Доля трицина в содержании сухого вещества в экстракте (%) Этанол 4,20,048 Метанол 11,70,035 н-Бутанол 2,40,057 Изопропанол 2,20,070 Этилацетат 1,90,065 Ацетон 1,80,095 Гексан 1,30Затем 50 г листа Кумазаса экстрагировали 1 л растворителя и этот растворитель в экстракте выпаривали с получением сухого остатка. Количество трицина (мг), содержащегося в этом сухом веществе, измеряли. Результаты показаны в таблице ниже. Растворитель Доля трицина в содержании сухого вещества (мг) Этанол2,02 Метанол 4,10н-Бутанол 1,37 Изопропанол1,54 Этилацетат 1,62 Ацетон1,71 Гексан 0В 500 мл метанола погружали 50 г листьев Кумазаса и полученную смесь оставляли стоять. После этого смесь фильтровали и растворитель в фильтрате выпаривали с получением 5,05 г в экстракте метанолом. Операцию распределения проводили с использованием гексана, хлороформа, этилацетата и н-бутанола в указанном порядке. Измеряли количество сухого вещества и количество трицина в нем. Эти результаты показаны в таблице ниже. РастворительДоля содержания сухого вещества в экстракте (%) Доля трицина в содержании сухого вещества в экстракте (%) Гексан 17,60 Хлороформ 4,70,61 Этилацетат 6,90,09 н-Бутанол 38,40 Водный слой 33,30Затем 50 г листьев Кумазаса экстрагировали 500 мл метанола. Растворитель в экстракте выпаривали и полученный осадок растворяли в воде с последующей операцией распределения с использованием различных растворителей. Измеряли количество трицина в полученном содержании сухого вещества. Эти результаты показаны в таблице ниже. Растворитель Доля трицина в содержании сухого вещества (%) Гексан0 Хлороформ 3,35Этилацетат 0,73 н-Бутанол0 Водный слой 0Различные экстракты, полученные с использованием водного этанола, листьев Кумазаса, концентрировали досуха с получением содержания сухого вещества (В). После растворения этого сухого вещества (В) в воде проводили операцию распределения с использованием этилацетата, и этот растворитель в полученном экстракте выпаривали с получением содержания сухого вещества (С). Доля содержания сухого вещества (С) в этилацетатном экстракте, при принятии содержания сухого вещества (В) за 100, показана в таблице ниже. Результаты анализа на трицин (в мас.%) в содержании сухого вещества (В) и в содержании сухого вещества (С) также показаны в этой таблице. Доля спирта в водном спирте (мас.%) Содержание сухого вещества (В) (мас.%) Трицин в (В) (мас.%) Содержание сухого вещества (С) (мас.%) Трицин в (С) (мас.%) 0*62,0 0,0255,5 0,385 3,0 0,0107,7 0,05710* 51,6 0,0317,1 0,2915 3,1 0,04311,1 0,1225 3,2 0,1512,2 0,7730* 55,4 0,09211,4 0,8070 4,9 0,3026,5 1,190 3,9 0,4533,3 0,95100* 23,8 0,1137,4 0,51 * Проводили предварительное концентрированиеГотовили различные экстракты с использованием водного этанола (D) листа или стебля тростника и листа бамбука (Take) и растворитель этих экстрактов выпаривали с получением содержания сухого вещества (Е). Это сухое вещество (Е) растворяли в воде и проводили операцию распределения с использованием этилацетата с получением содержания сухого вещества (F) в растворимой в этилацетате части. Анализировали количество трицина в содержании сухого вещества (Е) и в содержании сухого вещества (F) при использовании 100 г содержания сухого вещества (Е). Эти результаты показаны в таблице ниже. Экстракт DКоличество трицина в 100 г содержания сухого вещества (Е) (мг) Количество трицина в 100 г содержания сухого вещества (F) (мг) Лист тростника (25% этанол)31 45,8 Стебель тростника (25% этанол) 2819,6 Лист Take (70% этанол) 110 64,0Лист Take (90% этанол) 150109,2Бактерицидная композиция по данному изобретению Бактерицидный агент согласно данному изобретению, который содержит в качестве эффективного ингредиента по меньшей мере одно соединение, выбранное из вышеописанных соединений (ванилин, п-гидроксибензальдегид, транс-п-кумаровая кислота, 3-гидроксипиридин, 5,7,4'-тригидрокси-3',5'-диметоксифлавон), называемых здесь «соединениями согласно изобретению», может быть использован в различных формах. Например, этот агент согласно данному изобретению пригоден для защищающей слизистую оболочку композиции, профилактической и/или терапевтической композиции для бактериальной инфекции, в качестве предохраняющего агента и бактерицидного агента для аппарата фильтрации или т.п. Бактерицидный агент по данному изобретению может быть приготовлен в форме жидкости, твердого вещества или газа. Бактерицидный агент по данному изобретению может вводиться перорально или парентерально. Примеры форм перорального введения включают в себя таблетки, шарики, порошки, жидкости и пищевые формы, такие как жевательные резинки, конфеты, шоколадки, хлеб, печенье, японскую лапшу с добавлением гречневой муки, японскую лапшу из пшеничной муки, различные препараты для приготовления напитков и т.п. Примеры парентеральных форм введения включают в себя инъекционные растворы, формы для местного введения (такие как кремы, мази), суппозитории и т.п. Примеры готовых форм для местного введения включают в себя носители, такие как марли, изготовленные из природных или синтетических волокон, в которые импрегнирован бактерицидный агент согласно данному изобретению, и косметические средства, такие как губные помады и тому подобное, в которые включен бактерицидный агент согласно данному изобретению. Бактерицидный агент согласно данному изобретению может быть применим в качестве бактерицидного агента не только для человека, но также для других животных, таких как млекопитающие, птицы, рыбы, пресмыкающиеся и т.д. Таким образом, агент согласно данному изобретению может быть использован в качестве бактерицидного агента для этих животных (например, в качестве фармацевтического агента для домашних животных, их корма или т.п.). Кроме того, бактерицидный агент согласно данному изобретению применим в качестве агента для различных растений, а также животных, а также применим в качестве консерванта. Для получения бактерицидного агента согласно данному изобретению в различных готовых формах могут быть использованы такие материалы-основы как масляные компоненты, используемые в обычных фармацевтических композициях, косметических средствах, композициях для кожи и тому подобном; увлажнители; консерванты и тому подобное, наряду с предписанным количеством вышеописанного соединения. Вода, используемая для бактерицидного агента, не ограничивается, и она может быть водопроводной водой, природной водой, очищенной водой или т.п. Обычно используют предпочтительно воду с высокой чистотой, например воду, подвергнутую ионному обмену. Примеры масляного компонента включают в себя животные жиры, такие как сквалан, говяжий жир, лярд (свиной жир), лошадиный жир, ланолин, пчелиный воск и тому подобное; растительные масла, такие как оливковое масло, виноградное масло, пальмовое масло, масло хохоба, масло из зародышей семян (например, масло из зародышей семян риса) и тому подобное; синтетические масла, такие как жидкий парафин, эфир высших жирных кислот (например, октилпальмитат, изопропилапальмитат, октилдодецилмиристат), силиконовое масло и т.п.; и полусинтетические масла. Два или более из этих масляных компонентов используют подходящим образом в комбинации в зависимости от того, что является желательным, например защита кожи, смягчающее действие (для покрытия поверхности кожи тонким слоем для защиты кожи от высыхания и придания коже нежности и эластичности), легкая консистенция и т.д. Одним из предпочтительных примеров является комбинация сквалана, оливкового масла и октилдодецилмиристата. Для придания твердости и/или текучести бактерицидному агенту могут быть также использованы твердые жиры, такие как стеариновая кислота, стеариловый спирт, бегеновая кислота, цетанол, вазелин и т.п. Предпочтительно используют стеариновую кислоту и цетанол в комбинации. Для приготовления бактерицидного агента согласно данному изобретению в виде композиции крема используют кремообразующий агент, который делает смесь соединения согласно данному изобретению, воды и масляного агента кремообразной. Кремообразующий агент не ограничивается, и обычно используют комбинацию глицерилмоностеарата и самоэмульгирующегося глицерилмоностеарата (смесь глицерилмоностеарата и эмульгатора). Бактерицидный агент согласно данному изобретению может содержать (а) стабилизатор (стабилизаторы), увлажнитель (увлажнители), агент (агенты) для заживления ран, консервант (консерванты), поверхностно-активное вещество (поверхностно-активные вещества) или т.п. Примеры стабилизатора включают в себя комбинацию карбоксивинильного полимера и гидроксида калия, полиэтиленгликольдистеарата и т.п. В частности, предпочтительным является полиэтиленгликольсесквистеарат (смесь 1:1 полиэтиленгликольдистеарата и полиэтиленгликольмоностеарата) (молекулярная масса полиэтиленгликоля равна 1000-20000), так как он имеет высокую стабильность, и композиция, содержащая его, не разделяется на воду и масло, и, кроме того, он эффективно придает твердость композиции крема, который наносят на кожу. Примеры увлажнителя включают в себя гиалуронат натрия, коллаген, экстракт алоэ (особенно предпочтительным является экстракт алоэ (2), полученный из Aloe arborescens var. natalensi), мочевину, 1,3-бутиленгликоль, глицерин, трегалозу, сорбит, аминокислоту, пирролидонкарбоксилат и т.п. Примеры агента для заживления ран включают в себя аллантоин, динатрийглицирризинат, экстракт солодки, экстракт Artemisia и т.п. Консерванты используют необязательно, так как соединение этого изобретения само обладает бактерицидным действием. Примеры консерванта включают в себя бензоат натрия, низшие алкиловые эфиры пара-гидроксибензойной кислоты (например, эфиры, называемые парабенами, такие как метиловый, этиловый, пропиловый или бутиловый эфир), пропионат натрия, смешанный эфир жирных кислот (смесь глицерилкапрата, полиглицерил-2-лаурата и полиглицерил-10-лаурата), феноксиэтанол, светочувствительный пигмент Примеры поверхностно-активного вещества включают в себя N-ацил-L-глутамат натрия, полиоксиэтиленсорбитанмоностеарат и т.п. Кроме того, если требуется, могут содержаться ароматизирующие компоненты, такие как (эфирное) апельсиновое масло, (эфирное) лимонное масло, (эфирное) масло горького апельсина, вкусовые агенты и т.п. Защищающая слизистую оболочку композиция, профилактическая и/или терапевтическая композиция для бактериальной инфекции, которые содержат бактерицидный агент согласно данному изобретению, являются агентами, которые эффективно подавляют инвазию инфекционных агентов в тело через слизистую оболочку глаза, носа, глотки, уха, ануса, половых органов или т.п. и через раны и кожу и предотвращают и/или лечат посредством этого бактериальную инфекцию, в том числе нозокомиальную инфекцию. Более конкретные примеры защищающей слизистую оболочку композиции и профилактической и/или терапевтической композиции для бактериальной инфекции включают в себя защищающие слизистую оболочку ткани и композиции для применения для полости рта. Защищающая слизистую оболочку ткань является пропускающим воздух носителем, в котором бактерицидный агент согласно данному изобретению включен таким способом, как импрегнация, опрыскивание или тому подобное, где этот пропускающий воздух носитель является, например, природными волокнами, такими как шелк, хлопок, конопля и тому подобное, синтетическими волокнами, такими как полиуретан, полиэтилен, полипропилен, найлон, полиэфир, акрил и тому подобное, полусинтетическими волокнами или смешанными волокнами из двух или более этих волокон; или пряжей, тканным материалом, трикотажной тканью, нетканым материалом или бумагой из этих волокон. Термин «защитная (протективная) ткань» включает в себя, в данном контексте, не только ткани, но также и волокна per se, пряжи, бумагу, для удобства. Конкретные примеры формы защищающей слизистую оболочку ткани включают в себя не только защитные ткани, непосредственно контактирующие со слизистой оболочкой или кожей, которые классифицируются как санитарные (гигиенические) продукты, такие как марля, маски, глазные пластыри, гигиенические пояса, гигиенические салфетки, бандажи, туалетная бумага, марля для обработки геморроя, ушные тампоны, бандажи для жидкости и тому подобное, но также и изделия, контактирующие прямо или опосредованно с кожей, например такие ткани, как белые одежды и тому подобное; малые изделия из ткани, такие как перчатки, шапочки, носки, японские носки и тому подобное; постельные принадлежности, такие как постельные простыни, покрывала, наволочки, изделия для постели и тому подобное; аксессуары интерьера и отделочные материалы интерьера, такие как занавески, обои, ковры и тому подобное; медицинские материалы, такие как хирургический шовный материал и т.п., и т.д. Примеры композиций для применения для полости рта, содержащих бактерицидный агент согласно данному изобретению, включают в себя камеди, желе, пастилки, кондированные изделия, жевательные резинки, таблетки, шарики, жидкости для промывания полости рта, полоскания рта, зубные пасты, пленки для нанесения на слизистую оболочку, аэрозоли для лечения фарингеального воспаления и т.п. Как показано в вышеописанных экспериментальных примерах, соединение согласно данному изобретению содержится в экстракте Кумазаса в концентрации приблизительно 1/1000-1/100000 относительно содержания сухого вещества в нем. Таким образом, в случаях, когда соединение согласно данному изобретению используют в качестве бактерицидного агента, это соединение может быть использовано в концентрации приблизительно 1/1000-1/100000 используемого количества сухого вещества экстракта Кумазаса. Эта концентрация может быть подходящим образом определена в зависимости от цели применения. Например, защищающая слизистую оболочку ткань, в которую включено соединение этого изобретения, может быть получена, например, импрегнированием защитной ткани в 2-20 × (1/1000-1/100000) мас.% растворе соединения согласно данному изобретению (в воде, органическом растворителе, таком как спирт или ДМСО или их смесь) или опрыскиванием защитной ткани 2-20 × (1/1000-1/100000) мас.% раствором соединения согласно данному изобретению и затем высушиванием ее. Количество соединения согласно данному изобретению, используемое в импрегнировании или опрыскивании, равно PPS приблизительно 2-20 × (1/1000-1/100000) мас.%, более предпочтительно приблизительно 6-15 × (1/1000-1/100000) мас.%, наиболее предпочтительно приблизительно 8-12 × (1/1000-1/100000) мас.% в расчете на сухое вещество соединения согласно данному изобретению. При включении соединения согласно данному изобретению в композиции для применения для полости рта, такие как камеди, желе, пастилки, кондированные изделия, жевательные резинки, таблетки, шарики (например, сасатан), жидкости для промывания полости рта, полоскания рта, зубные пасты, пленки для нанесения на слизистую оболочку и тому подобное, соединение согласно данному изобретению может быть добавлено к исходному материалу композиции для применения для полости рта в количестве приблизительно 2-20 × (1/1000-1/100000) мас.%, более предпочтительно приблизительно 6-15 × (1/1000-1/100000) мас.%, наиболее предпочтительно приблизительно 8-12 × (1/1000-1/100000) мас.% в расчете на сухое вещество соединения согласно данному изобретению в любой из стадий приготовления этой композиции для применения для полости рта. Обычно используемый компонент (обычно используемые компоненты) может быть подходящим образом смешан с композицией для применения для полости рта согласно данному изобретению, в зависимости от ее готовой формы. Примеры обычно используемого компонента включают в себя такие эксципиенты, как глюкоза, лактоза, сахароза, сироп крахмала, декстрин, циклодекстрин и тому подобное; связующие вещества, такие как аравийская камедь, натрийкарбоксиметилцеллюлоза, кристаллическая целлюлоза, гуммиоснова и тому подобное; дезинтегрирующие агенты, такие как крахмал и тому подобное; смазывающие вещества, такие как стеарат магния, эфиры сахарозы и жирных кислот и тому подобное; хладагенты, такие как ароматизаторы, хлорофилл, перечная мята, 1-ментол и т.п., и т.д. В случаях, когда защищающую слизистую оболочку композицию согласно данному изобретению используют в форме защитной ткани, соединение согласно данному изобретению может быть включено в часть защитной ткани (например, марли), с которой контактирует слизистая оболочка или рана, и эта защитная ткань может заменяться свежей тканью один-три раза в день. При использовании защищающей слизистую оболочку композиции в форме хирургического шовного материала инвазия бактерий через зашитую зону может быть эффективно подавлена и воспаление пораженной зоны может быть подавлено со стимуляцией нормализации оперируемого участка. При использовании защищающей слизистую оболочку композиции в форме защитной ткани для предотвращения нозокомиальной инфекции в больнице или тому подобного, действие защищающей слизистую оболочку композиции согласно данному изобретению в предотвращении инфекции продолжается в течение продолжительного времени. Если это действие уменьшается мытьем, защитная ткань может быть подходящим образом заменена, или может выполняться снова процесс включения соединения согласно данному изобретению в эту защищающую слизистую оболочку ткань. В случаях, когда защищающую слизистую оболочку композицию по данному изобретению используют в форме композиции для применения в полости рта, прием этой композиции является неограниченным, и соединение согласно данному изобретению может приниматься в количестве приблизительно 2-15 × (1/1000-1/100000) мг в расчете на сухое вещество, например один-пять раз в день, обычно один-три раза в день. Этот прием и число приемов может быть подходящим образом изменено в зависимости от цели. Защищающая слизистую оболочку композиция согласно данному изобретению содержит соединение согласно данному изобретению в количестве 2-20 × (1/1000-1/100000) мас.% в расчете на сухое вещество и имеет значительное бактерицидное действие даже против устойчивых бактерий, в отношении которых общепринятые антибиотики являются неэффективными. В случаях, когда защищающую слизистую оболочку композицию по данному изобретению используют в форме композиции для применения в полости рта, инфекции инфекционными бактериями могут быть предотвращены и их рост может быть подавлен очень просто помещением подходящим образом этой композиции в рот, если это требуется. Композиция пролонгированного высвобождения, такая как жевательная резинка, конфета или тому подобное, может проявлять свое действие в течение длительного времени, и, следовательно, такая форма является предпочтительной. Защищающая слизистую оболочку композиция согласно данному изобретению может быть использована в форме лосьонов или масел. Нанесением на кожу лосьона или масла, содержащего соединение согласно данному изобретению в количестве 2-20 × (1/1000-1/100000) мас.% в расчете на сухое вещество, могут быть предотвращены инфекции инфекционными бактериями и может быть очень просто подавлен их рост. Консерванты Кроме того, данное изобретение предоставляет консервант, содержащий в качестве эффективного ингредиента соединение согласно данному изобретению. Форма консерванта не является ограниченной. Примеры композиции, в которой используют консервант согласно данному изобретению, включают в себя пищевые продукты, питьевую воду, приправы, косметические средства (в том числе лосьоны и масла), аэрозоли для лечения ран, аэрозоли для лечения фарингеального воспаления и т.п. Эти композиции могут, соответственно, содержать соединение согласно данному изобретению в количестве 2 × (1/1000-1/100000) мас.%, более предпочтительно приблизительно 6-15 × (1/1000-1/100000) мас.%, наиболее предпочтительно приблизительно 8-12 × (1/1000-1/100000) мас.% в расчете на сухое вещество. Фильтрующее устройство Данное изобретение предоставляет также воздухоочистительное фильтрующее устройство в качестве эффективного ингредиента соединения согласно данному изобретению. Примеры конкретной формы этого устройства включают в себя фильтры, которые помещают на участок, через который проходит воздух, например фильтры, применимые в вентиляторах, кондиционерах воздуха, кондиционерах воздуха в машинах, отверстиях притока воздуха, вытяжных отверстиях, экранирующих дверях, воздухоочистителях и т.п. Материал, из которого состоит фильтр, не является ограничиваемым, и примеры этого материала включают в себя тканные материалы, трикотажные ткани, нетканые материалы, бумагу и тому подобное, которые изготовлены из природных волокон, таких как шелк, хлопок, конопля, и тому подобного, синтетических волокон, таких как полиуретан, полиэтилен, полипропилен, найлон, полиэфир, акрил, и тому подобных, полусинтетических волокон или смешанных волокон из двух или более этих волокон. Соединение согласно данному изобретению может быть включено в такой фильтр таким способом, как импрегнирование, опрыскивание или тому подобное, и этот фильтр может быть высушен. Количество соединения согласно данному изобретению, содержащееся в этом фильтре, равно предпочтительно 2-20 × (1/1000-1/100000) мас.%, более предпочтительно приблизительно 6-15 × (1/1000-1/100000) мас.%, наиболее предпочтительно приблизительно 8-12 × (1/1000-1/100000) мас.% в расчете на сухое вещество. Формула изобретения1. Бактерицидный агент, содержащий в качестве эффективного ингредиента 5,7,4 2. Бактерицидная композиция, содержащая бактерицидный агент по п.1. Популярные патенты: 2061349 Рама универсальной навесной сельскохозяйственной машины ... штанги, а задние концы их соединены между собой поперечной планкой, которая посредством гибкой связи и продольно-горизонтального кронштейна связана с основным брусом. К основному брусу параллельно штангам и независимо от них через съемные опоры крепятся рычаги подъема, поворотные относительно опор. На поперечной планке штанг установлено дополнительное опорное устройство. 1 з п.ф-лы, 5 ил. , , , , ОПИСАНИЕ ИЗОБРЕТЕНИЯ К ПАТЕНТУ Изобретение относится к сельскохозяйственному машиностроению, в частности, к машинам для поверхностной обработки почвы, посеву и посадки с.-х. культур. Известна универсальная с.-х. машина, обеспечивающая выполнение нескольких ... 2281637 Способ производства зеленого корма при возделывании в орошаемом земледелии и устройство для его осуществления ... 6,960,73112 Прямой высев79,39 71,2675,33 0,867,96 0,76102 Кукуруза Zea mays L. сорт Анна + редька масличная Raphanus sativus L. var olcifomis Pars. [ssp. oleifrra (D.S.)Metzg.] Совместный при смешивании семян 64,4151,14 57,7831,245,31 0,86173 Подсевной во второй срок посева59,92 64,4162,16 11,986,10 0,71124Прямой высев66,45 59,4962,915,67 6,420,67 112НСР05 8,457,59 -- --- Таблица 8Продуктивность позднелетних кормовых смесей, выращиваемых третьим урожаем, т/га (среднее за 2002 и 2003 годы) Культура, сорт, смесьЗеленая массаВыход Кормовых единицПереваримого протеина m/гана 1 к.е., гПосев и возделывание многокомпонентной кормовой смеси после озимых культур ... 2140738 Производные n-арилгидразина, способ их получения, способ подавления насекомых и композиция для подавления насекомых ... ... 2450505 Порционное устройство для вытирания семян трав ... Корпус 1 может быть выполнен Г- или С-образной формы, пустотелым в виде кожуха, закрывающего электродвигатель 6 и опирающегося на стакан 5 по типу блендера или иной формы. Для установки съемного стакана 5 в корпусе 1 выполнено посадочное кольцевое углубление 7 с горизонтальными штифтами 8. Стакан 5 является быстросъемным и служит заправочной емкостью. На верхней кромке стакана 5 расположены L-образные вырезы 9, служащие для установки его на штифты 8 в кольцевое углубление 7 корпуса 1. При этом форма стакана 5 может быть не только цилиндрической, но и иной, например, конической, расширяющейся кверху, для облегчения надевания его на ротор 3.Возможно исполнение быстросъемного ... 2498561 Способ тандемного возделывания сельскохозяйственных культур для повышения производства пищевых зерновых культур ... пшеницы и горчицы, хотя имели истоки в умеренной части мира, в настоящее время широко возделываются в регионах полу-умеренного климата использованием сортов, разработанных применением методик растениеводства. Было выполнено исследование для сорта пшеницы, подходящей для позднего посева, и сорта горчицы, обладающих признаком раннего созревания в регионах полу-умеренного климата. Предусматривалось, что такие разновидности хорошо будут реагировать на изменения в сезонной окружающей среде Индо-Гангских равнин адаптивным образом. Данное исследование привело к идентификации разновидности пшеницы, названной Pusa Gold [2], и разновидности горчицы Agrani [с коричневыми семенами], обе ... |
Еще из этого раздела: 2050099 Косилка с всасывающим устройством 2093022 Устройство для выпаивания животных 2288561 Устройство для предпосевной обработки семян растений 2452155 Лапа культиватора 2195808 Способ хранения корнеплодов, картофеля и капусты 2253239 Способ производства средства для обработки растений (варианты) 2495561 Машина лесозаготовительная 2076603 Способ повышения урожайности сельскохозяйственных культур 2488422 Сеть фильтров 2055465 Система приготовления и подачи питательного раствора в теплице |
Изобретения в сельском хозяйстве
Обработка почвы в сельском и лесном хозяйствах
Посадка, посев, удобрение
Уборка урожая, жатва
Обработка и хранение продуктов полеводства и садоводства
Садоводство, разведение овощей, цветов, риса, фруктов, винограда, лесное хозяйство
Новые виды растений или способы их выращивания
Производство молочных продуктов
Животноводство, разведение и содержание птицы, рыбы, насекомых, рыбоводство, рыболовство
Поимка, отлов или отпугивание животных
Консервирование туш животных, или растений или их частей
Биоцидная, репеллентная, аттрактантная или регулирующая рост растений активность химических соединений или препаратов
Хлебопекарные печи, машины и прочее оборудование для хлебопечения
Машины или оборудование для приготовления или обработки теста
Обработка муки или теста для выпечки, способы выпечки, мучные изделия
|
|
||
 -тригидрокси-3
-тригидрокси-3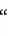 Sasa albo marginata Makino et Shibata
Sasa albo marginata Makino et Shibata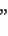 , и другие имеют названия, отличающиеся от этого названия. Кумазаса (Sasa albo marginata) растет в настоящее время почти по всей Японии, так как он искусственно культивируется.
, и другие имеют названия, отличающиеся от этого названия. Кумазаса (Sasa albo marginata) растет в настоящее время почти по всей Японии, так как он искусственно культивируется.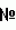 21 и 22, которые имели пятно в одном и том же положении согласно ТСХ, смешивали и полученную смесь концентрировали с получением концентрата (далее называемого
21 и 22, которые имели пятно в одном и том же положении согласно ТСХ, смешивали и полученную смесь концентрировали с получением концентрата (далее называемого 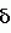 3,91 (с, 3Н), 6,94 (д, J=8,6 Гц, 1Н), 7,42 (д, J=8,6 Гц, 1Н), 7,43 (с, 1Н), 9,74 ((с, 1Н)
3,91 (с, 3Н), 6,94 (д, J=8,6 Гц, 1Н), 7,42 (д, J=8,6 Гц, 1Н), 7,43 (с, 1Н), 9,74 ((с, 1Н)