Раствор для перфузии и-или консервации органов и способы его примененияПатент на изобретение №: 2397641 Автор: ЯНГ Линдон Х. (US) Патентообладатель: ФИЛАДЕЛЬФИЯ КОЛЛЕДЖ ОФ ОСТЕОПЭТИК МЕДСИН (US) Дата публикации: 20 Февраля, 2009 Начало действия патента: 13 Января, 2006 Адрес для переписки: 119034, Москва, Пречистенский пер., 14, стр.1, 4 этаж, "Гоулингз Интернэшнл Инк.", Ю.В.Дементьевой Изображения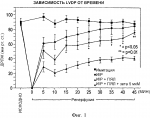    Настоящее изобретение относится к области фармацевтической промышленности, в частности к раствору для перфузии, консервации и/или реперфузии органов, особенно сердца, с целью трансплантации. Раствор содержит, по меньшей мере, один пептидный ингибитор протеинкиназы С ОБЛАСТЬ ИЗОБРЕТЕНИЯ Настоящее изобретение относится к раствору для консервирования, перфузии и/или реперфузии любого органа, особенно сердца, с целью трансплантации. Раствор содержит пептидный(ые) ингибитор(ы) протеинкиназы С бета II (ПКС ПРЕДПОСЫЛКИ СОЗДАНИЯ ИЗОБРЕТЕНИЯ Успеху трансплантации органов нередко препятствует их повреждение ввиду ишемии/реперфузии. Изолированные человеческие сердца, лишенные кислорода на более чем 4 часа, прогрессивно теряют жизнеспособность и часто не приживаются у реципиентов. Прочие органы, такие как почки, печень, поджелудочная железа и легкие, будучи удаленными из организма перед трансплантацией, также подвержены тканевому и клеточному повреждению. Причиной этого повреждения являются гипоксия и недостаток кровообращения, которые в физиологических условиях осуществляют поддержание необходимых концентраций кислорода и питательных веществ и устраняют токсические продукты метаболизма клеток. Трансплантаты органов чаще благополучно приживаются, если пересадка происходит немедленно после взятия органа. Последние научные достижения позволили увеличить частоту успешных пересадок органов и успешных операций на органах, например, таких как аортокоронарное шунтирование. Эти успешные хирургические вмешательства стали возможны благодаря появлению растворов для консервации и перфузии органов. Кроме того, усовершенствовались способы и устройства доставки перфузионного раствора к органу. Краткосрочная консервация миокарда в настоящее время осуществляется с помощью охлаждения после кардиоплегии. Тем не менее, существует множество способов, различающихся составом используемого раствора, температурой консервации и протокола введения. С целью защиты миокарда при операциях на сердце были разработаны различные растворы, останавливающие и консервирующие сердце. Примерами могут служить растворы Krebs-Henseleit, UW, St.Thomas II, растворы Collins и Stanford (см., например, патенты США Восстановление кровотока является первоочередной задачей при воздействии на органы и ткани, испытывающие длительную ишемию, например, при трансплантации. Тем не менее, реперфузия вызывает повреждение эндотелия и миоцитов, что приводит к органной дисфункции (Buerke и др., Am JPhysiol 266: Н128-136, 1994; Lucchesi и Mullne, Ann. Rev. Pharmacol. Toxicol. 26: 2011-2024, 1986; и Lucchesi и др., J.Mol. Cell. Cardiol. 21: 1241-1251, 1989). Последовательность событий, ассоциирующихся с реперфузионным повреждением, начинается с дисфункции эндотелия, которая характеризуется снижением базальной секреции клетками эндотелия оксида азота (NO) в течение первых 2.5-5 минут после восстановления кровотока (Tsao и Lefer, Am. J.phyiol. 259: Н1660-1666, 1990). Уменьшение высвобождения NO эндотелием ассоциируется с повышением концентрации молекул адгезии на мембранах эндотелиальных клеток и полиморфноядерных лейкоцитов (ПЯЛ) (Ma и др., Circ Res 72: 403-412, 1993; и Weyrich и др., J.Leuko. Biol. 57: 45-55, 1995). Это в свою очередь приводит к взаимодействию между ПЯЛ и эндотелием, которое имеет место через 10-20 минут после восстановления кровотока, с последующей инфильтрацией миокарда ПЯЛ, что можно наблюдать уже через 30 минут (Lefer и Hayward, B The Role of Nitric Oxide in Ischemia-Reperfusion: Contemporary Cardiology, Loscalzo и др. (Eds.), Humana Press, Totowa, NJ, pp.357-380, 2000; Lefer и Lefer, Cardiovadc. Res. 32: 743-751, 1996; T-sao и др., Circulation 82. 1402-1412, 1990; и Weyrich и соавт., J.Leuko. Biol. 57: 45-55, 1995). Из реперфузированной ткани высвобождаются молекулы хемотаксиса, которые вкупе с плазменными факторами активируют ПЯЛ, что способствует высвобождению из последних цитотоксических соединений (т.е., супероксид аниона) и усугубляет органную дисфункцию, следующую за ишемией/реперфузией (Lucchesi и др. L.Mol. Cell. Cardiol. 21: 1241-1251, 1989; Ma и др., Circ Res 69: 95-106, 1991; Tsao и др., Circulation 82: 1402-1412, 1990; и Tsao и др., Am Heart J.123: 1464-1471, 1992). Супероксид взаимодействует с NO с образованием пероксинитрит аниона и, таким образом, снижает биодоступность NO и усугубляет дисфункцию эндотелия и инфильтрацию ПЯЛ после ишемии/реперфузии миокарда (Clancey и др., J. Clin. Invest. 90: 1116-1121, 1992; Hansen, Circulation 91: 1872-85, 1995; Lucchesi и др., J.Mol. Cell. Cardiol. 21: 1241-1251, 1989; Rubanyi и Vanhoutte, Am LPhysiol 250: Н815-821, 1986; Tsao и др., Am Heart J123: 1464-1471, 1992; и Weiss, New Eng.J.Med. 320: 365-375, 1989). Таким образом, в настоящее время сохраняется потребность в более качественных растворах, которые могли бы увеличить время консервации трансплантируемого органа и защитить его от реперфузионного повреждения после ишемии, с тем чтобы орган мог должным образом функционировать после восстановления кровотока. СУЩНОСТЬ ИЗОБРЕТЕНИЯ Данное изобретение представляет собой раствор для консервации, перфузии и/или реперфузии органов, особенно сердца, содержащий пептидный(ые) ингибитор(ы) протеинкиназы С Данный раствор содержит около 5-10 µM пептидного ингибитора ПКС Данный раствор может быть использован как перфузионная среда или как консервирующий раствор. В качестве перфузионного раствора он вводится в сосудистое русло органа с целью защиты тканей и клеток. При использовании в качестве консерванта орган погружается в раствор целиком. Желательно, чтобы орган и перфузировался раствором, и был погружен в него. Далее, данный раствор также служит и раствором для реперфузии при восстановлении кровотока в органе после ишемии. Настоящее изобретение включает также способы использования данного раствора. К ним относятся способы консервации органа для трансплантации, способы защиты ишемизированного органа от повреждения, уменьшения степени органной дисфунции после ишемии, сохранения высвобождения оксида азота в ишемизированном органе и защиты изолированного от кровообращения органа от повреждения. КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ Фиг.1. Зависимость ДРЛЖ (давление, развиваемое левым желудочком = конечное систолическое давление в левом желудочке - конечное диастолическое давление в левом желудочке) от времени в сердцах-имитациях и сердцах крыс, перфузируемых в режимах И/Р (И/Р = ишемия/реперфузия), И/Р+ПЯЛ и И/Р+ПЯЛ+ПКС Фиг.2. Начальное и конечное ДРЛЖ, выраженное в мм рт.ст., развиваемое изолированными перфузируемыми сердцами крыс до ишемии (И) (исходно) и через 45 минут после реперфузии (Р) (конечное значение). Сердца перфузировались в присутствии или в отсутствии ПЯЛ. ПЯЛ вызывали значительную контрактильную дисфункцию, которая уменьшалась под действием пептидного ингибитора ПКС Фиг.3. Исходное и конечное максимальное ДРЛЖ (+dP/dt max), выраженное в мм рт.ст./с в изолированных перфузированных сердцах крыс до ишемии (И) и после реперфузии (Р). Сердца перфузировались в присутствии или в отсутствии ПЯЛ. ПЯЛ вызывали значительную контрактильную дисфункцию, которая уменьшалась под действием пептидного ингибитора ПКС Фиг.4а. Гистологическая оценка общего числа внутрисосудистых и инфильтрирующих ПЯЛ в изолированных перфузированных сердцах крыс (образцы брались у 3 крыс из группы и из 10 участков сердца). Общее число внутрисосудистых и инфильтрирующих ПЯЛ в претерпевшей реперфузию ткани сердца и прилежащих к коронарному руслу значительно уменьшалось под действием пептидного ингибитора ПКС Фиг.4b. Гистологическая оценка внутрисосудистых ПЯЛ, прилежащих к коронарному руслу в изолированных перфузированных сердцах крыс (у 3 крыс из группы забиралось по 10 образцов из 10 участков миокарда). Число ПЯЛ, прилежащих к коронарному руслу не различалось достоверно в зависимости от И/Р+ПЯЛ. Заштрихованные столбики касаются сердец, перфузированных без ПЯЛ, а черные столбики - сердец, перфузированных ПЯЛ. Все значения представляют собой среднее количество ПЯЛ/мм площади сердца ±m. Фиг.5. Определение высвобождения NO из фрагментов аорты крыс. Высвобождение NO эндотелием достоверно увеличивалось по сравнению с базальным уровнем во фрагментах, обработанных пептидным ингибитором ПКС Фиг.6. Высвобождение супероксида из ПЯЛ крыс. Высвобождение супероксида исследовалось на 5×106 ПЯЛ после стимуляции форбол-12-миристат-13-ацетатом (FMA) (15 nM). В качестве положительного контроля использовалась супероксиддисмутаза (COD) (10 µg/ml). Изменение оптической плотности ( Фиг.7. Зависимость ДРЛЖ от времени в имитациях и сердцах крыс, перфузируемых в режимах И/Р, И/Р, И/Р+ПЯЛ и И/Р+ПЯЛ+ Фиг.8. Исходное и конечное ДРЛЖ в мм рт.ст. в изолированных перфузируемых сердцах крыс перед ишемией (И) (исходно) и через 45 минут после реперфузии (Р) (конечное значение). Сердца перфузировались в присутствии или в отсутствии ПЯЛ. ПЯЛ вызывали значительную контрактильную дисфункцию, которая уменьшалась под действием пептидного ингибитора ПКС Фиг.9. Исходное и конечное ДРЛЖ+dP/dt max, выраженное в мм рт.ст./с в изолированных перфузированных сердцах крыс до ишемии (И) и после реперфузии (Р). Сердца перфузировались в присутствии или в отсутствие ПЯЛ. ПЯЛ вызывали значительную контрактильную дисфункцию, которая уменьшалась под действием пептидного ингибитора ПКС Фиг.10. Определение высвобождения NO из фрагментов аорты крыс; высвобождение NO эндотелием достоверно увеличивалось по сравнению с базальным уровнем во фрагментах, обработанных пептидным ингибитором ПКС Фиг.11. Высвобождение супероксида из ПЯЛ крыс. Высвобождение супероксида исследовалось на 5×106 ПЯЛ после стимуляции формил-метионил-лейцил-фенилаланином (fMLF) (200 nM). COD (10 µg/ml) использовалась в качестве позитивного контроля. Изменение оптической плотности ( Фиг.12. Зависимость ДРЛЖ от времени в имитациях и сердцах крыс, перфузируемых в режимах И/Р, И/Р+ПЯЛ и И/Р+ПЯЛ+ПКС Фиг.13. Исходное и конечное ДРЛЖ в мм рт.ст. в изолированных перфузируемых сердцах крыс перед ишемией (И) (исходно) и через 45 минут после реперфузии (Р) (конечное значение). Сердца перфузировались в присутствии или в отсутствии ПЯЛ. ПЯЛ вызывали значительную контрактильную дисфункцию, которая уменьшалась под действием пептидных ингибиторов ПКС Фиг.14. Исходное и конечное ДРЛЖ+dP/dt max, выраженное в мм рт.ст./с в изолированных перфузированных сердцах крыс до ишемии (И) и после реперфузии (Р). Сердца перфузировались в присутствии или в отсутствии ПЯЛ. ПЯЛ вызывали значительную контрактильную дисфункцию, которая уменьшалась под действием пептидных ингибиторов ПКС Фиг.15. Гистологическая оценка общего числа внутрисосудистых и инфильтрирующих ПЯЛ в изолированных перфузированных сердцах крыс (образцы брались у 3 крыс из группы и из 10 участков сердца). Общее число внутрисосудистых и инфильтрирующих ПЯЛ в претерпевшей реперфузию ткани сердца и прилежащих к коронарному руслу значительно уменьшалось под действием пептидных ингибиторов ПКС Фиг.16. Гистологическая оценка внутрисосудистых ПЯЛ, прилежащих к коронарному руслу в изолированных перфузированных сердцах крыс. Количество ПЯЛ, прилежащих к коронарному руслу в сердцах, обработанных пептидными ингибиторами ПКС Фиг.17. Определение высвобождения NO из фрагментов аорты крыс. Высвобождение NO эндотелием достоверно увеличивалось по сравнению с базальным уровнем во фрагментах, обработанных пептидными ингибиторами ПКС Фиг.18. Высвобождение супероксида из ПЯЛ крыс. Высвобождение супероксида исследовалось на 5×106 ПЯЛ после стимуляции FMA (15 nM). COD (10 µg/ml) использовалась в качестве позитивного контроля. Изменение оптической плотности ( Фиг.19. Зависимость ДРЛЖ от времени в имитациях и сердцах крыс, перфузируемых в режимах И/Р, И/Р+ПЯЛ и И/Р+ПЯЛ+ПКС Фиг.20. Исходное и конечное ДРЛЖ в мм рт.ст. в изолированных перфузируемых сердцах крыс перед ишемией (И) (исходно) и через 45 минут после реперфузии (Р) (конечное значение). Сердца перфузировались в присутствии или в отсутствии ПЯЛ. ПЯЛ вызывали значительную контрактильную дисфункцию, которая уменьшалась под действием ПКС Фиг.21. Исходное и конечное ДРЛЖ+dP/dt max, выраженное в мм рт.ст./с в изолированных перфузированных сердцах крыс до ишемии (И) и после реперфузии (Р). Сердца перфузировались в присутствии или в отсутствии ПЯЛ; ПЯЛ вызывали значительную контрактильную дисфункцию, которая уменьшалась под действием ПКС Фиг.22. Высвобождение супероксида из ПЯЛ крыс. Высвобождение супероксида исследовалось на 5×106 ПЯЛ после стимуляции FМА (15 nM). Изменение оптической плотности ( Фиг.23а. Гистологическая оценка общего числа внутрисосудистых и инфильтрирующих ПЯЛ в изолированных перфузированных сердцах крыс (образцы брались у 3 крыс из группы и из 10 участков сердца). Общее число внутрисосудистых и инфильтрирующих ПЯЛ в претерпевшей реперфузию ткани сердца и прилежащих к коронарному руслу уменьшалось под действием пептидного активатора ПКС Фиг.23b. Гистологическая оценка внутрисосудистых ПЯЛ, прилежащих к коронарному руслу в образцах изолированных перфузированных сердец крыс, бравшихся у 3 крыс из группы и из 10 участков сердца. Количество ПЯЛ, прилежащих к коронарному руслу, уменьшалось под действием пептидного активатора ПКС Фиг.24. Зависимость конечного диастолического давления в полости левого желудочка (ДДЛЖ) от времени в имитациях и сердцах крыс, перфузируемых в режимах И/Р, И/Р+ПЯЛ и И/Р+ПЯЛ+ПКС ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ Настоящее изобретение представляет собой раствор для консервации, перфузии и/или реперфузии органов, в особенности сердца. Раствор содержит пептидный(ые) ингибитор(ы) протеинкиназы С В предпочтительном воплощении пептидный ингибитор ПКС В предпочтительном воплощении пептидный(ые) ингибитор(ы) или пептидный(ые) активатор(ы) растворены в растворе хлорида натрия, предпочтительно изотоническом (0.9% NaCl). Пептидные ингибитор(ы) могут также растворяться в известных консервирующих растворах, таких как растворы Кребса-Гензелейта, UW, Ст.Томас II, Коллинза, Станфордском и подобных. Раствор может также содержать натрий (Na+), калий (K+), кальций (Ca 2+), магний (Mg2+), глутамат, аргинин, аденозин, маннитол, аллопуринол, глутатион, раффмозу и лактобиониковую кислоту в концентрациях приблизительно 4-7 мМ, приблизительно 0.2-0.3 мМ, приблизительно 108-132 мМ, приблизительно 13-16 мМ, приблизительно 18-22 мМ, приблизительно 2-4 мМ, приблизительно 0.5-1 мМ, приблизительно 27-33 мМ, приблизительно 0.9-1.1 мМ, приблизительно 2.7-3.3 мМ, приблизительно 25-35 мМ, и приблизительно 80-120 мМ, соответственно. Na+ может быть в форме NaOH; K+ - в форме KCl и/или KH2PO 4, оптимально в соотношении примерно 2-3.5 мМ KCl и примерно 2-3.5 мМ KH2PO4; Ca2+ может присутствовать в форме CaCl2; и Mg2 может быть в форме MgCl2. Желательно поддерживать физиологический pH раствора - около 7,2-7,4. Данный раствор может быть использован во время всех фаз трансплантации органов, особенно сердца, включая следующие (но не ограничиваясь ими): 1) изоляцию органа от донора (кардиоплегический раствор); 2) консервацию органа (хранение и транспортировка в условиях гипотермии); и 3) имплантация органа реципиенту (раствор для реперфузии). Во время фазы перфузии или реперфузии, особенно это касается сердца, желательно поддерживать скорость перфузии органа около 1 мл/мин в течение приблизительно 5 мин. Скорость перфузии может меняться, но она не должна превышать приблизительно 25 мл/мин. В целом, скорость перфузии не должна быть столь высокой, чтобы создавать чрезмерное давление на сосудистую систему органа. Раствор по изобретению можно приготовить следующим образом: 1) растворить пептидный(ые) ингибитор(ы) и другие компоненты в дистиллированной воде; 2) довести pH до приблизительно 7.2-7.4, например, с помощью NaOH; и 3) простерилизовать раствор, например с помощью фильтрации через 0.2 µm фильтр. Стерилизованный раствор должен затем храниться в условиях, изолированных от возможных загрязнителей окружающей среды. Специалист может, используя предшествующее описание и следующие за ним иллюстрирующие примеры, без дальнейших пояснений приготовить и использовать компоненты настоящего изобретения и использовать заявленные способы. Следующий пример приведен для иллюстрации настоящего изобретения. Необходимо иметь в виду, что сфера применения настоящего изобретения не ограничивается специфическими условиями или деталями, описанными в примере. Пример 1. Эффекты пептидного ингибитора ПКС Крысы-самцы Sprague Dawley (275-325 g, Ace Animals, Boyertown, PA) были подвергнуты анестезии пентобарбиталом натрия 60 мг/кг внутрибрюшинно (в/б). Также в/б вводилась натриевая соль гепарина (1,000 U). Сердца были быстро удалены, восходящие аорты канюлированы, после чего была начата ретроградная перфузия сердца модифицированными буфером Кребса при температуре 37°С и постоянном давлении 80 мм рт.ст. Буфер Кребса имел следующий состав, ммоль/л: 17 глюкозы, 120 NaCl, 25 NaHCO3, 2.5 CaCl2, 0.5 ЭДТА, 5.9 KCl, и 1.2 MgCL. Перфузирующий раствор аэрировался смесью из 95% O2 и 5% CO2 , pH его поддерживалось на уровне 7.3-7.4. Два боковых разъема в перфузионной линии, находившихся проксимально по отношению к входной канюле позволяли вводить ПЯЛ, плазму без пептидного ингибитора ПКС ДРЛЖ, +dP/dtmax, и коронарный кровоток измерялись каждые 5 минут в течение 15 минут для того, чтобы уравновесить сердца и получить исходные измерения. ДРЛЖ определялось как конечное систолическое давление в левом желудочке минус конечное диастолическое давление в левом желудочке. Через 15 минут скорость циркуляции буфера Кребса снижалась до нуля на 20 минут с целью создания глобальной ишемии. После реперфузии в сердца вводились в течение 5 минут 200×106 ПЯЛ, взвешенных в 5 мл буфера Кребса плюс 5 мл плазмы со скоростью 1 мл/мин. В некоторых экспериментах пептидный ингибитор ПКС Использовались следующие группы изолированных перфузируемых сердец: Группа 1: Сердца - имитации ишемии/реперфузии (И/Р) не подвергались ишемии и не перфузировались ПЯЛ, но перфузировались 5 мл плазмы (1 мл/мин) на 35-й минуте (в то же самое время, когда в сердца И/Р вводились бы 5 мл плазмы, 15 минут исходных записей плюс 20 минут ишемии). Эти сердца представляют собой контрольную группу, призванную установить, способно ли изолированное сердце крысы поддерживать ДРЛЖ и + dP/dtm в течение 80-минутного протокола (n=6). Группа 2: Сердца - имитации И/Р + пептидный ингибитор ПКС Группа 3: Сердца И/Р в течение 20 минут подвергались ишемии и перфузировались 5 мл плазмы (1 мл/мин) в течение первых 5 минут реперфузии, но не перфузировались ПЯЛ. Эти сердца представляли собой контрольную группу, призванную продемонстрировать, что 20-минутная ишемия с последующей реперфузией приводят к станнингу миокарда, но ДРЛЖ и + dP/dtmax восстановятся к исходным значениям максимум к концу 45-минутного периода реперфузии (n=6). Группа 4: Сердца И/Р + пептидный ингибитор ПКС Группа 5: Сердца И/Р+ПЯЛ подвергались ишемии в течение 20 минут и перфузировались 5 мл плазмы (1 мл/мин) и ПЯЛ (взвешенными в 5 мл буфера Кребса) во время первых 5 минут реперфузии. Эти сердца представляли собой контрольную группу, призванную установить, приводит ли 20-минутная ишемия с последующей реперфузией в течение 45 минут в присутствии ПЯЛ (200×10 6) к стойкой сократительной дисфункции сердца в течение всего 45-минутного периода реперфузии по сравнению с исходными значениями (n=6). Группа 6: Сердца И/Р+ПЯЛ + пептидный ингибитор ПКС (1 µM) подвергались ишемии в течение 20 минут и перфузировались 1 µM пептидного ингибитора ПКС Группа 7: Сердца И/Р+ПЯЛ + пептидный ингибитор ПКС (2.5 µМ) подвергались ишемии в течение 20 минут и перфузировались 2.5 µМ пептидного ингибитора ПКС Группа 8: Сердца И/Р+ПЯЛ + пептидный ингибитор ПКС (5 µМ) подвергались ишемии в течение 20 минут и перфузировались 5 µМ пептидного ингибитора ПКС Группа 9: Сердца И/Р+ПЯЛ + пептидный ингибитор ПКС Данные регистрировались каждые 5 минут в течение 45 минут после реперфузии. После завершения каждого эксперимента левый желудочек был изолирован, фиксирован в 4% растворе параформальдегида и хранился при температуре 4°С до последующего гистологического анализа. На фиг.1 показана зависимость сократительной функции сердца (то есть, ДРЛЖ) от времени. Результаты, полученные в группах имитации И/Р, И/Р, И/Р+ПЯЛ + пептидный ингибитор ПКС Для того чтобы определить, не обладает ли пептидный ингибитор ПКС прямым инотропным действием на сократительную функцию сердца, неишемизированные сердца из группы имитации И/Р перфузировались пептидным ингибитором ПКС На фиг.2 и 3 показаны исходные и конечные значения ДРЛЖ и + dP/dtmax в изолированных перфузируемых сердцах крыс. Исходные значения были сходными во всех группах. Тем не менее, конечные ДРЛЖ и + dP/dtmax (45 минут после реперфузии) сердец И/Р, реперфузированных с ПЯЛ, достоверно снизились (p<0.01) соответственно на 47±7% и 41±7% по сравнению с исходными значениями. Пептидный ингибитор ПКС Повреждение сердца, ассоциированное с И/Р, в этой модели тесно коррелировало со значительным количеством ПЯЛ, инфильтрировавших миокард в течение 45-минутного периода реперфузии. Во время реперфузии существенное число ПЯЛ мигрировало в миокард, где их число возросло к концу периода реперфузии от менее чем 25 ПЯЛ/мм2 в группе имитации И/Р до более чем 180 ПЯЛ/мм2 в сердцах группы И/Р+ПЯЛ (фиг.4а). Напротив, в сердцах, подвергшихся И/Р+ПЯЛ + пептидный ингибитор ПКС Прилегание ПЯЛ к эндотелию коронарных сосудов также исследовалось в рамках оценки общего количества внутрисосудистых и инфильтрирующих ПЯЛ. Как показано на фиг.4b, число прилежащих к коронарному эндотелию ПЯЛ достоверно не уменьшилось в сердцах группы И/Р+ПЯЛ + пептидный ингибитор ПКС Другой механизм кардиопротективного действия пептидного ингибитора ПКС Пример 2. Действие пептидного ингибитора ПКС Эксперименты с пептидными ингибиторами ПКС Использовались следующие группы изолированных перфузируемых сердцах крыс: Группа 1: Сердца-имитации И/Р не подвергались ишемии и не перфузировались с ПЯЛ, но перфузировались с 5 мл плазмы (1 мл/мин) на 35 минуте перфузии (в то же самое время, когда в сердца из группы И/Р вводились бы 5 мл плазмы, 15 минут записи исходных значений плюс 20 минут ишемии). Эти сердца представляли собой контрольную группу, призванную установить, может ли изолированное сердце крысы поддерживать стабильный уровень ДРЛЖ и + dP/dtmax в течение 80-минутного протокола (n=6). Группа 2: Имитация И/Р + пептидный ингибитор ПКС Группа 3: Сердца И/Р подвергались ишемии на 20 минут и перфузировались 5 мл плазмы (1 мл/мин) в течение первых 5 мин реперфузии, но не перфузировались с ПЯЛ. Эти сердца представляют собой контрольную группу, целью которой было установить, что 20 минут ишемии с последующей реперфузией вызывают станнинг миокарда, но ДРЛЖ и + dP/dtmax восстанавливаются к исходным значениям к концу 45-минутного периода реперфузии (n=6). Группа 4: И/Р + пептидный ингибитор ПКС Группа 5: Сердца группы И/Р+ПЯЛ подвергались 20-минутной ишемии и перфузировались в течение первых 5 минут реперфузии 5 мл плазмы (1 мл/мин) и ПЯЛ (в виде суспензии в 5 мл буфера Кребса). Эти сердца представляли собой контрольную группу, призванную установить, вызывает ли 20-минутная ишемия с последующей 45-минутной реперфузией в присутствии ПЯЛ (200×10 6) стойкую сократительную дисфункцию сердца, сохраняющуюся в течение всего 45-минутного периода реперфузии, по сравнению с исходными значениями (n=9). Группа 6: И/Р+ПЯЛ + пептидный ингибитор ПКС Группа 7: И/Р+ПЯЛ + пептидный ингибитор ПКС Эти сердца представляли собой группу, призванную установить эффективность ингибирования ПКС Группа 8: И/Р+ПЯЛ + пептидный ингибитор ПКС Группа 9: И/Р+ПЯЛ + пептидный ингибитор ПКС Предыдущие исследования показали, что сердца-имитации И/Р при введении ПЯЛ не претерпевали никаких изменений по сравнению с исходными контрольными значениями (Lefer и др., Circulation 100: 178-184, 1999). Результаты фиксировались каждые 5 минут в течение 45 минут после реперфузии. После каждого эксперимента левый желудочек изолировался, фиксировался в 4% параформальдегиде и хранился перед последующим гистрологическим анализом при 4°С. Рисунок 7 демонстрирует зависимость сократительной функции сердца (ДРЛЖ) от времени в группах имитации И/Р, И/Р, И/Р+ПЯЛ + пептидный ингибитор ПКС Для того чтобы установить, обладает ли пептидный ингибитор ПКС Фиг.8 и 9 демонстрируют исходные и конечные значения ДРЛЖ и + dP/dtmax изолированных перфузируемых сердец крыс соответственно. Между исходными значениями во всех изучаемых группах не было достоверной разницы. Также не было достоверных различий между исходными и конечными значениями ДРЛЖ и + dP/dt в группах имитации И/Р, И/Р, имитации И/Р + пептидный ингибитор ПКС Присутствие пептидного ингибитора ПКС В группе И/Р+ПЯЛ + пептидный ингибитор ПКС Чтобы уточнить, реализуется ли кардиозащитный эффект пептидного ингибитора ПКС Ацетилхолин (Ach, 500 nM) использовался при данном количественном анализе в качестве положительного контроля и стимулировал эндотелий, вызывая превышение базальных значений на 3.75±0.58 пмоль NO/мг ткани. L-NAME использовался в качестве еще одного контроля с целью снижения базального высвобождения NO до нуля. Выработка NO, стимулированная и ацетилхолином, и пептидным ингибитором ПКС Еще одним механизмом реализации кардиозащитных эффектов (т.е. влияния на ДРЛЖ) пептидного ингибитора ПКС Пример 3. Эффекты комбинации пептидных ингибиторов ПКС Эксперименты с пептидными ингибиторами ПКС Использовались следующие группы изолированных перфузируемых сердец крыс: Группа 1: Сердца-имитации И/Р не подвергались ишемии и не перфузировались с ПЯЛ, но перфузировались с 5 мл плазмы (1 мл/мин) на 35 минуте перфузии (в то же самое время, когда в сердца из группы И/Р вводились бы 5 мл плазмы, 15 минут записи исходных значений плюс 20 минут ишемии). Эти сердца представляли собой контрольную группу, призванную установить, может ли изолированное сердце крысы поддерживать стабильный уровень ДРЛЖ и + dP/dtmax в течение 80-минутного протокола (n=6). Группа 2: Имитация И/Р + пептидные ингибиторы ИКС Группа 3: Сердца И/Р подвергались ишемии на 20 минут и перфузировались 5 мл плазмы (1 мл/мин) в течение первых 5 мин реперфузии, но не перфузировались с ПЯЛ. Эти сердца представляли собой контрольную группу, целью которой было установить, что 20 минут ишемии с последующей реперфузией вызывают станнинг миокарда, но ДРЛЖ и + dP/dtmax восстанавливаются к исходным значениям к концу 45-минутного периода реперфузии (n=6). Группа 4: И/Р + пептидные ингибиторы ПКС Группа 5: Сердца группы И/Р+ПЯЛ подвергались 20-минутной ишемии и перфузировались в течение первых 5 минут реперфузии 5 мл плазмы (1 мл/мин) и ПЯЛ (в виде суспензии в 5 мл буфера Кребса). Эти сердца представляли собой контрольную группу, призванную установить, вызывает ли 20-минутная ишемия с последующей 45-минутной реперфузией в присутствии ПЯЛ (200×106) стойкую сократительную дисфункцию сердца, сохраняющуюся в течение всего 45-минутного периода реперфузии, по сравнению с исходными значениями (n=11). Группа 6: И/Р+ПЯЛ + пептидные ингибиторы ПКС Группа 7: И/Р+ПЯЛ + пептидные ингибиторы ПКС Группа 8: И/Р+ПЯЛ + пептидные ингибиторы ПКС Группа 9: И/Р+ПЯЛ + пептидные ингибиторы ПКС Из графика на фиг.12 видно, что комбинация пептидных ингибиторов ПКС На фиг.13 и 14 показаны начальные и конечные значения соответственно ДРЛЖ и + dP/dt max изолированных перфузируемых сердец. Как и ожидалось, подобно наблюдавшемуся в Примерах 1 и 2, исходные и конечные значении ДРЛЖ и + dP/dtmax в группе И/Р+ПЯЛ достоверно различались, при этом ДРЛЖ к 45-й минуте постреперфузии снизилось приблизительно на 50%, а + dP/dtmax - на 45% по сравнению с исходными значениями (p<0.01). Присутствие пептидных ингибиторов ПКС С другой стороны, повышение дозы пептидного ингибитора ПКС Кардиозащитные эффекты комбинации пептидных ингибиторов ПКС Ассоциированное с И/Р повреждение сердца в этой модели тесно коррелировало с существенным числом ПЯЛ, инфильтрировавших миокард в течение 45-минутного периода реперфузии. Во время реперфузии значительное количество ПЯЛ мигрировало в миокард, где их число к концу периода реперфузии возросло с менее 25 ПЯЛ /мм2 в группе имитации И/Р до более 175 ПЯЛ/мм2 в сердцах И/Р+ПЯЛ (фиг.15). Напротив, в сердцах группы И/Р+ПЯЛ + пептидные ингибиторы ПКС Прилегание ПЯЛ к эндотелию коронарных сосудов также исследовалось в рамках оценки общего количества внутрисосудистых и инфильтрирующих ПЯЛ. Как показано на фиг.16, число прилегающих к коронарному эндотелию ПЯЛ уменьшалось в сердцах группы И/Р+ПЯЛ + пептидные ингибиторы ПКС На фиг.17 в эндотелии сердец, обработанных пептидными ингибиторами ПКС Сравнение воздействия пептидных ингибиторов ПКС В анализе на NO ацетилхолин (500 нМ) использовался в качестве положительного контроля. При его применении происходит достоверное увеличение высвобождения NO по сравнению с базальным высвобождением NO. L-NAME использовался в качестве другого контроля в целью снижения базального высвобождения NO до нуля. Продукция NO, вызванная как ацетилхолином, так и пептидными ингибиторами, полностью ингибировалась при обработке эндотелия при помощи L-NAME (400 мкМ). Другой механизм кардиопротективных эффектов пептидных ингибиторов ПКС Все примеры свидетельствуют о том, что присутствие достаточного количества пептидного ингибитора ПКС Пример 4 - Эффекты пептидного активатора ПКС Эксперименты с использованием пептидного активатора ПКС Использовались следующие группы изолированных перфузированных сердец крыс: Группа 1: Сердца из группы с имитацией И/Р не подвергались воздействию ишемии и не перфузировались с ПЯЛ, но перфузировались 5 мл плазмы (1 мл/мин) в течение 35 минут (в тот момент, когда сердца, подвергающиеся И/Р, обрабатывались 5 мл плазмы, в течение 15 минут проводилась исходная регистрация, а в течение 20 мин создавались условия ишемии). Эти сердца составляли контрольную группу, которая служила для определения, способны ли изолированные сердца крыс поддерживать ДРЛЖ и + dP/dtmax по протоколу в течение 80 минут (n=6). Группа 2: Сердца с имитацией И/Р + сердца с пептидным ингибитором ПКС Группа 3: Сердца, подвергающиеся И/Р, в течение 20 минут подвергались воздействию ишемии и перфузировались при помощи 5 мл плазмы (1 мл/мин) в течение первых 5 минут реперфузии, но не перфузировались ПЯЛ. Эти сердца представляли собой контрольную группу, используемую для решения вопроса о том, вызывает ли ишемия, действующая в течение 20 минут и следующая за ней реперфузия, эффект оглушения в сердце, однако ДРЛЖ и + dP/dtmax возвращались к исходным значениям (начальным значениям) к конце 45-минутного периода реперфузии (n=6). Группа 4: Сердца, подвергавшиеся воздействию И/Р+обработанные пептидным активатором ПКС Группа 5: Сердца, на которые воздействовали с использованием И/Р и ПЯЛ, в течение 20 минут подвергались ишемии и перфузировались 5 мл плазмы (1 мл/мин) и ПЯЛ (в виде суспензии в 5 мл буфера Кребса) в течение первых 5 минут реперфузии. Эти сердца представляли контрольную группу, использующуюся для определения, приводит ли ишемия в течение 20 минут, за которой следует реперфузия в течение 45 минут в присутствии ПЯЛ (200×106 ), к развитию устойчивой сократительной дисфункции сердца в течение 45-минутного реперфузионного периода по сравнению с начальными и исходными значениями (n=10). Группа 6: Сердца, на которые воздействовали с использованием И/Р+ПЯЛ + пептидного активатора (1 мкМ), подвергались воздействию ишемии в течение 20 минут и перфузировались с использованием пептидного ингибитора ПКС Группа 7: Сердца, на которые воздействовали с использованием И/Р+ПЯЛ + пептидного активатора ПКС Группа 8: Сердца, на которые воздействовали с использованием И/Р+ПЯЛ + пептидного активатора ПКС В предыдущих исследованиях было показано, что для сердец, подвергающихся воздействию И/Р и ПЯЛ, не наблюдается изменений по сравнению с исходными контрольными значениями (Lefer и др., Chirculation 100; 178-184, 1999). Данные регистрировались через каждые 5 минут в течение 45 минут после реперфузии. После каждого эксперимента проводилась изоляция левого желудочка и фиксация при помощи параформальдегида. Препараты сохранялись при температуре 4°С для проведения дальнейшего гистологического исследования. На фиг.19 показан характер сократительной функции сердца (ДРЛЖ) для следующих групп: имитации И/Р, И/Р, И/Р+ПЯЛ + пептидный активатор ПКС С целью установления, оказывает ли пептидный активатор ПКС На фиг.20 и 21 показаны исходные и конечные значения ДРЛЖ и + dP/dtmax соответственно для перфузируемых изолированных сердец. Достоверных различий между начальными исходными значениями во всех исследуемых группах выявлено не было. Также не выявлялось достоверных различий между исходными и конечными значениями ДРЛЖ и + dP/dtmax для групп имитации И/Р, И/Р, имитации И/Р + пептидный активатор ИКС Присутствие пептидного активатора ПКС Доза 1 мкМ пептидного активатора ПКС Механизм, который способствует кардиопротективным эффектам (т.е. ДРЛЖ) пептидного активатора ПКС Хотя некоторые из предпочтительных воплощений данного изобретения были описаны, для специалистов очевидно, что различные модификации описанных и показанных здесь воплощений могут быть выполнены без отклонения от его сути и объема. В соответствии с этим предполагается, что данное изобретение ограничивается только прилагаемой формулой изобретения. Формула изобретения1. Раствор для перфузии, консервации и/или реперфузии изъятого органа, содержащий по меньшей мере один пептидный ингибитор протеинкиназы С 2. Раствор по п.1, в котором пептидные ингибиторы растворены в солевом растворе. 3. Раствор по п.1, дополнительно содержащий хлорид калия. 4. Раствор по п.1, где орган представляет собой сердце. 5. Раствор по п.1, где орган представляет собой орган млекопитающего. 6. Раствор по п.5, где орган млекопитающего представляет собой орган человека. 7. Раствор по п.1, где орган представляет собой орган, предназначенный для трансплантации. 8. Раствор по п.1, в котором пептидные ингибиторы/активатор меристилированы. 9. Способ сохранения органов, предназначенных для трансплантации, включающий перфузирование органа раствором по п.1. 10. Способ по п.9, при котором пептидные ингибиторы/активатор растворены в солевом растворе. 11. Способ по п.9, дополнительно включающий использование хлорида калия. 12. Способ по п.9, при котором по меньшей мере один ингибитор ПКС 13. Способ по п.9, при котором по меньшей мере один активатор ПКС 14. Способ по п.9, при котором по меньшей мере один ингибитор ПКС 15. Способ по п.9, при котором концентрация по меньшей мере одного пептидного ингибитора ПКС 16. Способ по п.9, при котором концентрация по меньшей мере одного пептидного активатора ПКС 17. Способ по п.9, при котором концентрация по меньшей мере одного пептидного ингибитора ПКС 18. Способ по п.9, при котором орган представляет собой сердце. 19. Способ по п.9, при котором орган представляет собой орган млекопитающего. 20. Способ по п.19, при котором орган млекопитающего представляет собой орган человека. 21. Способ по п.9, при котором орган представляет собой орган, предназначенный для трансплантации. 22. Способ по п.9, при котором пептидные ингибиторы/активатор меристилированы. 23. Способ по п.9, при котором перфузию проводят со скоростью менее 20 мл/мин. 24. Способ по п.9, при котором перфузию проводят со скоростью около 1 мл/мин. 25. Способ по п.9, при котором перфузия представляет собой ретроградную перфузию. 26. Способ по п.9, при котором перфузию проводят в течение примерно 5 мин. 27. Способ защиты ишемизированного органа от повреждений, включающий перфузию органа раствором по п.1. 28. Способ по п.27, при котором пептидные ингибиторы/активаторы растворены в солевом растворе. 29. Способ по п.27, дополнительно включающий использование хлорида калия. 30. Способ по п.27, при котором по меньшей мере один ингибитор ПКС 31. Способ по п.27, при котором по меньшей мере один активатор ПКС 32. Способ по п.27, при котором по меньшей мере один ингибитор ПКС 33. Способ по п.27, при котором концентрация по меньшей мере одного пептидного ингибитора ПКС 34. Способ по п.27, при котором концентрация по меньшей мере одного пептидного активатора ПКС 35. Способ по п.27, при котором концентрация по меньшей мере одного пептидного ингибитора ПКС 36. Способ по п.27, при котором орган представляет собой сердце. 37. Способ по п.27, при котором орган представляет собой орган млекопитающего. 38. Способ по п.37, при котором орган представляет собой орган человека. 39. Способ по п.27, при котором орган представляет собой орган, предназначенный для трансплантации. 40. Способ по п.27, при котором пептидные ингибиторы/активатор меристилированы. 41. Способ по п.27, при котором перфузию проводят со скоростью менее 20 мл/мин. 42. Способ по п.27, при котором перфузию проводят со скоростью около 1 мл/мин. 43. Способ по п.27, при котором перфузия представляет собой ретроградную перфузию. 44. Способ по п.27, при котором перфузию проводят в течение примерно 5 мин. 45. Способ уменьшения дисфункции органа после ишемии, включающий перфузию органа раствором по п.1. 46. Способ по п.45, при котором пептидные ингибиторы/активаторы растворены в солевом растворе. 47. Способ по п.45, дополнительно включающий использование хлорида калия. 48. Способ по п.45, при котором по меньшей мере один ингибитор ПКС 49. Способ по п.45, при котором по меньшей мере один активатор ПКС 50. Способ по п.45, при котором по меньшей мере один ингибитор ПКС 51. Способ по п.45, при котором концентрация по меньшей мере одного пептидного ингибитора ПКС 52. Способ по п.45, при котором концентрация по меньшей мере одного пептидного активатора ПКС 53. Способ по п.45, при котором концентрация по меньшей мере одного пептидного ингибитора ПКС 54. Способ по п.45, при котором орган представляет собой сердце. 55. Способ по п.45, при котором орган представляет собой орган млекопитающего. 56. Способ по п.55, при котором орган представляет собой орган человека. 57. Способ по п.45, при котором орган представляет собой орган, предназначенный для трансплантации. 58. Способ по п.45, при котором пептидные ингибиторы/активатор меристилированы. 59. Способ по п.45, при котором перфузию проводят со скоростью менее 20 мл/мин. 60. Способ по п.45, при котором перфузию проводят со скоростью менее 1 мл/мин. 61. Способ по п.45, при котором перфузия представляет собой ретроградную перфузию. 62. Способ по п.45, при котором перфузию проводят в течение примерно 5 мин. 63. Способ поддержания высвобождения оксида азота в ишемизированном органе, включающий перфузию органа раствором по п.1. 64. Способ по п.63, при котором пептидные ингибиторы/активаторы растворены в солевом растворе. 65. Способ по п.63, дополнительно включающий использование хлорида калия. 66. Способ по п.63, при котором по меньшей мере один ингибитор ПКС 67. Способ по п.63, при котором по меньшей мере один активатор ПКС 68. Способ по п.63, при котором по меньшей мере один ингибитор ПКС 69. Способ по п.63, при котором концентрация по меньшей мере одного пептидного ингибитора ПКС 70. Способ по п.63, при котором концентрация по меньшей мере одного пептидного активатора ПКС 71. Способ по п.63, при котором концентрация по меньшей мере одного пептидного ингибитора ПКС 72. Способ по п.63, при котором орган представляет собой сердце. 73. Способ по п.63, при котором орган представляет собой орган млекопитающего. 74. Способ по п.73, при котором орган млекопитающего представляет собой орган человека. 75. Способ по п.63, при котором орган представляет собой орган, предназначенный для трансплантации. 76. Способ по п.63, при котором пептидные ингибиторы/активатор меристилированы. 77. Способ по п.63, при котором перфузию проводят со скоростью менее 20 мл/мин. 78. Способ по п.63, при котором перфузию проводят со скоростью менее 1 мл/мин. 79. Способ по п.63, при котором перфузия представляет собой ретроградную перфузию. 80. Способ по п.63, при котором перфузию проводят в течение примерно 5 минут. 81. Способ защиты органа от повреждения после изоляции от системы кровообращения, включающий перфузию органа раствором по п.1. 82. Способ по п.81, при котором пептидные ингибиторы/активаторы растворены в солевом растворе. 83. Способ по п.81, дополнительно включающий использование хлорида калия. 84. Способ по п.81, при котором по меньшей мере один ингибитор ПКС 85. Способ по п.81, при котором по меньшей мере один активатор ПКС 86. Способ по п.81, при котором по меньшей мере один ингибитор ПКС 87. Способ по п.81, при котором концентрация по меньшей мере одного пептидного ингибитора ПКС 88. Способ по п.81, при котором концентрация по меньшей мере одного пептидного активатора ПКС 89. Способ по п.81, при котором концентрация по меньшей мере одного пептидного ингибитора ПКС 90. Способ по п.81, при котором орган представляет собой сердце. 91. Способ по п.81, при котором орган представляет собой орган млекопитающего. 92. Способ по п.91, при котором орган млекопитающего представляет собой орган человека. 93. Способ по п.81, при котором орган представляет собой орган, предназначенный для трансплантации. 94. Способ по п.81, при котором пептидные ингибиторы/активатор меристилированы. 95. Способ по п.81, при котором перфузию проводят со скоростью менее 20 мл/мин. 96. Способ по п.81, при котором перфузию проводят со скоростью менее 1 мл/мин. 97. Способ по п.81, при котором перфузия представляет собой ретроградную перфузию. 98. Способ по п.81, при котором перфузию проводят в течение примерно 5 мин. Популярные патенты: 2271095 Многофункциональное устройство ... углом привод с измельчающим устройством с помощью устройства поворота и фиксации и осуществить необходимую переналадку. Формула изобретения 1. Многофункциональное устройство, содержащее раму и установленное на ней с возможностью поворота и фиксации измельчающее устройство, включающее рабочий орган с приводом, камеру измельчения и зоны загрузки и выгрузки материала, отличающееся тем, что измельчающее устройство установлено с возможностью поворота и фиксации относительно рамы под углом 0...360°, а устройство поворота и фиксации выполнено в виде, по меньшей мере, одной стойки и оси поворота, которая посредством втулок закреплена к верхней части стойки, причем с одной стороны на ... 2108013 Рабочий орган культиватора ... упругий элемент выполнены из разнокачественных материалов; носок S-образной подпружиненной стойки снабжен нишей для установки упругого элемента; ниша носка стойки выполнена в виде Л-образного выступа, выполненного парой параллельных прорезей и деформацией основного материала в направлении от нижней грани стойки; фронтальная часть носка S-образной стойки снабжена режущей кромкой на лезвии; лезвие носка образовано прокаткой нагретой торцевой части S-образной стойки; упругий элемент выполнен плоским, а его фронтальная часть снабжена режущей кромкой на одностороннем лезвии; торцевые участки упругого элемента выполнены скошенными назад и снабжены лезвиями; упругий элемент снабжен ... 2066320 Производные тиазола, способ их получения и способ борьбы с грибками ... Фунгицидные композиции часто формируются и транспортируются в концентрированной форме, которую впоследствии разбавляют перед применением. Наличие небольших количеств носителя, который является поверхностно-активным агентом, облегчает этот процесс разбавления. Таким образом, предпочтительно по крайней мере один носитель в композиции согласно изобретения является поверхностно-активным агентом. Например, композиция может содержать по крайней мере два носителя, один из которых по крайней мере является поверхностно-активным агентом. Поверхностно-активным агентом может быть эмульгирующий агент, диспергирующий агент или увлажняющий агент; он может быть неионным или ионным. Примеры ... 2456799 Ловушка для поимки животных, обитающих в земле ... расположена в шестом отверстии 35 втулки 13, описанной далее. При этом часть стержня 14 между втулкой 13 и пятым отверстием 7 расположена внутри второй пружины 9, описанной далее.Втулка 13 представляет собой деталь цилиндрической формы. Во втулке 13 выполнено шестое отверстие 35 и седьмое отверстие 34. Шестое отверстие 35 выполнено соосно втулке 13. Шестое отверстие 35 выполнено сквозным. Диаметр шестого отверстия 35 выполнен больше диаметра стержня 14. Седьмое отверстие 34 выполнено перпендикулярно оси втулки 13. В седьмом отверстии 34 выполнена резьба. Втулка 13 соединена со стержнем 14 при помощи переключателя 12, описанного далее.Переключатель 12 выполнен в виде стержня 14 с ... 2391804 Почвообрабатывающий каток ... почвы ограничена упорами, при этом поводки с брусьями катков дополнительно соединены посредством винтовых пружин, один конец которых неподвижно закреплен на брусьях катков, а второй - на поводках через регулировочные винтовые тяги, а на валах с шагом С закреплены неподвижно посредством спиц винтовые полосы шириной а, имеющие шаг t и составляющие угол с образующей цилиндрической поверхности, описывающей каток, при этом угол наклона проекций винтовых полос на любую поверхность, проходящую через ось катка, к оси катка определяют по выражению: где Н - максимальная высота необработанных гребней почвы для обработанного поля, мм; D - диаметр винтового катка, мм; С - расстояние между ... |
Еще из этого раздела: 2132610 Устройство обогрева сельскохозяйственных животных и птицы 2228022 Способ ведения виноградных кустов 2142331 Устройство для гомогенизации и гомогенизирующая головка 2260932 Способ уборки льна и тресты при неблагоприятных погодных условиях 2216908 Комбайн для уборки урожая с кустарников 2241344 Способ производства зеленого корма 2125366 Доильный аппарат 2488263 Система механической подачи недомолота для вторичного обмолота на возвратную доску 2463776 Система и способ для массовой валки деревьев 2384038 Устройство для посадки сеянцев, выращенных в контейнерах |
Изобретения в сельском хозяйстве
Обработка почвы в сельском и лесном хозяйствах
Посадка, посев, удобрение
Уборка урожая, жатва
Обработка и хранение продуктов полеводства и садоводства
Садоводство, разведение овощей, цветов, риса, фруктов, винограда, лесное хозяйство
Новые виды растений или способы их выращивания
Производство молочных продуктов
Животноводство, разведение и содержание птицы, рыбы, насекомых, рыбоводство, рыболовство
Поимка, отлов или отпугивание животных
Консервирование туш животных, или растений или их частей
Биоцидная, репеллентная, аттрактантная или регулирующая рост растений активность химических соединений или препаратов
Хлебопекарные печи, машины и прочее оборудование для хлебопечения
Машины или оборудование для приготовления или обработки теста
Обработка муки или теста для выпечки, способы выпечки, мучные изделия
|
|
||
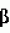 II (ПКС
II (ПКС 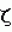 (ПКС
(ПКС 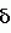 (ПКС
(ПКС 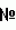
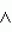 -нитро-L-аргинин метил эфиром (L-NAME). Все значения представлены в виде среднего ±m. Количество исследованных сердец представлено внизу столбиков. **p<0.01, по сравнению с конечным И/Р+ПЯЛ; нз = не значимо.
-нитро-L-аргинин метил эфиром (L-NAME). Все значения представлены в виде среднего ±m. Количество исследованных сердец представлено внизу столбиков. **p<0.01, по сравнению с конечным И/Р+ПЯЛ; нз = не значимо.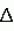 ) измерялось через 360 сек после добавления FMA (пиковый ответ). Высвобождение супероксида достоверно подавлялось пептидным ингибитором ПКС
) измерялось через 360 сек после добавления FMA (пиковый ответ). Высвобождение супероксида достоверно подавлялось пептидным ингибитором ПКС 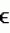 , наблюдается достоверно более выраженное высвобождение NO, особенно при использовании дозы 10 мкМ.
, наблюдается достоверно более выраженное высвобождение NO, особенно при использовании дозы 10 мкМ.